140 bài tập trắc nghiệm Hóa 11 Chương 2: Nitơ, Photpho có đáp án
Với các bài tập trắc nghiệm Hóa 11 Chương 2: Nitơ - Photpho có đáp án chi tiết đầy đủ các mức độ nhận biết, thông hiểu, vận dụng sẽ giúp học sinh ôn tập trắc nghiệm Hóa học 11.
140 bài tập trắc nghiệm Hóa 11 Chương 2: Nitơ, Photpho có đáp án
- 15 câu trắc nghiệm Nitơ có đáp án
- 16 câu trắc nghiệm Amoniac và muối amoni có đáp án
- 16 câu trắc nghiệm Axit nitric và muối nitrat có đáp án
- 15 câu trắc nghiệm Photpho có đáp án
- 15 câu trắc nghiệm Axit photphoric và muối photphat có đáp án
- 15 câu trắc nghiệm Phân bón hóa học có đáp án
- 16 câu trắc nghiệm Tính chất của nitơ, photpho có đáp án
- 4 câu trắc nghiệm Thực hành Tính chất của một số hợp chất nitơ, photpho có đáp án
- Đề kiểm tra 1 tiết Hóa học 11 Học kì 1 có đáp án (Bài số 2)
Trắc nghiệm Hóa 11 Chương 2 theo bài học
- Trắc nghiệm Hóa 11 Bài 7: Nitơ có đáp án
- Trắc nghiệm Hóa 11 Bài 8: Amoniac và muối amoni có đáp án
- Trắc nghiệm Hóa 11 Bài 9: Axit nitric và muối nitrat có đáp án
- Trắc nghiệm Hóa 11 Bài 10: Photpho có đáp án
- Trắc nghiệm Hóa 11 Bài 11: Axit photphoric và muối photphat có đáp án
- Trắc nghiệm Hóa 11 Bài 12: Phân bón hóa học có đáp án
- Trắc nghiệm Hóa 11 Bài 13 Luyện tập: Tính chất của nitơ, photpho có đáp án
- Trắc nghiệm Hóa 11 Bài 14: Bài thực hành 2: Tính chất của một số hợp chất nitơ, photpho có đáp án
Trắc nghiệm Nitơ có đáp án
Câu 1: Cấu hình electron nguyên tử của nitơ là
A. 1s22s22p1. B. 1s22s22p5.
C. 1s22s22p63s23p2. D. 1s22s22p3.
Đáp án: D
Câu 2: Khi có tia lửa điện hoặc ở nhiệt độ cao, nitơ tác dụng trực tiếp với ôxi tạo ra hợp chất X. Công thức của X là
A. N2O. B. NO2. C. NO. D. N2O5.
Đáp án: C
Câu 3: Nitơ thể hiện tính khử trong phản ứng với chất nào sau đây ?
A. H2. B. O2. C. Mg. D. Al.
Đáp án: B
Câu 4: Có thể thu được nitơ từ phản ứng nào sau đây ?
A. Đun nóng dung dịch bão hòa natri nitrit với amoni clorua.
B. Nhiệt phân muối bạc nitrat.
C. Cho bột Cu vào dung dịch HNO3 đặc nóng.
D. Cho muối amoni nitrat vào dung dịch kiềm.
Đáp án: A
Câu 5: Ở nhiệt độ thường, khí nitơ khá trơ về mặt hóa học. Nguyên nhân là do
A. trong phân tử N2 có liên kết ba rất bền.
B. trong phân tử N2, mỗi nguyên tử nitơ còn 1 cặp electron chưa tham gia liên kết.
C. nguyên tử nitơ có độ âm điện kemms hơn oxi.
D. nguyên tử nitơ có bán kính nhỏ.
Đáp án: A
Câu 6: Nung nóng 4,8 gam Mg trong bình phản ứng chứa 1 mol khí N2. Sau một thời gian, đưa bình về nhiệt độ ban đầu, thấy áp suất khí trong bình giảm 5% so với áp suất ban đầu. Thành phần phần trăm Mg đã phản ứng là
A. 37,5%. B. 25,0%. C. 50%. D. 75%.
Đáp án: D
Trong bình phản ứng cùng thể tích nhiệt độ do đó áp suất tỉ lệ với số mol, áp suất bình giảm 5% so với ban đầu ⇒ nN2 pư = 5% ban đầu = 0,05 mol
3Mg + N2 -toC→ Mg3N2
nMg = 3nN2 = 0,15
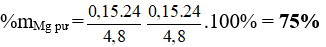
Câu 7: Hỗn hợp N2 và H2 trong bình phản ứng ở nhiệt độ không đổi. Sau thời gian phản ứng, áp suất các khí trong bình thay đổi 5% so với áp suất ban đầu. biết rằng số mol N2 đã phản ứng là 10%. Thành phần phần trăm số mol N2 trong hỗn hợp ban đầu là
A. 20%. B. 25%. C. 10%. D. 5%.
Đáp án: D
N2 + 3H2 -toC→ 2NH3
Áp suất thay đổi 5% so với áp suất ban đầu
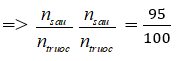
Giả sử trước phản ứng có 1 mol ⇒ sau phản ứng có 0,95 mol
ntrước – nsau = 2nN2 pư = 0,05 mol
nN2 ban đầu = 0,025 : 10% = 0,25 ⇒ %nN2 = 25%
Câu 8: Hỗn hợp khi X gồm N2 và H2 có tỉ khối hơi so với He bằng 1,8. Đun nóng trong bình kín một thời gian (có bột Fe làm xúc tác) thu được hỗn hợp khí Y có tỉ khối hơn sô với He bằng 2. Hiệu suất phản ứng tổng hợp NH3 là
A. 10%. B. 20%. C. 25%. D. 5%.
Đáp án: C
MX = 4.1,8 = 7,2
Xét 1 mol hỗn hợp gồm a mol N2 và b mol H2:
a + b = 1; 28a + 2b = 7,2 ⇒ a = 0,2; b = 0,8 (mol)
N2 + 3H2 → 2NH3
nY = 1 – 2a
Mà MY = 4.2 = 8; mY = mX = 7,2 ⇒ nY = 0,9 = 1 – 2a
⇒ a = 0,05 (mol). Vậy H = (0,05/0,2). 100% = 25%
Câu 9: Người ta sản xuất khi nitơ trong công nghiệp bằng cách nào sau đây?
A. Chưng cất phân đoạn không khí lỏng.
B. Nhiệt phân dung dịch NH4NO2 bão hoà.
C. Dùng photpho để đốt cháy hết oxi không khí.
D. Cho không khí đi qua bột đồng nung nóng
Đáp án: A
Câu 10: Hiệu suất của phản ứng giữa N2 và H2 tạo thành NH3 tăng nếu
A. giảm áp suất, tăng nhiệt độ.
B. giảm áp suất, giảm nhiệt độ.
C. tăng áp suất, tăng nhiệt độ.
D. tăng áp suất, giảm nhiệt độ.
Đáp án: D
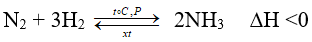
Chiều thuận của phản ứng có tổng số mol khí giảm ⇒ muốn tăng hiệu suất thì tăng áp suất
Chiều thuận của phản ứng là chiều tỏa nhiệt ⇒ tăng hiệu suất thì giảm nhiệt độ
Trắc nghiệm Amoniac và muối amoni có đáp án
Câu 1: Tính bazơ của NH3 do
A. trên N còn cặp e tự do.
B. phân tử có 3 liên kết cộng hóa trị phân cực.
C. NH3 tan được nhiều trong nước.
D. NH3 tác dụng với nước tạo NH4OH.
Đáp án: A
Câu 2: Để tách riêng NH3 ra khỏi hỗn hợp gồm N2 , H2, NH3 trong công nghiệp người ta đã
A. Cho hỗn hợp qua nước vôi trong dư.
B. Cho hỗn hợp qua bột CuO nung nóng.
C. nén và làm lạnh hỗn hợp để hòa lỏng NH3.
D. Cho hỗn hợp qua dung dịch H2SO4 đặc.
Đáp án: C
Câu 3: Chất nào sau đây có thể làm khô khí NH3 có lẫn hơi nước ?
A. P2O5. B. H2SO4 đặc. C. CuO bột. D. NaOH rắn.
Đáp án: D
Câu 4: Trong các phản ứng sau, phản ứng nào NH3 đóng vai trồ là chất oxi hóa ?
A. 2NH3 + H2O2 +MnSO4 → MnO2 + (NH4)2SO4
B. 2NH3 + 3Cl2 → N2 + 6HCl
C. 4NH3 + 5O2 → 4NO + 6H2O
D. 2HN3 + 2 Na → 2NaNH2 + H2
Đáp án: D
Câu 5: Muối được làm bột nở trong thực phẩm là
A. (NH4)2CO3. B. Na2CO3. C. NH4HSO3. D. NH4Cl.
Đáp án: C
Câu 6: Dãy các chất đều phản ứng với NH3 trong điều kiện thích hợp là :
A. HCl, O2, Cl2, FeCl5. B. H2SO4, Ba(OH)2, FeO, NaOH
C. HCl, HNO3, AlCl3, CaO D. KOH, HNO3, CuO, CuCl2
Đáp án: A
Câu 7: X là muối khi tác dụng với dung dịch NaOH dư sinh khí mùi khai, tác dụng với dung dịch BaCl2 sinh kết tủa trắng không tan trong HNO3. X là muối nào trong số các muối sau?
A. (NH4)2CO3. B. (NH4)2SO3. C. NH4HSO3. D. (NH4)3PO4.
Đáp án: C
Câu 8: Nhận xét nào sau đây không đúng về muối amoni ?
A. Muối amoni bền với nhiệt.
B. Các muối amoni đều là chất điện li mạnh.
C. Tất cả các muối amoni đều tan trong nước.
D. các muối amoni đều bị thủy phân trong nước.
Đáp án: A
Câu 9: Oxi hóa 6 lít NH3 (tạo ra N2 và NO theo tỉ lệ mol 1 : 4) cần vừa đủ V là không khí ( chứa 20% oxi về thể tích). Các thể tích đó ở cùng điều kiện. Giá trị của V là
A. 6,5. B. 22,5. C. 32,5. D. 24,5.
Đáp án: C
12NH3 + 13O2 → 8NO + 2N2 + 18H2O
VO2 = (6 x 13) / 12 = 6,5 mol
⇒ Vkk = 6,5 : 20% = 32,5 lít
Câu 10: Cho 22,4 lít hỗn hợp khi X gồm N2 và H2 đi qua xúc tác Fe, nung nống để tổng hợp NH3 thu được 20,16 lít hỗn hợp khí Y. Hấp thụ toàn bộ Y vào dung dịch AlCl3 dư, thu được m gam kết tủa. Các thể tích khí đó ở cùng điều kiện. Giá trị của m là
A. 13. B. 2,6. C. 5,2. D. 3,9.
Đáp án: B
nX = 1 mol; nNH3 = nX - nY = 1- 0,9 = 0,1 mol
⇒ nAl(OH)3 = 0,1 /3 ⇒ m =2,6g
Xem thêm Bài tập & Câu hỏi trắc nghiệm Hóa học 11 có đáp án khác:
- Chương 1: Sự điện li
- Chương 3: Cacbon - Silic
- Chương 4: Đại cương về hóa học vô cơ
- Chương 5: Hidrocacbon no
- Chương 6: Hidrocacbon không no
- Chương 7: Hidrocacbon thơm. Nguồn hidrocacbon thiên nhiên. Hệ thống hóa về hidrocacbon
- Chương 8: Dẫn xuất halogen - ancol - phenol
- Chương 9: Andehit - Xeton - Axit cacboxylic
Tủ sách VIETJACK shopee lớp 10-11 cho học sinh và giáo viên (cả 3 bộ sách):
Săn shopee siêu SALE :
- Sổ lò xo Art of Nature Thiên Long màu xinh xỉu
- Biti's ra mẫu mới xinh lắm
- Tsubaki 199k/3 chai
- L'Oreal mua 1 tặng 3
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 11 Global Success
- Giải sgk Tiếng Anh 11 Smart World
- Giải sgk Tiếng Anh 11 Friends Global
- Lớp 11 - Kết nối tri thức
- Soạn văn 11 (hay nhất) - KNTT
- Soạn văn 11 (ngắn nhất) - KNTT
- Giải sgk Toán 11 - KNTT
- Giải sgk Vật Lí 11 - KNTT
- Giải sgk Hóa học 11 - KNTT
- Giải sgk Sinh học 11 - KNTT
- Giải sgk Lịch Sử 11 - KNTT
- Giải sgk Địa Lí 11 - KNTT
- Giải sgk Giáo dục KTPL 11 - KNTT
- Giải sgk Tin học 11 - KNTT
- Giải sgk Công nghệ 11 - KNTT
- Giải sgk Hoạt động trải nghiệm 11 - KNTT
- Giải sgk Giáo dục quốc phòng 11 - KNTT
- Giải sgk Âm nhạc 11 - KNTT
- Lớp 11 - Chân trời sáng tạo
- Soạn văn 11 (hay nhất) - CTST
- Soạn văn 11 (ngắn nhất) - CTST
- Giải sgk Toán 11 - CTST
- Giải sgk Vật Lí 11 - CTST
- Giải sgk Hóa học 11 - CTST
- Giải sgk Sinh học 11 - CTST
- Giải sgk Lịch Sử 11 - CTST
- Giải sgk Địa Lí 11 - CTST
- Giải sgk Giáo dục KTPL 11 - CTST
- Giải sgk Tin học 11 - CTST
- Giải sgk Công nghệ 11 - CTST
- Giải sgk Hoạt động trải nghiệm 11 - CTST
- Giải Giáo dục quốc phòng 11 - CTST
- Giải sgk Âm nhạc 11 - CTST
- Lớp 11 - Cánh diều
- Soạn văn 11 Cánh diều (hay nhất)
- Soạn văn 11 Cánh diều (ngắn nhất)
- Giải sgk Toán 11 - Cánh diều
- Giải sgk Vật Lí 11 - Cánh diều
- Giải sgk Hóa học 11 - Cánh diều
- Giải sgk Sinh học 11 - Cánh diều
- Giải sgk Lịch Sử 11 - Cánh diều
- Giải sgk Địa Lí 11 - Cánh diều
- Giải sgk Giáo dục KTPL 11 - Cánh diều
- Giải sgk Tin học 11 - Cánh diều
- Giải sgk Công nghệ 11 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 11 - Cánh diều
- Giải sgk Giáo dục quốc phòng 11 - Cánh diều
- Giải sgk Âm nhạc 11 - Cánh diều









