Lý thuyết Điều chế kim loại (hay, chi tiết nhất)
Bài viết Lý thuyết Điều chế kim loại với phương pháp giải chi tiết giúp học sinh ôn tập, biết cách làm bài tập Lý thuyết Điều chế kim loại.
Lý thuyết Điều chế kim loại (hay, chi tiết nhất)
Bài giảng: Bài 21: Điều chế kim loại - Cô Nguyễn Thị Thu (Giáo viên VietJack)
I. Nguyên tắc điều chế kim loại
Khử ion kim loại thành nguyên tử.
Mn+ + ne → M
II. Phương pháp điều chế kim loại
1. Phương pháp thuỷ luyện
Nguyên tắc: Dùng những dung dịch thích hợp như: H2SO4, NaOH, NaCN, … để hoà tan kim loại hoặc các hợp chất của kim loại và tách ra khỏi phần không tan có ở trong quặng. Sau đó khử những ion kim loại này trong dung dịch bằng những kim loại có tính khử mạnh như Fe, Zn, …
Phạm vi áp dụng: Thường sử dụng để điều chế các kim loại có tính khử yếu.
Ví dụ:
Fe + CuSO4 → FeSO4 + Cu↓
Fe + Cu2+ → Fe2+ + Cu↓
2. Phương pháp nhiệt luyện
Nguyên tắc: Khử ion kim loại trong hợp chất ở nhiệt độ cao bằng các chất khử như C, CO, H2 hoặc các kim loại hoạt động.
Phạm vi áp dụng: Sản xuất các kim loại có tính khử trung bình (Zn, FE, Sn, Pb, …) trong công nghiệp.
Ví dụ:
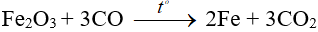
3. Phương pháp điện phân
a. Điện phân hợp chất nóng chảy
Nguyên tắc: Khử các ion kim loại bằng dòng điện bằng cách điện phân nóng chảy hợp chất của kim loại.
Phạm vi áp dụng: Điều chế các kim loại hoạt động hoá học mạnh như K, Na, Ca, Mg, Al.
Ví dụ: Điện phân MgCl2 nóng chảy để điều chế Mg.
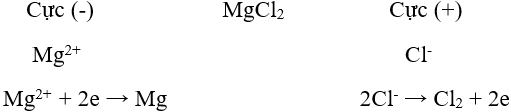
Phương trình điện phân:
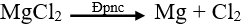
b. Điện phân dung dịch
Nguyên tắc: Điện phân dung dịch muối của kim loại.
Phạm vi áp dụng: Điều chế các kim loại có độ hoạt động hoá học trung bình hoặc yếu.
Ví dụ: Điện phân dung dịch CuCl2 để điều chế kim loại Cu.
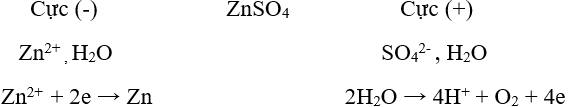
Phương trình điện phân:
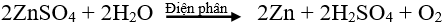
III. Định luật faraday
Tính lượng chất thu được ở các điện cực
Dựa vào công thức Farađây: 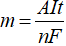
m: Khối lượng chất thu được ở điện cực (g).
A: Khối lượng mol nguyên tử của chất thu được ở điện cực.
n: Số electron mà nguyên tử hoặc ion đã cho hoặc nhận.
I: Cường độ dòng điện (ampe).
t: Thời gian điện phân (giấy).
F: Hằng số Farađây (F = 96.500).
Xem thêm các phần Lý thuyết Hóa học lớp 12 ôn thi THPT Quốc gia hay khác:
- Lý thuyết Kim loại
- Lý thuyết Hợp kim
- Lý thuyết Dãy điện hóa của kim loại
- Lý thuyết Sự điện phân, sự ăn mòn
- Dạng 1: Tính chất chung của kim loại
Sách VietJack thi THPT quốc gia 2024 cho học sinh 2k6:
Săn shopee siêu SALE :
- Sổ lò xo Art of Nature Thiên Long màu xinh xỉu
- Biti's ra mẫu mới xinh lắm
- Tsubaki 199k/3 chai
- L'Oreal mua 1 tặng 3
- Soạn Văn 12
- Soạn Văn 12 (bản ngắn nhất)
- Văn mẫu lớp 12
- Giải bài tập Toán 12
- Giải BT Toán 12 nâng cao (250 bài)
- Bài tập trắc nghiệm Giải tích 12 (100 đề)
- Bài tập trắc nghiệm Hình học 12 (100 đề)
- Giải bài tập Vật lý 12
- Giải BT Vật Lí 12 nâng cao (360 bài)
- Chuyên đề: Lý thuyết - Bài tập Vật Lý 12 (có đáp án)
- Bài tập trắc nghiệm Vật Lí 12 (70 đề)
- Luyện thi đại học trắc nghiệm môn Lí (18 đề)
- Giải bài tập Hóa học 12
- Giải bài tập Hóa học 12 nâng cao
- Bài tập trắc nghiệm Hóa 12 (80 đề)
- Luyện thi đại học trắc nghiệm môn Hóa (18 đề)
- Giải bài tập Sinh học 12
- Giải bài tập Sinh 12 (ngắn nhất)
- Chuyên đề Sinh học 12
- Đề kiểm tra Sinh 12 (có đáp án)(hay nhất)
- Ôn thi đại học môn Sinh (theo chuyên đề)
- Luyện thi đại học trắc nghiệm môn Sinh (18 đề)
- Giải bài tập Địa Lí 12
- Giải bài tập Địa Lí 12 (ngắn nhất)
- Giải Tập bản đồ và bài tập thực hành Địa Lí 12
- Bài tập trắc nghiệm Địa Lí 12 (70 đề)
- Luyện thi đại học trắc nghiệm môn Địa (20 đề)
- Giải bài tập Tiếng anh 12
- Giải bài tập Tiếng anh 12 thí điểm
- Giải bài tập Lịch sử 12
- Giải tập bản đồ Lịch sử 12
- Bài tập trắc nghiệm Lịch Sử 12
- Luyện thi đại học trắc nghiệm môn Sử (20 đề)
- Giải bài tập Tin học 12
- Giải bài tập GDCD 12
- Giải bài tập GDCD 12 (ngắn nhất)
- Bài tập trắc nghiệm GDCD 12 (37 đề)
- Luyện thi đại học trắc nghiệm môn GDCD (20 đề)
- Giải bài tập Công nghệ 12









