Hóa 12 Bài 30: Thực hành: Tính chất của natri, magie, nhôm và hợp chất của chúng
Hóa học 12 Bài 30: Thực hành: Tính chất của natri, magie, nhôm và hợp chất của chúng
Video Giải bài tập Hóa 12 Bài 30: Thực hành: Tính chất của natri, magie, nhôm và hợp chất của chúng - Cô Phạm Thị Thu Phượng
Bài 1 (trang 135 SGK Hóa 12): Viết bản tường trình
Thí nghiệm 1: So sánh khả năng phản úng của Na, Mg, Al với nước.
- Tiến hành TN: Lấy 3 ống nghiệm
+ Rót nước vào ống nghiệm 1, thêm vài giọt phenolphtalein. Đặt lên giá và cho vào ống nghiệm 1 mẩu Na nhỏ
+ Rót vào ống nghiệm 2 khoảng 5ml H2O, thêm vài giọt phenolphtalein. Đặt lên giá và cho vào ống nghiệm 1 mẩu Mg nhỏ
+ Rót vào ống nghiệm 3 khoảng 5ml H2O, thêm vài giọt phenolphtalein. Đặt lên giá và cho vào ống nghiệm 1 mẩu Al đã cạo sạch lớp oxit.
Quan sát hiện tượng
- Hiện tượng: Khi chưa đun:
+ Ống 1: Khí thoát ra mạnh, dung dịch thu được có màu hồng.
+ Ống 2 và ống 3 không có hiện tượng.
Giải thích: Ống 1 xảy ra phản ứng.
Na + H2O → NaOH + 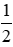
Khí thoát ra là H2 dung dịch thu được là dung dịch kiềm nên phenolphtalein chuyển màu hồng.
- Ống 2 + 3: Không có hiện tượng do Mg và Al không phản ứng với H2O
Khi đun sôi:
+ Ống 1: Khí thoát ra mạnh, dung dịch thu được có màu hồng.
+ Ống 2: Dung dịch thu được có màu hồng nhạt.
+ Ống 3: Không có hiện tượng.
Giải thích: Ống 2: Mg tác dụng với nước ở nhiệt độ cao tạo ra dung dịch bazơ yếu nên dung dịch có màu hồng nhạt.
Ống 3: Lớp bảo vệ Al(OH)3 ngăn không cho Al tác dụng với nước ở mọi điều kiện
Kết luận: Khả năng phản ứng với nước Na > Mg > Al.
Thí nghiệm 2: Nhôm tác dụng với dung dịch kiềm.
- Tiến hành TN:
+ Rót vào ống nghiệm 2-3 ml dd NaOH loãng, thêm vào đó 1 mẩu nhôm.
+ Đun nóng nhẹ ống nghiệm và quan sát hiện tượng.
- Hiện tượng: Có bọt khí thoát ra.
- Giải thích:
Khi cho Al vào dung dịch NaOH thì lớp Al2O3 trên bề mặt Al bị bào mòn.
Al2O3 + 2NaOH → 2NaAlO2 + H2O.
Al mất lớp bảo vệ Al2O3 tác dụng với nước:
2Al + 6H2O → 2Al(OH)3 + 3H2.
Al(OH)3 sinh ra lại tan trong dung dịch kiềm
Al(OH)3 + NaOH → NaAlO2 + 2H2O.
2 phản ứng xảy ra xen kẽ nhau đến khi Al tan hoàn toàn.
Thí nghiệm 3: Tính chất lưỡng tính của Al(OH)3.
- Tiến hành TN:
+ Rót vào 2 ống nghiệm, mỗi khoảng 3ml dd AlCl3, sau đó nhỏ dd NH3 dư vào 2 ống nghiệm
+ Tiếp tục nhỏ dd H2SO4 vào ống 1, lắc nhẹ. Nhỏ dd NaOH vào ống 2, lắc nhẹ
Quan sát hiện tượng
- Hiện tượng: Nhỏ NH3 vào cả 2 ống đều xuất hiện kết tủa trắng
Sau khi thêm H2SO4 và NaOH vào 2 ống thấy kết tủa trong cả 2 ống đều tan.
- Giải thích
Kết tủa trắng là Al(OH)3 tạo thành sau phản ứng:
AlCl3 + 3H2O + 3NH3 → Al(OH)3 + 3NH4Cl.
Kết tủa tan là do Al(OH)3 phản ứng với axit và kiềm tạo ra muối tan:
Al(OH)3 + NaOH → NaAlO2 + 2H2O.
2Al(OH)3 + 3H2SO4 → Al2(SO4)3 + 6H2O
Kết luận : Al(OH)3 là hiđroxit lưỡng tính.
Các bài Giải bài tập Hóa 12, Để học tốt Hóa học 12 Chương 6 khác:
- Bài 31: Sắt
- Bài 32: Hợp chất của sắt
- Bài 33: Hợp kim của sắt
- Bài 34: Crom và hợp chất của crom
- Bài 35: Đồng và hợp chất của đồng
Sách VietJack thi THPT quốc gia 2024 cho học sinh 2k6:
Săn shopee siêu SALE :
- Sổ lò xo Art of Nature Thiên Long màu xinh xỉu
- Biti's ra mẫu mới xinh lắm
- Tsubaki 199k/3 chai
- L'Oreal mua 1 tặng 3
- Soạn Văn 12
- Soạn Văn 12 (bản ngắn nhất)
- Văn mẫu lớp 12
- Giải bài tập Toán 12
- Giải BT Toán 12 nâng cao (250 bài)
- Bài tập trắc nghiệm Giải tích 12 (100 đề)
- Bài tập trắc nghiệm Hình học 12 (100 đề)
- Giải bài tập Vật lý 12
- Giải BT Vật Lí 12 nâng cao (360 bài)
- Chuyên đề: Lý thuyết - Bài tập Vật Lý 12 (có đáp án)
- Bài tập trắc nghiệm Vật Lí 12 (70 đề)
- Luyện thi đại học trắc nghiệm môn Lí (18 đề)
- Giải bài tập Hóa học 12
- Giải bài tập Hóa học 12 nâng cao
- Bài tập trắc nghiệm Hóa 12 (80 đề)
- Luyện thi đại học trắc nghiệm môn Hóa (18 đề)
- Giải bài tập Sinh học 12
- Giải bài tập Sinh 12 (ngắn nhất)
- Chuyên đề Sinh học 12
- Đề kiểm tra Sinh 12 (có đáp án)(hay nhất)
- Ôn thi đại học môn Sinh (theo chuyên đề)
- Luyện thi đại học trắc nghiệm môn Sinh (18 đề)
- Giải bài tập Địa Lí 12
- Giải bài tập Địa Lí 12 (ngắn nhất)
- Giải Tập bản đồ và bài tập thực hành Địa Lí 12
- Bài tập trắc nghiệm Địa Lí 12 (70 đề)
- Luyện thi đại học trắc nghiệm môn Địa (20 đề)
- Giải bài tập Tiếng anh 12
- Giải bài tập Tiếng anh 12 thí điểm
- Giải bài tập Lịch sử 12
- Giải tập bản đồ Lịch sử 12
- Bài tập trắc nghiệm Lịch Sử 12
- Luyện thi đại học trắc nghiệm môn Sử (20 đề)
- Giải bài tập Tin học 12
- Giải bài tập GDCD 12
- Giải bài tập GDCD 12 (ngắn nhất)
- Bài tập trắc nghiệm GDCD 12 (37 đề)
- Luyện thi đại học trắc nghiệm môn GDCD (20 đề)
- Giải bài tập Công nghệ 12









