Giải thích vì sao bán kính nguyên tử Na, Mg lớn hơn bán kính
Giải Hóa học 10 Bài 10: Liên kết ion
Bài 3 trang 56 Hóa học 10:
a) Giải thích vì sao bán kính nguyên tử Na, Mg lớn hơn bán kính của các ion kim loại tương ứng.
b) Vì sao cả Na2O và MgO đều là chất rắn ở điều kiện thường?
c) Vì sao nhiệt độ nóng chảy của MgO (2 852oC) cao hơn rất nhiều so với Na2O (1 132oC)?
Lời giải:
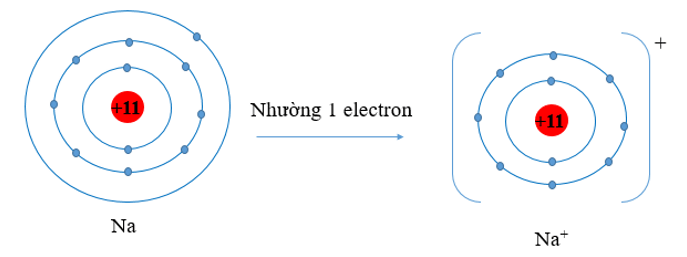
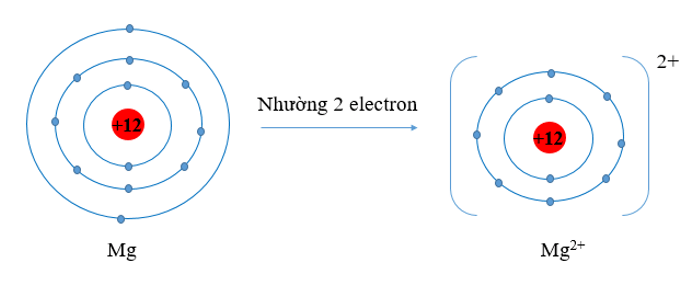
a) Nguyên tử kim loại có 1, 2, 3 electron lớp ngoài cùng, có xu hướng nhường 1, 2, 3 electron này để đạt cấu hình bền vững giống như khí hiếm. Khi nhường electron các ion kim loại mất đi 1 lớp electron ngoài cùng. Do đó bán kính ion kim loại nhỏ hơn bán kính nguyên tử kim loại tương ứng.
- Nguyên tử Na có 3 lớp electron, 1 electron lớp ngoài cùng. Nguyên tử Na đã nhường đi 1 electron ở lớp thứ 3 để trở thành ion Na+. Khi đó ion Na+ chỉ còn 2 lớp electron
⇒ Bán kính Na+ nhỏ hơn bán kính nguyên tử Na.
- Nguyên tử Mg có 3 lớp electron, 2 electron lớp ngoài cùng. Nguyên tử Mg đã nhường đi 2 electron ở lớp thứ 3 để trở thành ion Mg2+. Khi đó ion Mg2+ chỉ còn 2 lớp electron
⇒ Bán kính Mg2+ nhỏ hơn bán kính nguyên tử Mg2+.
b) Mỗi nguyên tử Na đã nhường 1 electron, nguyên tử O nhận 2 electron từ nguyên tử Na để hình thành hợp chất ion Na2O.
2Na+ + O2- → Na2O
Vì Na2O là hợp chất ion ⇒ Ở điều kiện thường Na2O tồn tại ở thể rắn.
Nguyên tử Mg nhường 2 electron, nguyên tử O nhận 2 electron từ nguyên tử Mg để hình thành hợp chất ion MgO.
Mg2+ + O2- → MgO
Vì MgO là hợp chất ion ⇒ Ở điều kiện thường MgO tồn tại ở thể rắn.
c) Ta có:
+ Bán kính ion Na+ > bán kính ion Mg2+
+ Điện tích ion Mg2+ > điện tích ion Na+
Vậy nhiệt độ nóng chảy của MgO (2852oC) cao hơn rất nhiều so với Na2O (1132oC) do năng lượng phân li tỉ lệ thuận với điện tích ion và tỉ lệ nghịch với bán kính ion.
Xem thêm lời giải bài tập Hóa học lớp 10 Cánh diều hay, chi tiết khác:
Mở đầu trang 53 Hóa học 10: Phát biểu nào dưới đây phù hợp với sơ đồ phản ứng ở Hình 10.1? ....
Câu hỏi 1 trang 53 Hóa học 10: Phát biểu nào sau đây là đúng? ....
Luyện tập 1 trang 54 Hóa học 10: Hãy nêu một số hợp chất ion ....
Câu hỏi 2 trang 54 Hóa học 10: Viết hai giai đoạn của sự hình thành CaO ....
Luyện tập 2 trang 54 Hóa học 10: Cho các ion: Li+, Ca2+, Al3+, F-, O2-, PO43- ....
Luyện tập 3 trang 54 Hóa học 10: Cho các chất sau: SiO2 là thành phần chính của thạch anh ....
Thực hành 1 trang 55 Hóa học 10: Lắp ráp mô hình tinh thể NaCl ....
Thực hành 2 trang 55 Hóa học 10: Từ mô hình NaCl, hãy cho biết xung quanh mỗi ion Na+ ....
Vận dụng 1 trang 55 Hóa học 10: Hãy kể tên một số hợp chất ion có xung quanh em ....
Bài 1 trang 56 Hóa học 10: Những phát biểu nào sau đây là đúng? ....
Bài 2 trang 56 Hóa học 10: Những tính chất nào sau đây là tính chất điển hình của hợp chất ion? ....
Xem thêm các tài liệu học tốt lớp 10 hay khác:
- Giải sgk Hóa học 10 Cánh diều
- Giải Chuyên đề Hóa học 10 Cánh diều
- Giải SBT Hóa học 10 Cánh diều
- Giải lớp 10 Cánh diều (các môn học)
- Giải lớp 10 Kết nối tri thức (các môn học)
- Giải lớp 10 Chân trời sáng tạo (các môn học)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Soạn văn 10 (hay nhất) - Cánh diều
- Soạn văn 10 (ngắn nhất) - Cánh diều
- Soạn văn 10 (siêu ngắn) - Cánh diều
- Giải sgk Toán 10 - Cánh diều
- Giải Tiếng Anh 10 Global Success
- Giải Tiếng Anh 10 Friends Global
- Giải sgk Tiếng Anh 10 iLearn Smart World
- Giải sgk Tiếng Anh 10 Explore New Worlds
- Giải sgk Vật lí 10 - Cánh diều
- Giải sgk Hóa học 10 - Cánh diều
- Giải sgk Sinh học 10 - Cánh diều
- Giải sgk Địa lí 10 - Cánh diều
- Giải sgk Lịch sử 10 - Cánh diều
- Giải sgk Kinh tế và Pháp luật 10 - Cánh diều
- Giải sgk Tin học 10 - Cánh diều
- Giải sgk Công nghệ 10 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 10 - Cánh diều
- Giải sgk Giáo dục quốc phòng 10 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

