Cấu hình electron của Cu, copper (đồng) chương trình mới
Bài viết hướng dẫn cách viết Cấu hình electron của Cu, copper (đồng) theo chương trình sách mới của ba bộ sách Kết nối tri thức, Cánh diều, Chân trời sáng tạo giúp học sinh dễ dàng nắm vững cách viết Cấu hình electron của Cu, copper (đồng).
Cấu hình electron của Cu, copper (đồng) chương trình mới
Copper có tên thông thường là đồng, kí hiệu hóa học là Cu, số hiệu nguyên tử bằng 29. Dựa vào cấu hình electron của copper ta sẽ biết được vị trí trong bảng tuần hoàn và tính chất hóa học của copper. Bài viết dưới đây sẽ giúp các em làm rõ vấn đề này.
1. Cấu hình electron nguyên tử copper (Z = 29)
- Cu có số hiệu nguyên tử là 29 ⇒ nguyên tử Cu có 29 electron.
- Do có sự chèn mức năng lượng, theo trật tự phân mức năng lượng các electron được phân bố như sau:
1s22s22p63s23p64s23d9.
- Do trạng thái này không bền nên 1 electron ở phân lớp 4s chuyển sang phân lớp 3d để đạt trạng thái bão hòa bền vững hơn.
- Sau đó, sắp xếp các phân lớp theo từng lớp để thu được cấu hình electron của Cu là:
1s22s22p63s23p63d104s1.
Viết gọn: [Ar]3d104s1.
2. Cấu hình electron của nguyên tử copper (Z = 29) theo ô orbital
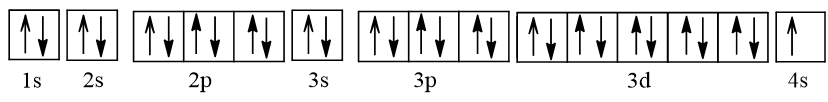
- Cấu hình electron của nguyên tử copper (Z = 29) theo ô orbital là:
- Nguyên tử Cu có 1 electron độc thân, thuộc AO 4s.
3. Mối quan hệ giữa cấu hình electron với vị trí trong bảng tuần hoàn và tính chất nguyên tố
- Vị trí Cu trong bảng tuần hoàn:
Từ cấu hình electron của Cu là 1s22s22p63s23p63d104s1 ta xác định được:
+ Cu thuộc ô số 29 (do Z = 29)
+ Chu kì 4 (do có 4 lớp electron)
+ Nhóm IB (do có tổng số electron thuộc hai phân lớp 3d và 4s là 11).
+ Là nguyên tố d (do Cu là nguyên tố nhóm B, nguyên tử có cấu hình electron phân lớp ngoài cùng và phân lớp sát ngoài cùng là 3d104s1).
Lưu ý: Với nguyên tố nhóm B, số thứ tự của nhóm bằng tổng số electron thuộc hai phân lớp (n - 1)d và ns. Nếu tổng số electron của hai phân lớp (n - 1)d và ns là 8, 9, 10 thì nguyên tố đó thuộc nhóm VIIIB; là 11 thì thuộc nhóm IB; là 12 thì thuộc nhóm IIB.
- Tính chất nguyên tố:
+ Cu thuộc chu kì 4, nhóm IB nên đồng là kim loại chuyển tiếp dãy thứ nhất.
+ Số oxi hóa phổ biến của đồng trong hợp chất là +2, ngoài ra còn số oxi hóa +1.
4. Ví dụ
Câu 1: Nguyên tử của nguyên tố X có cấu hình electron ở phân lớp ngoài cùng và sát ngoài cùng là 3d104s1. Cấu hình electron của nguyên tử X là
A. [Ar] 3d94s1.
B. [Ar] 3d9 4s2.
C. [Ar] 3d10 4s1.
D. [Ar] 3d10 4s2.
Lời giải:
Đáp án đúng là: C
Cấu hình electron của X là 1s22s22p63s23p63d104s1.
Viết gọn: [Ar]3d104s1.
Câu 2: Nguyên tử của nguyên tố X có cấu hình electron lớp ngoài cùng là 4s1. Số electron phân lớp d nhiều hơn số electron phân lớp s là 3 electron. Vị trí của X trong bảng tuần hoàn hóa học?
A. Chu kì 4, nhóm IA.
B. Chu kì 4, nhóm IB.
C. Chu kì 4, nhóm VIIB.
D. Chu kì 4, nhóm VIIIB.
Lời giải:
Đáp án đúng là: B
Nguyên tử của nguyên tố X có cấu hình electron lớp ngoài cùng là 4s1.
Nguyên tố X thuộc chu kì 4 và có tổng số electron phân lớp s là 7.
Số electron phân lớp d nhiều hơn số electron phân lớp s là 3 electron.
⇒ Số electron phân lớp d là 10.
Tổng số electron trên phân lớp 3d và 4s là 11 ⇒ Nguyên tố X thuộc nhóm IB.
Xem thêm cách viết cấu hình electron của các ion hay, chi tiết khác:
Sách VietJack thi THPT quốc gia 2025 cho học sinh 2k7:
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)








 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp



