CuO + C2H5OH → Cu + CH3CHO + H2O | CuO ra Cu | C2H5OH ra CH3CHO
Phản ứng CuO + C2H5OH hay CuO ra Cu hoặc C2H5OH ra CH3CHO thuộc loại phản ứng oxi hóa khử đã được cân bằng chính xác và chi tiết nhất. Bên cạnh đó là một số bài tập có liên quan về CuO có lời giải, mời các bạn đón xem:
CuO + C2H5OH → Cu + CH3CHO + H2O
1. Phương trình hoá học của phản ứng ethanol tác dụng với CuO
CH3CH2OH + CuO CH3CHO + Cu + H2O
Cách lập phương trình hoá học:
Bước 1: Xác định các nguyên tử có sự thay đổi số oxi hoá, từ đó xác định chất oxi hoá – chất khử:
Chất khử: CH3CH2OH; chất oxi hoá: CuO.
Bước 2: Biểu diễn quá trình oxi hoá, quá trình khử
- Quá trình oxi hoá:
- Quá trình khử:
Bước 3: Tìm hệ số thích hợp cho chất khử và chất oxi hoá
Bước 4: Điền hệ số của các chất có mặt trong phương trình hoá học. Kiểm tra sự cân bằng số nguyên tử của các nguyên tố ở hai vế.
CH3CH2OH + CuO CH3CHO + Cu + H2O
2. Điều kiện để ethanol tác dụng với CuO
Phản ứng giữa ethanol và CuO diễn ra ở điều kiện đun nóng.
3. Cách tiến hành thí nghiệm
Cho hơi C2H5OH đi qua ống sứ đựng CuO dư đun nóng.
4. Hiện tượng phản ứng
CuO từ màu đen chuyển sang màu đỏ là Cu
5. Mở rộng tính chất hóa học của ancol
5.1. Phản ứng thế H của nhóm OH ancol (phản ứng đặc trưng của ancol)
- Tính chất chung của ancol tác dụng với kim loại kiềm:
Ví dụ:
2CH3CH2OH + 2Na → 2CH3CH2ONa + H2
Tổng quát:
+ Với ancol đơn chức:
2ROH + 2Na → 2RONa + H2↑
+ Với ancol đa chức:
2R(OH)x + 2xNa → 2R(ONa)x + xH2↑
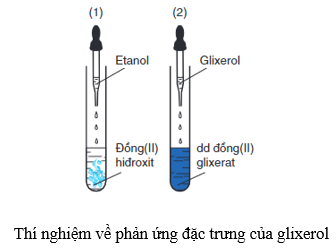
- Tính chất đặc trưng của glycerol hòa tan Cu(OH)2
Ví dụ:
2C3H5(OH)3 + Cu(OH)2 → [C3H5(OH)2O]2Cu + 2H2O
Không chỉ glycerol, các ancol đa chức có các nhóm – OH liền kề cũng có tính chất này.
⇒ Phản ứng này dùng để phân biệt ancol đơn chức với ancol đa chức có các nhóm - OH cạnh nhau trong phân tử.
5.2. Phản ứng thế nhóm OH
a) Phản ứng với axit vô cơ:
Ví dụ:
C2H5OH + HBr C2H5Br + H2O
Các ancol khác cũng có phản ứng tương tự, phản ứng này chứng tỏ phân tử ancol có nhóm – OH.
b) Phản ứng với ancol
Ví dụ:
2C2H5OH C2H5OC2H5 + H2O
C2H5OC2H5: điEthyl ete
⇒ Công thức tính số ete tạo thành từ n ancol khác nhau là
5.3. Phản ứng tách nước (phản ứng đehidrat hoá)
Ví dụ:
CH3CH2OH CH2 = CH2 + H2O
Trong điều kiện tương tự, các ancol no, đơn chức, mạch hở (trừ CH3OH) có thể bị tách nước tạo thành alkene. Tổng quát:
CnH2n + 1OH CnH2n + H2O
5.4. Phản ứng oxi hoá
- Phản ứng oxi hoá hoàn toàn:
Khi bị đốt các ancol cháy, tỏa nhiều nhiệt. Tổng quát cho đốt cháy ancol no, đơn chức, mạch hở:
CnH2n + 2O + O2 nCO2 + (n + 1)H2O
- Phản ứng oxi hoá không hoàn toàn bởi CuO, to
+ Các ancol bậc I bị oxi hóa không hoàn toàn tạo thành anđehit. Ví dụ:
CH3CH2OH + CuO CH3CHO (anđehit axetic) + Cu + H2O
+ Các ancol bậc II bị oxi hóa không hoàn toàn tạo thành ketone. Ví dụ:
CH3- CH(OH) – CH3 + CuO CH3 – CO – CH3 + Cu + H2O
+ Trong điều kiện trên, ancol bậc III không phản ứng.
6. Bài tập liên quan
Câu 1: Công thức nào đúng với tên gọi tương ứng?
A. ancol sec-butylic: (CH3)2CH-CH2OH
B. ancol iso-amylic: (CH3)2CHCH2CH2CH2OH
C. ethyl alcohol: CH3OH
D. allyl alcohol: CH2=CHCH2OH
Hướng dẫn giải:
Đáp án D
Ancol sec-butylic: CH3-CH(OH)-CH2-CH3
Ancol isoamylic: (CH3)2CHCH2CH2OH
ethyl alcohol: CH3CH2OH
Câu 2: Rượu pha chế dùng cồn công nghiệp có chứa hàm lượng methanol cao, có thể gây ngộ độc nguy hiểm đến tính mạng. Công thức phân tử của methanol là
A. C2H5OH B. C3H5OH
C. CH3OH D. C3H7OH
Hướng dẫn giải:
Đáp án C
Methanol: CH3OH.
Câu 3:Phản ứng nào sau đây không xảy ra:
A. C2H5OH + CH3COOH B. C2H5OH + HBr
C. C2H5OH + O2 D. C2H5OH + NaOH
Hướng dẫn giải:
Đáp án D
Ancol hầu như không phản ứng được với NaOH.
Câu 4:Độ rượu là
A. Số ml rượu nguyên chất có trong 100 ml dung dịch rượu.
B. Số ml rượu nguyên chất có trong 100 gam dung dịch rượu.
C. Khối lượng rượu nguyên chất có trong 100 gam dung dịch rượu.
D. Khối lượng rượu nguyên chất có trong 100 ml dung dịch rượu.
Hướng dẫn giải:
Đáp án A
Độ rượu là số ml rượu nguyên chất có trong 100 ml hỗn hợp rượu với nước (dung dịch rượu).
Câu 5:Điều kiện của phản ứng tách nước : CH3-CH2-OH → CH2 = CH2 + H2O là :
A. H2SO4 đặc, 120oC B. H2SO4 loãng, 140oC
C. H2SO4 đặc, 170oC D. H2SO4 đặc, 140oC
Hướng dẫn giải:
Đáp án C
CH3-CH2-OH CH2 = CH2 + H2O
Câu 6:Cho Na tác dụng vừa đủ với 1,24 gam hỗn hợp 3 ancol đơn chức X, Y, Z thấy thoát ra 0,336 lít khí H2 (đkc). Khối lượng muối natri ancolat thu được là :
A. 2,4 gam.
B. 1,9 gam.
C. 2,85 gam.
D. 3,8 gam
Hướng dẫn giải:
Đáp án B
Số mol khí H2 =
Đặt công thức phân tử trung bình của ba ancol là
Phương trình phản ứng :
Theo giả thiết, phương trình phản ứng (1), kết hợp với định luật bảo toàn khối lượng ta có:
1,24 + 0,03.23 – 0,015.2 = 1,9 gam.
Câu 7:Cho 0,1 lít cồn etylic 95o tác dụng với Na dư thu được V lít khí H2 (đktc). Biết rằng ethyl alcohol nguyên chất có khối lượng riêng là 0,8 g/ml, khối lượng riêng của nước là 1 g/ml. Giá trị của V là
A. 43,23 lít.
B. 37 lít.
C. 18,5 lít.
D. 21,615 lít
Hướng dẫn giải:
Đáp án D
Trong 0,1 lít cồn etylic 95o có:
Số ml C2H5OH nguyên chất = 0,1.1000.0,95 = 95 ml; khối lượng C2H5OH nguyên chất = 95.0,8 = 76 gam; số mol C2H5OH = mol.
Số ml nước = 5 ml; khối lượng nước = 5.1 = 5 gam; số mol nước = mol.
Phương trình phản ứng của Na với dung dịch ancol :
2H2O + 2Na → 2NaOH + H2 (1)
2C2H5OH + 2Na → 2C2H5ONa + H2 (2)
Theo phương trình (1), (2) và giả thiết ta có :
→= 0,965.22,4 = 21,616 lít
Câu 8:13,8 gam ancol A tác dụng với Na dư giải phóng 5,04 lít H2 ở đktc, biết MA < 100. Vậy A có công thức cấu tạo thu gọn là
A. CH3OH.
B. C2H5OH.
C. C3H6(OH)2.
D. C3H5(OH)3
Hướng dẫn giải:
Đáp án D
Ta có:
Đặt công thức của ancol là R(OH)a.
Phương trình phản ứng :
Vậy A có công thức cấu tạo thu gọn là C3H5(OH)3.
Câu 9: Cho 15,6 gam hỗn hợp hai ancol (rượu) đơn chức, kế tiếp nhau trong dãy đồng đẳng tác dụng hết với 9,2 gam Na, thu được 24,5 gam chất rắn. Hai ancol đó là
A. C3H5OH và C4H7OH.
B. C2H5OH và C3H7OH
C. C3H7OH và C4H9OH.
D. CH3OH và C2H5OH
Hướng dẫn giải:
Đáp án B
Đặt công thức trung bình của hai ancol là
Phản ứng hóa học:
+ Na → +
Áp dụng định luật bảo toàn khối lượng cho phản ứng, ta có:
=> gam, mol
=>
→
Ta thấy 29 < < 43 =>Hai ancol là : C2H5OH và C3H7OH
Câu 10:Có hai thí nghiệm sau :
Thí nghiệm 1: Cho 6 gam ancol, mạch hở, đơn chức A tác dụng với m gam Na, thu được 0,075 gam H2
Thí nghiệm 2: Cho 6 gam ancol, mạch hở, đơn chức A tác dụng với 2m gam Na, thu được không tới 0,1 gam H2.
A có công thức là
A. CH3OH.
B. C2H5OH.
C. C3H7OH.
D. C4H7OH
Hướng dẫn giải:
Đáp án D
Cùng lượng ancol phản ứng nhưng ở thí nghiệm 2 thu được nhiều khí H2 hơn, chứng tỏ ở thí nghiệm 1 ancol còn dư, Na phản ứng hết.
Ở thí nghiệm 2 lượng Na dùng gấp đôi ở thí nghiệm 1 nhưng lượng H2 thu được ở thí nghiệm 2 nhỏ hơn 2 lần lượng H2 ở thí nghiệm 1, chứng tỏ ở thí nghiệm 2 Na dư, ancol phản ứng hết.
Đặt công thức phân tử của ancol là ROH, phương trình phản ứng :
2ROH + 2Na → 2RONa + H2 (1)
Thí nghiệm 1: 0,075 0,0375 : mol
Thí nghiệm 2: 2x < 0,1 x < 0,05 : mol
Ở thí nghiệm 1 ancol dư nên:
Ở thí nghiệm 2 số mol H2 thu được không đến 0,05 nên:
→ 60 < Mancol < 80
→ Công thức phân tử của ancol là C4H7OH (M = 72 gam/mol).
Xem thêm các phương trình hóa học hay khác:
- CuO + 2HCl → CuCl2 + H2O
- CuO + H2SO4 → CuSO4 + H2O
- CuO + 2HNO3 → Cu(NO3)2 + H2O
- CuO + CO → Cu + CO2
- CuO + H2 → Cu + H2O
- 3CuO + 2Al → 3Cu + Al2O3
- CuO + C → Cu + CO2
- 3CuO + 2NH3 → 3Cu + N2 + 3H2O
- CuO + CH3OH → Cu + HCHO + H2O
Sách VietJack thi THPT quốc gia 2025 cho học sinh 2k7:
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)








 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp



