300 bài tập trắc nghiệm Hóa học 10 Chương 6 có đáp án Kết nối tri thức, Chân trời sáng tạo, Cánh diều
Với 300 bài tập trắc nghiệm Hóa học 10 Chương 6 có đáp án sách mới Kết nối tri thức, Chân trời sáng tạo, Cánh diều đầy đủ các mức độ nhận biết, thông hiểu, vận dụng sẽ giúp học sinh ôn tập trắc nghiệm Hóa 10 Chương 6. Bạn vào tên bài học hoặc Xem chi tiết để theo dõi bài viết.
Trắc nghiệm Hóa học 10 Chương 6 có đáp án Kết nối tri thức, Chân trời sáng tạo, Cánh diều
Thi online Hóa 10 KNTTThi online Hóa 10 CDThi online Hóa 10 CTST
(Kết nối tri thức) Trắc nghiệm Hóa 10 Chương 6: Tốc độ phản ứng
(Chân trời sáng tạo) Trắc nghiệm Hóa 10 Chương 6: Tốc độ phản ứng hóa học
(Cánh diều) Trắc nghiệm Hóa 10 Chủ đề 6: Tốc độ phản ứng hóa học
Lưu trữ: Trắc nghiệm Hóa học 10 Chương 6: Oxi; Lưu huỳnh (sách cũ)
- 15 bài tập trắc nghiệm Oxi; Ozon (có đáp án)
- 15 bài tập trắc nghiệm Lưu huỳnh (có đáp án)
- Bài tập trắc nghiệm Thực hành: Tính chất của oxi, lưu huỳnh (có đáp án)
- 15 bài tập trắc nghiệm Hiđro sunfua; Lưu huỳnh đioxit; Lưu huỳnh trioxit (có đáp án)
- 15 bài tập trắc nghiệm Axit sunfuric; Muối sunfat (có đáp án)
- 15 bài tập ôn tập Oxi và lưu huỳnh (có đáp án)
- Bài tập trắc nghiệm Thực hành số: Tính chất các hợp chất của lưu huỳnh (có đáp án)
- Đề kiểm tra 1 tiết Hóa 10 Học kì 2 (có đáp án)
Trắc nghiệm Oxi, Ozon (có đáp án)
Câu 1: Nguyên tố oxi có số hiệu nguyên tử là 8. Vị trí của oxi trong bảng tuần hoàn các nguyên tố hóa học là
A. chu kì 3, nhóm VIA.
B. chu kì 2, nhóm VIA.
C. chu kì 3, nhóm IVA.
D. chu kì 2, nhóm IVA.
Đáp án: B
Câu 2: Tính chất hóa học đặc trưng của nguyên tố oxi là
A. tính oxi hóa mạnh.
B. tính khử mạnh.
C. tính oxi hóa yếu.
D. vừa có tính oxi hóa, vừa có tính khử.
Đáp án: A
Câu 3: Trong phòng thí nghiệm, người ta điều chế oxi bằng cách
A. điện phân nước.
B. nhiệt phân Cu(NO3)2
.C. nhiệt phân KClO3 có xúc tác MnO2.
D. chưng cất phân đoạn không khí lỏng.
Đáp án: C
Câu 4: Dãy gồm các chất đều tác dụng được với oxi là
A. Mg, Al, C, C2H5OH
B. Al, P, Cl2, CO
C. Au, C, S, CO
D. Fe, Pt, C, C2H5OH
Đáp án: A
Câu 5: Ở nhiệt độ thường
A. O2 không oxi hóa được Ag, O3 oxi hóa được Ag.
B. O2 oxi hóa được Ag, O3 không oxi hóa được Ag.
C. Cả O2 và O3 đều không oxi hóa được Ag.
D. Cả O2 và O3 đều oxi hóa được Ag.
Đáp án: A
Câu 6: Phương trình hóa học nào sau đây sai?
A. KMnO4 to → K + Mn + 2O2
B. 2KClO3 to → 2KCl + 3O2
C. 2Ag + O3 → Ag2O + O2
D. C2H5OH + 3O2 to → 2CO2 + 3H2O
Đáp án: A
Câu 7: Cặp chất nào sau đây không tác dụng được với nhau?
A. Ag và O3
B. CO và O2
C. Mg và O2
D. CO2 và O2
Đáp án: D
Câu 8: Ứng dụng nào sau đây không phải của ozon?
A. Khử trùng nước sinh hoạt.
B. Chữa sâu răng.
C. Tẩy trắng tinh bột, dầu ăn.
D. Điều chế oxi trong phòng thí nghiệm.
Đáp án: D
Câu 9: Trái cây được bảo quản lâu hơn trong môi trường vô trùng. Trong thực tế, người ta sử dụng nước ozon để bảo quản trái cây. Ứng dụng trên dựa vào tính chất nào sau đây?
A. Ozon trơ về mặt hóa học.
B. Ozon là chất khí có mùi đặc trưng.
C. Ozon là chất có tính oxi hóa mạnh.
D. Ozon không tác dụng được với nước.
Đáp án: C
Câu 10: Phát biểu nào sau đây sai?
A. Khí oxi không màu, không mùi, nặng hơn không khí.
B. Khí ozon màu xanh nhạt, có mùi đặc trưng.
C. Ozon là một dạng thù hình của oxi, có tính oxi hóa mạnh hơn oxi.
D. Ozon và oxi đều được dùng để khử trùng nước sinh hoạt.
Đáp án: D
Trắc nghiệm Lưu huỳnh (có đáp án)
Câu 1: Nguyên tố lưu huỳnh có số hiệu nguyên tử là 16. Vị trí của lưu huỳnh trong bảng tuần hoàn các nguyên tố hóa học là
A. chu kì 3, nhóm VIA.
B. chu kì 5, nhóm VIA.
C. chu kì 3, nhóm IVA.
D. chu kì 5, nhóm IVA.
Đáp án: A
Câu 2: Cho các phản ứng hóa học sau:
S + O2 to → SO2
S + 3F2 to → SF6
S + Hg → HgS
S + 6HNO3 (đặc) to → H2SO4 + 6NO2 + 2H2O
Trong các phản ứng trên, số phản ứng trong đó S thể hiện tính khử là
A. 3 B. 2 C. 4 D. 1
Đáp án: A
Câu 3: Hơi thủy ngân rất dộc, bởi vậy khi làm vỡ nhiệt kế thủy ngân thì chất bột được dùng để rắc lên thủy ngân rồi gom lại là
A. vôi sống.
B. cát.
C. muối ăn.
D. lưu huỳnh.
Đáp án: D
Câu 4: Nguyên tử S đóng vai trò vừa là chất khử, vừa là chất oxi hóa trong phản ứng nào sau đây?
A. 4S + 6NaOH (đặc) to → 2Na2S + Na2S2O3 +3H2O
B. S + 3F2 to → SF6
C. S + 6HNO3 (đặc) to → H2SO4 + 6NO2 + 2H2O
D. S + 2Na to → Na2S
Đáp án: A
Câu 5: Đun nóng 4,8 gam bột Mg với 9,6 gam bột lưu huỳnh (trong điều kiện không có không khí), thu được chất rắn X. Cho toàn bộ X vào lượng dư dung dịch HCl, thu được V lít khí (đktc). Giá trị của V là
A. 2,24 B. 3,36 C. 4,48 D. 6,72
Đáp án: C
Mg + S to → MgS
nMg = 4,8/24 = 0,2 (mol); nS = 9,6/32 = 0,3 (mol) ⇒ S dư; nMgS = 0,2 (mol)
MgS + 2HCl → MgCl2 + H2S ↑
⇒ V = 0,2.22,4 = 4,48 (lít)
Câu 6: Cho 11 gam hỗn hợp bột sắt và bột nhôm tác dụng với bột lưu huỳnh trong điều kiện không có không khí) thấy có 12,8 gam lưu huỳnh tham gia phản ứng. Khối lượng sắt có trong 11 gam hỗn hợp đầu là
A. 5,6 gam. B. 11,2 gam. C. 2,8 gam. D. 8,4 gam.
Đáp án: A
nS = 12,8/32 = 0,4 (mol)
⇒ mhh = mFe + mAl
Bảo toàn electron: 2nFe+ 3nAl = 2nS
⇒ 56nFe + 27 nAl = 11 ; 2nFe + 3nAl = 2.0,4)
⇒ nFe = 0,1 nAl = 0,2) ⇒ mFe = 0,1.56 = 5,6 (gam)
Câu 7: Trong 5,6 gam bột sắt với 2,4 gam bột lưu huỳnh rồi nung nóng (trong điều kiện không có không khí), thu được hỗn hợp rắn M. Cho M tác dụng với lượng dư dung dịch HCl, giải phóng hỗn hợp khí X và còn lại một phần không tan G. Để đốt cháy hoàn toàn X và G cần vừa đủ V lít khí O2 (đktc). Giá trị của V là
A. 2,80 B. 3,36 C. 3,08 D. 4,48
Đáp án: A
nFe = 5,6/56 = 0,1 (mol); nS = 2,4/32 = 0,075 (mol)
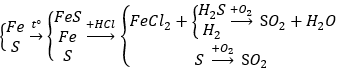
Bảo toàn electron ⇒ 4nO2 = 2nFe + 4nS = 2.0,1 + 4.0,075
⇒ nO2 = 0,125 mol
⇒ V = 0,125. 22,4 = 2,8 (lít)
Câu 8: Nung nóng hỗn hợp bột X gồm a mol Fe và b mol S trong khí trơ, hiệu suất phản ứng bằng 50%, thu được hỗn hợp rắn Y. Cho Y vào dung dịch HCl dư, sau khi các phản ứng xảy ra haonf toàn, thu được hỗn hợp khí Z có tỉ khối so với H2 bằng 5. Tỉ lệ a:b bằng
A. 2:1 B. 1:1 C. 3:1 D. 3:2
Đáp án: A
Fe + S to → FeS
FeS + 2HCl → FeCl2 + H2S; Fe + 2HCl → FeCl2 + H2
MZ = 5.2 = 10; Chọn 1 mol Z
⇒ nH2 + nH2S = 1
2nH2 + 34nH2S=10
⇒ nH2 = 0,75 ; nH2S = 0,25
nFeS = nH2S = 0,25 mol; nFe (dư) = nH2 = 0,75 mol
⇒ nFe(bđ) = 0,25 + 0,75 = 1 (mol) ⇒ nS(bđ) = 0,25.100/50 = 0,5 (mol)
⇒ a : b = 1 : 0,5 = 2 : 1
Câu 9: Lưu huỳnh tác dụng với axit sunfuric đặc, nóng:
S + 2H2SO4 đặc 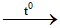
Trong phản ứng này, tỉ lệ số nguyên tử lưu huỳnh bị khử và số nguyên tử lưu huỳnh bị oxi hoá là:
A. 1 : 2.
B. 1 : 3.
C. 3 : 1.
D. 2 : 1.
Đáp án: D

Câu 10: Lưu huỳnh có thể tồn tại ở những trạng thái số oxi hoá nào ?
A. -2; +4; +5; +6
B. -3; +2; +4; +6.
C. -2; 0; +4; +6
D. +1 ; 0; +4; +6
Đáp án: C
Thi online Hóa 10 KNTTThi online Hóa 10 CDThi online Hóa 10 CTST
Xem thêm Bài tập & Câu hỏi trắc nghiệm Hóa học 10 cực hay có đáp án khác:
- 100 Bài tập trắc nghiệm Nguyên tử
- 100 Bài tập trắc nghiệm Bảng tuần hoàn các nguyên tố hóa học và định luật tuần hoàn
- 100 Bài tập trắc nghiệm Liên kết hóa học
- 100 Bài tập trắc nghiệm Phản ứng oxi hóa - khử
- 100 Bài tập trắc nghiệm Nhóm halogen
- 100 Bài tập trắc nghiệm Tốc độ phản ứng và cân bằng hóa học
Để học tốt lớp 10 các môn học sách mới:
- Giải bài tập Lớp 10 Kết nối tri thức
- Giải bài tập Lớp 10 Chân trời sáng tạo
- Giải bài tập Lớp 10 Cánh diều
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 10 Global Success
- Giải Tiếng Anh 10 Friends Global
- Giải sgk Tiếng Anh 10 iLearn Smart World
- Giải sgk Tiếng Anh 10 Explore New Worlds
- Lớp 10 - Kết nối tri thức
- Soạn văn 10 (hay nhất) - KNTT
- Soạn văn 10 (ngắn nhất) - KNTT
- Soạn văn 10 (siêu ngắn) - KNTT
- Giải sgk Toán 10 - KNTT
- Giải sgk Vật lí 10 - KNTT
- Giải sgk Hóa học 10 - KNTT
- Giải sgk Sinh học 10 - KNTT
- Giải sgk Địa lí 10 - KNTT
- Giải sgk Lịch sử 10 - KNTT
- Giải sgk Kinh tế và Pháp luật 10 - KNTT
- Giải sgk Tin học 10 - KNTT
- Giải sgk Công nghệ 10 - KNTT
- Giải sgk Hoạt động trải nghiệm 10 - KNTT
- Giải sgk Giáo dục quốc phòng 10 - KNTT
- Lớp 10 - Chân trời sáng tạo
- Soạn văn 10 (hay nhất) - CTST
- Soạn văn 10 (ngắn nhất) - CTST
- Soạn văn 10 (siêu ngắn) - CTST
- Giải Toán 10 - CTST
- Giải sgk Vật lí 10 - CTST
- Giải sgk Hóa học 10 - CTST
- Giải sgk Sinh học 10 - CTST
- Giải sgk Địa lí 10 - CTST
- Giải sgk Lịch sử 10 - CTST
- Giải sgk Kinh tế và Pháp luật 10 - CTST
- Giải sgk Hoạt động trải nghiệm 10 - CTST
- Lớp 10 - Cánh diều
- Soạn văn 10 (hay nhất) - Cánh diều
- Soạn văn 10 (ngắn nhất) - Cánh diều
- Soạn văn 10 (siêu ngắn) - Cánh diều
- Giải sgk Toán 10 - Cánh diều
- Giải sgk Vật lí 10 - Cánh diều
- Giải sgk Hóa học 10 - Cánh diều
- Giải sgk Sinh học 10 - Cánh diều
- Giải sgk Địa lí 10 - Cánh diều
- Giải sgk Lịch sử 10 - Cánh diều
- Giải sgk Kinh tế và Pháp luật 10 - Cánh diều
- Giải sgk Tin học 10 - Cánh diều
- Giải sgk Công nghệ 10 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 10 - Cánh diều
- Giải sgk Giáo dục quốc phòng 10 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

