Trắc nghiệm Hóa học 10 Bài 23 có đáp án Kết nối tri thức
Với bài tập trắc nghiệm Hóa học 10 Bài 23 có đáp án sách mới Kết nối tri thức đầy đủ các mức độ nhận biết, thông hiểu, vận dụng sẽ giúp học sinh ôn tập trắc nghiệm Hóa 10 Bài 23. Bạn vào tên bài học hoặc Xem chi tiết để theo dõi bài viết.
Trắc nghiệm Hóa học 10 Bài 23 có đáp án Kết nối tri thức
Thi online Hóa 10 KNTTThi online Hóa 10 CDThi online Hóa 10 CTST
Lưu trữ: Trắc nghiệm Hóa học 10 Bài 23: Hiđro clorua; Axit clohiđric và muối clorua (sách cũ)
Bài 1: Phản ứng trong đó HCl thể hiện tính khử là
A. HCl + NaOH → NaCl + H2O
B. 2HCl + Mg → MgCl2 + H2
C. MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
D. CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Đáp án: C
Bài 2: Cho các phản ứng sau:
4HCl + MnO2 → MnCl2 + Cl2 + 2H2O
2HCl + Fe → FeCl2 + H2
3HCl + Fe(OH)3 → FeCl3 + 3H2O
6HCl + 2Al → 2AlCl3 + 3H2
16HCl + 2KMnO4 → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
Số phản ứng trong đó HCl thể hiện tính oxi hóa là
A. 2 B. 1 C. 4 D. 3
Đáp án: A
Bài 3: Cho 23,7 gam KMnO4 phản ứng hết với dung dịch HCl đặc (dư), thu được V lít khí Cl2 (đktc). Giá trị của V là
A. 6,72 B. 8,40 C. 3,36 D. 5,60
Đáp án: B
nKMnO4 = 0,15 mol
Bảo toàn electron
2nCl2 = 5nKMnO4 ⇒ nCl2 = 0,375 mol ⇒ V = 8,4l
Bài 4: Cho 0,5 gam một kim loại hóa trị II phản ứng hết với dung dịch HCl dư, thu được 0,28 lít H2 (đktc). Kim loại đó là
A. Ca B. Ba C. Sr D. Mg
Đáp án: A
nH2 = 0,0125 mol
Bảo toàn electron
2nM = 2nH2 ⇒ nM = nH2 = 0,0125 mol
⇒ M = 0,5 / 0,0125 = 40 (Ca)
Bài 5: Hòa tan 2 gam một kim loại M thuộc nhóm IIA trong dung dịch HCl (dư). Cô can dung dịch, thu được 5,55 gam muối. Kim loại X là
A. canxi B. bari C. magie D. beri
Đáp án: A
M + HCl → MCl2 + H2
nM = nMCl2 ⇒
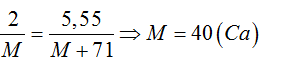
Bài 6: Cho 7,8 gam hỗn hợp X gồm Al, Mg tác dụng với dung dịch HCl dư, thu được 8,96 lít H2 (đktc). Thành phần phần trăm khối lượng của Al trong X là
A. 69,23% B. 34,60% C. 38,46% D. 51,92%
Đáp án: A
nH2 = 0,4 mol
Bảo toàn electron
3nAl + 2nMg = 2nH2 ⇒ 3nAl + 2nMg = 0,8 (1)
mhh = 27nAl + 24nMg = 7,8 (2)
Giải hệ (1) và (2) ⇒ nAl = 0,2 (mol); nMg = 0,1 mol
⇒ %mAl = 0,2.27/7,8 .100% = 69,23%
Bài 7: Hòa tan hoàn toàn 3,22 gam hỗn hợp X gồm Fe, Mg và Zn bằng một lượng vừa đủ dung dịch HCl, thu được 1,344 lit hidro (đktc) và dung dịch chứa m gam muối. Giá trị của m là
A. 5,23 B. 7,60
C. 7,48 D. 5,35
Đáp án: C
nH2 = 1,334/22,4 = 0,06 mol ⇒ nHCl = 2nH2 = 0,12 mol
Bảo toàn khối lượng
3,22 + 0,12.365 = m + 0,06.2 ⇒ m = 7,48 gam
Bài 8: Hòa tan hoàn toàn 20,6 gam hỗn hợp gồm Na2CO3 và CaCO3 bằng dung dịch HCl dư, thu được V lít CO2 (đktc) và dung dịch chứa 22,8 gam hỗn hợp muối. Giá trị của V là
A. 4,48 B. 1,79
C. 5,6 D. 2,24
Đáp án:
nH2O = nCO2 = a mol ⇒ nHCl = 2nH2O = 2a mol
Bảo toàn khối lượng:
20,6 + 2a.36,5 = 22,8 + 44a + 18a ⇒ a = 0,2 mol
⇒ V = 0,2.22,4 = 4,48 lít
Bài 9: Hòa tan hoàn toàn 2,96 gam hỗn hợp X gồm Fe, Zn, Al bằng dung dịch HCl dư, thu được 1,568 lít khí H2 (đktc). Mặt khác, cho 2,96 gam X phản ứng hoàn toàn với khí Cl2 dư, thu được 8,64 gam muối. Khối lượng Al trong 2,96 gam X là
A. 0,54 gam. B. 0,81 gam.
C. 0,27 gam. D. 1,08 gam.
Đáp án:
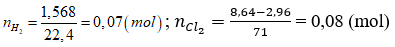
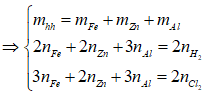
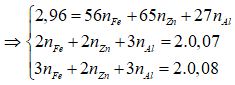
⇒ nFe = nZn = nAl = 0,02 mol ⇒ nAl = 0,02.27 = 0,54 gam
Bài 10: Hòa tan hoàn toàn hỗn hợp X gồm Fe và Mg bằng một lượng vừa đủ dung dịch HCl 20%, thu được dung dịch Y. Nồng độ phần trăm của FeCl2 trong dung dịch Y là 15,76%. Nồng độ phần trăm của MgCl2 trong dung dịch Y là
A. 24,24% B. 11,79%
C. 28,21% D. 15,76%
Đáp án:
Lấy 1 mol
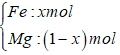
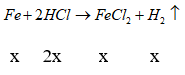
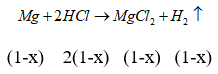
nH2 = 1 mol; nHCl = 2 mol
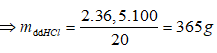
mdd Y = 56x + 24(1 - x) + 365 - 1.2 = 387 + 32x
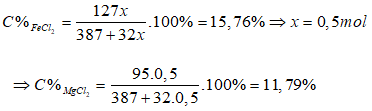
Bài 11: Nhúng giấy quỳ tím vào dung dịch HCl, quỳ tím
A. hóa đỏ. B. hóa xanh. C. không đổi màu. D. mất màu.
Đáp án: A
Bài 12: Kim loại tác dụng với dung dịch HCl và tác dụng với khí Cl2 đều thu được cùng một muối là
A. Fe B. Zn C. Cu D. Ag
Đáp án: B
Bài 13: Trong phòng thí nghiệm có thể điều chế khí hidro clorua bằng cách
A. Cho NaCl tinh thể tác dụng với H2SO4 đặc, đun nóng.
B. Cho NaCl tinh thể tác dụng với HNO3 đăc, đun nóng.
C. Cho NaCl tinh thể tác dụng với H2SO4 loãng, đun nóng.
D. Cho NaCl tinh thể tác dụng với HNO3 loãng, đun nóng.
Đáp án: A
Bài 14: Phát iểu nào sau đây sai?
A. NaCl được dung làm muối ăn và bảo quản thực phẩm.
B. HCl là chất khí không màu, mùi xốc, ít tan trong nước.
C. Axit clohidric vừa có tính oxi hóa, vừa có tính khử.
D. Nhỏ dung dịch AgNO3 vào dung dịch HCl, có kết tủa trắng.
Đáp án: B
Bài 15: Khi cho các chất: Ag, Cu, CuO, Al, Fe vào dung dịch axit HCl thì các chất đều bị tan hết là
A. Cu, Al, Fe
B. Cu, Ag, Fe
C. CuO, Al, Fe
D. Al, Fe, Ag
Đáp án: C
Bài 16: Dãy gồm các chất đều tác dụng được với dung dịch HCl loãng là
A. KNO3, CaCO3, Fe(OH)3
B. NaHCO3, AgNO3, CuO
C. FeS, BaSO4, KOH
D.AgNO3, (NH4)2CO3, CuS
Đáp án: B
Thi online Hóa 10 KNTTThi online Hóa 10 CDThi online Hóa 10 CTST
Xem thêm Bài tập & Câu hỏi trắc nghiệm Hóa học 10 có lời giải hay khác:
- Trắc nghiệm Sơ lược về hợp chất có oxi của clo (có lời giải)
- Trắc nghiệm Flo - Brom - Iot (có lời giải)
- Trắc nghiệm Luyện tập nhóm halogen (có lời giải)
- Trắc nghiệm Tính chất hóa học của khí clo và hợp chất của clo (có lời giải)
- Trắc nghiệm Tính chất hóa học của brom và iot (có lời giải)
Để học tốt lớp 10 các môn học sách mới:
- Giải bài tập Lớp 10 Kết nối tri thức
- Giải bài tập Lớp 10 Chân trời sáng tạo
- Giải bài tập Lớp 10 Cánh diều
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 10 Global Success
- Giải Tiếng Anh 10 Friends Global
- Giải sgk Tiếng Anh 10 iLearn Smart World
- Giải sgk Tiếng Anh 10 Explore New Worlds
- Lớp 10 - Kết nối tri thức
- Soạn văn 10 (hay nhất) - KNTT
- Soạn văn 10 (ngắn nhất) - KNTT
- Soạn văn 10 (siêu ngắn) - KNTT
- Giải sgk Toán 10 - KNTT
- Giải sgk Vật lí 10 - KNTT
- Giải sgk Hóa học 10 - KNTT
- Giải sgk Sinh học 10 - KNTT
- Giải sgk Địa lí 10 - KNTT
- Giải sgk Lịch sử 10 - KNTT
- Giải sgk Kinh tế và Pháp luật 10 - KNTT
- Giải sgk Tin học 10 - KNTT
- Giải sgk Công nghệ 10 - KNTT
- Giải sgk Hoạt động trải nghiệm 10 - KNTT
- Giải sgk Giáo dục quốc phòng 10 - KNTT
- Lớp 10 - Chân trời sáng tạo
- Soạn văn 10 (hay nhất) - CTST
- Soạn văn 10 (ngắn nhất) - CTST
- Soạn văn 10 (siêu ngắn) - CTST
- Giải Toán 10 - CTST
- Giải sgk Vật lí 10 - CTST
- Giải sgk Hóa học 10 - CTST
- Giải sgk Sinh học 10 - CTST
- Giải sgk Địa lí 10 - CTST
- Giải sgk Lịch sử 10 - CTST
- Giải sgk Kinh tế và Pháp luật 10 - CTST
- Giải sgk Hoạt động trải nghiệm 10 - CTST
- Lớp 10 - Cánh diều
- Soạn văn 10 (hay nhất) - Cánh diều
- Soạn văn 10 (ngắn nhất) - Cánh diều
- Soạn văn 10 (siêu ngắn) - Cánh diều
- Giải sgk Toán 10 - Cánh diều
- Giải sgk Vật lí 10 - Cánh diều
- Giải sgk Hóa học 10 - Cánh diều
- Giải sgk Sinh học 10 - Cánh diều
- Giải sgk Địa lí 10 - Cánh diều
- Giải sgk Lịch sử 10 - Cánh diều
- Giải sgk Kinh tế và Pháp luật 10 - Cánh diều
- Giải sgk Tin học 10 - Cánh diều
- Giải sgk Công nghệ 10 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 10 - Cánh diều
- Giải sgk Giáo dục quốc phòng 10 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

