Đề kiểm tra 1 tiết Hóa học 11 Học kì 1 có đáp án (Bài số 1)
Đề kiểm tra 1 tiết Hóa học 11 Học kì 1 có đáp án (Bài số 1)
Thi online Hóa 11 KNTTThi online Hóa 11 CDThi online Hóa 11 CTST
Câu 1: Dãy các chất nào sau đây KHÔNG PHẢI là chất điện li ?
A. NaCl, CaCO và HNO B. CH3COOH, HCl và Ba(OH)2
C. H2O , CH3COOH và Mg(OH)2 D. C2H5OH , C5H12O6 và CH3CHO
Đáp án: D
Câu 2: Cho các chất sau đây : H2O HCl , NaOH , NaCl, CH3COOH , CuSO4. Các chất điện li yếu là
A. H2O, CH3COOH , CuSO4 B. CH3COOH, CuSO4
C. H2O, CH3COOH D. H2O , NaCl, CH3COOH , CuSO4
Đáp án: C
Câu 3: HCOOH là một axit yếu. Độ điện li của axit này sẽ biến đổi như thế nào khi nhỏ vào dung dịch HCOOH vài giọt dung dịch HCl (coi V không thay đổi )?
A. tăng B. giảm
C. không biến đổi D. không xác định được.
Đáp án: B
Câu 4: Cho các dung dịch : NH3, NaOH, Ba(OH)2 có cùng nồng độ mol và có các giá trị pH lần lượt là pH1,pH2 và pH3. Sự sắp xếp nào sau đây đúng ?
A. pH1 < pH2 < pH3 B. pH1 < pH3 < pH2
C. pH3 < pH2 < pH1 D. pH3 < pH1 < pH2
Đáp án: A
Câu 5: Một trong các nguyên nhân gây bệnh đau dạ dầy là do lượng axit trong dạ dày quá cao. Để giảm bớt lượng axit, người ta thường uống dược phẩm Nabica (NaHCO3). Phương trình ion rút gọn của phản ứng xảy ra là
A. 2H+ + CO → H2O + CO2
B. H+ + OH- → H2O.
C. H+ + NaHCO3 → Na+ + H2O + CO2.
D. H+ + HCO → H2O + CO2
Đáp án: D
Câu 6: Những cặp chất nào sau đây cùng tồn tại trong một dung dịch ?
A. NaHCO3 và NaOH B. K2SO4 và NaNO3
C. HCl và AgNO3 D. NaHSO3 và NaHSO4.
Đáp án: B
Câu 7: Trong dãy các ion sau dãy nào chứa các ion đều phản ứng được với OH-
A. NH4+, HCO3-, CO32- B. Mg2+ ,HSO3- ,SO32-
C. H+, Ba2+, Al3+ D. Fe3+ ,HPO42- ,HS-
Đáp án: D
Câu 8: Dung dịch Ba(OH)2 có thể tác dụng với tất cả các chất trong dãy nào sau đây ?
A. FeCl3, MgO, SO2, H2SO4 B.CO2, Al(OH)3, Fe(OH)3 và Na2CO3
C. ZnCl2, Cl2, P2O5,KHSO4 D. NH3,Zn(OH)2,FeO, NaHCO3
Đáp án: C
Câu 9: Cho các cặp dung dịch sau :
(1) BaCl2 và Na2CO3; (2) NaOH và AlCl33;
(3) BaCl2 và NaHSO4; (4) Ba(OH)2 và H2SO4
(5) Pb(NO3)2 và Na2S
Số trường hợp xảy ra phản ứng khi trộn các dung dịch trong từng cặp với nhau là
A. 5. B. 4. C. 3. D. 2.
Đáp án: A
Câu 10: Có 12 ion : NH4+, Al3+, Ag+, Ba2+, Mg2+, SO42-, CO32-, NO3-, Cl-, Br-, PO43- thuộc 3 dung dịch loãng X, Y, Z ; mỗi dung dịch chứa 2 cation, 2 anion không trùng lập. Dung dịch X có thể chứa các ion là
A. NH4+ , Al3+, SO42- , Cl- B. Mg2+, Na+, NO3- , Br-
C. NH4+ , Ba2+ , NO3- , Cl- D. NH4+ , Na+, CO32- , PO43-
Đáp án: D
Câu 11: Cho Ba dư vào dung dịch đồng thời chứa các ion : NH4+ , HCO3- , SO42- ,K+ . Số phản ứng xảy ra là
A. 2. B. 3. C. 4. D. 5.
Đáp án: C
Câu 12: Cho dung dịch Ba(HCO3)2 lần lượt vào các dung dịch : CaCl2, NaOH, Na2CO3, KHSO4, Na2SO4, Ca(OH)2, H2SO4, HCl. Số trường hợp có tạo ra kết tuả là
A. 6. B. 5. C. 7. D. 4.
Đáp án: A
Câu 13: cho các dung dịch sau ; Ba(OH)2, NaHSO4, K2CO3, Ba(HCO3)2. Khi trộn lần lượt các dung dịch vào nhau từng đôi một thì số cặp chất phản ứng xảy ra là
A. 5. B. 6. C. 7. D. 8.
Đáp án: B
Câu 14: X,Y,Z là các dung dịch muối (trung hoà hoặc axit) ứng với 3 gốc axit khác nhau, thỏa mãn điều kiện; X tác dụng với Y có khí thoát ra ; Y tác dụng với Z có kết tủa ; X tác dụng với Z vừa có khí vừa tạo kết tủa. X , Y , Z lần lượt là
A. CaCO3, NaHSO4, Ba(HSO3)2. B. NaHSO4, Na2CO3, Ba(HSO3)2.
C. Na2CO3, NaHSO3, Ba(HSO3)2. D. , NaHSO4,CaCO3, Ba(HSO3)2.
Đáp án: B
Câu 15: Cho các phản ứng xảy ra trong dung dịch :
(1) BaS + H2SO4 (2) AgNO3 + (NH4)3PO4
(3) Na2CO3 + CaCl2 (4) Mg(HCO3)2 + HCl
(5) (NH4)2SO4 + KOH (6) NH4HCO3 + Ba(OH)2
Trong số các phản ứng trên, số phản ứng thu được sản phẩm đồng thời có cả kết tủa và khí bay ra là
A. 2. B. 3. C. 4. D. 5.
Đáp án: A
(1) và (6)
1) BaS + H2SO4 → BaSO4 + H2S
6) NH4HCO3 + Ba(OH)2 → BaCO3 + NH3 + 2H2O
Câu 16: Chỉ dùng 1 thuốc thử có thể phân biệt các dung dịch nào sau đây bằng phương pháp hóa học ?
A. K2SO4, NaNO3, NH4NO3,Na2CO3.
B. K2SO3, (NH4)2SO4, Na2SO4, NH4Cl
C. NaCl, NH4NO3, (NH4)2SO4, (NH4)2CO3
D. (NH4)2SO4, NaNO3, NH4NO3, Na2CO3
Đáp án: D
Sử dụng Ba(OH)2, hiện tượng
(NH4)2SO4: Có khí mùi khai và kết tủa trắng
NaNO3: Không hiện tượng
NH4NO3: Có khí mùi khai
Na2CO3: Có sủi bọt khí không mùi
Câu 17: Trộn 100 ml dung dịch gồm Ba(OH)2 0,1M và NaOH 0,1M với 400 ml dung dịch gồm H2SO4 0,0375M và HCl 0,0125M thu được dung dịch X. giá trị pH của dung dịch X là
A. 7. B. 2. C. 1. D. 6.
Đáp án: B
nOH- = 2. 0,1. 0,1 + 0,1. 0,1 = 0,03
nH+ = 0,0375. 2. 0,4 + 0,0125. 0,4 = 0,035
⇒ H+ dư; ndư = 0,035 - 0,03 = 0,005 mol
[H+] = 0,005 : (0,1 + 0,4) = 0,01 ⇒ pH = 2
Câu 18: Khi cho 100 ml dung dịch KOH 1M vào 100 ml dung dịch HCl thu được dung dịch có chứa 6,525 gam chất tan. Nồng độ mol của HCl trong dung dịch đã dùng là
A. 0,75M. B. 1M. C. 0,25M. D. 0,5M.
Đáp án: D
KOH + HCl → KCl + H2O
nKOH = 0,1 mol
Nếu chất tan chỉ có KCl
⇒ nKCl = 0,1 mol ⇒ mKCl = 0,1. 74,5 = 7,45 > 6,525g
⇒ chất tan chứa KCl dư
Đặt nKCl = x; nKOH dư = y
x + y = 0,1
74,5x + 56y = 6,525
⇒ x = y = 0,05
⇒ nHCl = nKCl = 0,05 mol ⇒ CM(HCl) = 0,5M
Câu 19: Cho 100 ml dung dịch H3PO4 vào 200 ml dung dịch NaOH 1,2M thì thu được dung dịch có chứa 19,98 gam chất tan. Nồng độ mol của dung dịch H3PO4 là
A. 1,5M. B. 0,1M. C. 1,2M. D. 1,6M.
Đáp án: A
nNaOH = 0,2.1,2 = 0,24 mol
Gọi nồng độ H3PO4 là x
Nếu NaOH vừa đủ ⇒ nH2O sinh ra = 0,24 mol
⇒ muối là Na3PO4 0,08 mol ⇒ mchất tan = 0,08.164 = 13,12 gam < 19,98
Vậy NaOH hết, H3PO4 dư để tạo muối axit, tăng khối lượng chất tan
Bảo toàn khối lượng: mH3PO4 + mNaOH = mchất tan + mH2O
98.0,1x + 40.0,2 = 19,98 + 18.0,24 ⇒ x = 1,5 mol/l
Câu 20: Cho 6,9 gam Na vào 100,0 ml dung dịch HCl thu được dung dịch chứa 14,59 gam chất tan. Cho dung dịch X vào dung dịch AgNO3 dư, thu được số gam kết tủa là
A. 39,20 gam. . B. 38,65 gam. C. 37,58 gam. D. 40,76 gam.
Đáp án: B
2Na + 2H2O → 2NaOH + H2 ↑
NaOH + HCl → NaCl + H2O
nNaOH = nNa = 0,3 mol
Nếu chất tan chỉ có NaCl ⇒ nNaCl = 0,3 mol
⇒ mNaCl = 0,3.58,5 = 17,55 > 14,59 gam ⇒ chất tan phải chứa NaOH dư
Đặt nNaCl = x ; nNaOH = y
⇒ x + y = 0,3
58,5x + 40y = 14,59
⇒ x = 0,14; y = 0,16
Ag+ + Cl+ → AgCl ↓
2Ag+ + OH- → Ag2O ↓ + H2O
⇒ nAgCl = nCl - = nNaCl = 0,14 mol
nAg2O = 1/2 nOH- = 1/2 nNaOH = 0,08 mol
⇒ mkết tủa = 143,5.0,14 + 232.0,08 = 38,65 gam
Câu 21: Cho 3,36 lít khí CO2 vào 200 ml dung dịch chứa NaOH x(M) và Na2CO3 0,4M thu được dung dịch X chứa 19,98 gam hỗn hợp muối. Giá trị của X là
A. 0,70. B. 0,50. C. 0,75. D. 0,60.
Đáp án: B
Hỗn hợp muối gồm NaHCO3 (a mol) và Na2CO3 (b mol)
nCO2 = 0,15 mol
nNa2CO3 = 0,08 mol
Áp dụng phương pháp bảo toàn nguyên tố đối với Na và C suy ra:
84a + 106b = 19,98
a + b = 0,15 + 0,08
a + 2b = 0,2x + 0,16
⇒ a = 0,2; b= 0,03; x = 0,5
Câu 22: Hấp thụ hoàn toàn 4,48 lít khí CO2 (đktc) vào 500 ml dung dịch hỗn hợp gồm NaOH 0,1M và Ba(OH)2 0,2M, sinh ra m gam kết tủa. Giá trị của m là
A. 9,85. B. 11,82. C. 19,70. D. 17,73.
Đáp án: A
nCO2 = 0,2 mol;
nOH- = 0,1. 0,5 + 0,2. 2. 0,5 = 0,25 mol
Ta có: 1 < nOH-/nCO2 < 2 ⇒ Tạo 2 muối
Gọi nCO32- = x mol; nHCO3- = y mol
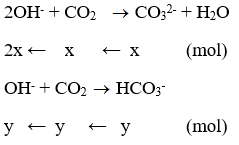
Ta có
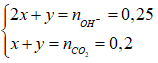
⇒ x = 0,05 mol; y = 0,15 mol
nBa2+ = 0,1 ⇒ nBaCO3 = nCO32- = 0,05
⇒ m = 0,05. 197 = 9,85 gam
Câu 23: Cho dung dịch Ca(OH)2 dư vào 100 ml dung dịch Mg(HCO3)2 0,15M, sau phản ứng thu được m gam kết tủa. Giá trị của m là
A. 0,87. B. 2,37. C. 3,87. D. 2,76.
Đáp án: D
nHCO3- = 0,03 mol
OH- (0,03) + HCO3- (0,03) → CO32- (0,03 mol) + H2O
nOH- = 0,03 ⇒ nCa2+ = nCa(OH)2 = 0,015 mol
m = mMgCO3 + mCaCO3 = mCa2+ + mMg2+ + mCO32-
m = 0,015. 40 + 0,015. 24 + 0,03. 60 = 2,76 gam
Câu 24: Cho 3,36 lít khí CO2 (đktc) vào 400 ml dung dịch hỗn hợp KOH 0,25M và K2CO3 0,4M thu được dung dịch X. cho dung dịch BaCl2 dư vào dung dịch X thu được kết tủa, lọc lấy kết tủa đem ung đến khối lượng không đổi thu được m gam chất rắn. Giá trị của m là
A. 16,83. B. 21,67. C. 71,91. D. 48,96.
Đáp án: A
nCO2 = 0,15 mol
nOH- = 0,1 mol; nCO32- = 0,16 mol
CO2 (0,15) + 2OH- (0,1 mol) → CO32- + H2O
CO2 dư; nCO32- = nCO2 pư = 1/2. nOH- = 0,05 mol ⇒ nCO2 dư = 0,1
0,16 + 0,05 = 0,21 mol ⇒ nBaCO3 = 0,21 mol
CO32- (0,21) + CO2 (0,1 mol) + H2O → 2HCO3-
CO32- dư; nCO32- pư = nCO2 = 0,1 mol
nCO32- dư = nBaCO3 = 0,21 – 0,1 = 0,11 mol
BaCO3 (0,11) -to→ BaO (0,11 mol) + CO2
mBaO = m = 0,11.153 = 16,83 gam
Câu 25: Lấy a gam P2O5 cho tác dụng với 338 ml dung dịch NaOH 2M. Sau phản ứng cô cạn dung dịch thu được 3a gam chất rắn. Giá trị của a là
A. 11,36. B. 17,04. C. 12,78. D. 14,20.
Đáp án: A
nP2O5 = a/142 ⇒ nH3PO4 = 2. (a/142) = 0,08
+ Nếu NaOH dư
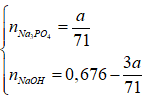
⇒ 3a = 164.a/71 + 40.(0,676 - 3a/71) ⇒ m = 11,36 (A)
+ Nếu NaOH hết ⇒ các kết quả không cho như đáp án
Câu 26: Dung dịch X chứa 0,07 mol Na+; 0,02 mol SO42- và x mol OH-. Dung dịch Y chứa CO4- , NO3- và y mol H+ , tổng số mol ClO và NO là 0,04. Trộn X và Y được 100 ml dung dịch Z. Dung dịch Z cố pH (bỏ qua sự diện li của H2O là
A. 12. B. 2. C. 1. D. 13.
Đáp án: C
Bảo toàn điện tích với dung dịch X và Y ta có: x = 0,03 mol; y = 0,04 mol
Trộn X và Y: H+ + OH- → H2O
⇒ H+ dư = 0,01 mol ⇒ [H+] = 0,01 : 0,1 = 0,1
⇒ pH = 1
Câu 27: Cho m gam NaOH vào 2 lít dung dịch NaHCO3 nồng độ a mol/l thu được 2 lít dung dịch X. Lấy 1 lít dung dịch X tác dụng với dung dịch BaCl2 (dư) thu được 11,82 gam kết tủa. Mặt khác cho 1 lít dung dịch X vào dung dịch CaCl2 (dư) rồi đun nóng, sau khi kết thúc các phản ứng thu được 7,0 gam kết tủa. Giá trị của a và m tương ứng là
A. 0,08 và 4,8. B. 0,04 và 4,8.
C. 0,14 và 2,4. D. 0,07 và 3,2.
Đáp án: A
OH- + HCO3- → CO32- + H2O
Lấy 1 lít dung dịch X ( 1/2 dung dịch X):
nBaCO3 = 0,06 < 0,07 = nCaCO3 ⇒ Trong X có HCO3-
2HCO3- -to→ CO32- + CO2 + H2O
⇒ nHCO3- = ( 0,07 – 0,06). 2 = 0,02
nHCO3- ban đầu = 0,02 + 0,06 = 0,08 mol ⇒ a = 0,08
nOH- = nCO32- = 0,06 mol (1 lít dung dịch X)
m = 2. 0,06. 40 = 4,8 gam
Chú ý: các số liệu tính toán xử lí khi lấy 1l dung dịch X (1/2 dung dịch X ban đầu) do đó khi tính a và m phải nhân 2.
Câu 28: Dung dịch X chứa các ion : Ca2+ ,Na+ , HCO3- và Cl , trong đó số mol của Cl- là 0,1. cho 1/2 dung dịch X phản ứng với dung dịch NaOH (dư), thu được 2 gam kết tủa. Cho 1/2 dung dịch X còn lại phản ứng với dung dịch Ca(OH)2 (dư), thu được 3 gam kết tủa. Mặt khác nếu đun sôi đến cạn dung dịch X thì thu được m gam chất rắn khan. Giá trị của m là
A. 9,21. B. 9,26. C. 8,79. D. 7,47.
Đáp án: C
1/2 dung dịch X: n↓phần 1 = 0,02 < n↓phần 2 = 0,03
phần 1: Ca2+ kết tủa hết, CO32- dư ⇒ nCa2+ (trong X) = 0,02. 2 = 0,04mol
Bảo toàn C: nHCO3- = n↓phần 2 = 0,03 ⇒ nHCO3- (trong X) = 0,06 mol
Bảo toàn điện tích ⇒ nNa+ = 0,08
Đun sôi X: 2HCO3- -to→ CO32- + CO2 + H2O
nCO32- = 1/2. nHCO3- = 0,03 mol
m = mNa+ + mCa2+ + mCO32- + mCl-
m = 0,08.23 + 0,04.40 + 0,03.60 + 0,1.35,5 = 8,79 gam
Câu 29: Hòa tan vào nước 3,38 gam hỗn hợp muối cacbonat và muối hiđrocacbonat của một kim loại hóa trị I. Dung dịch thu được cho tác dụng với dung dịch HCl dư thấy có 0,672 lít khí (đktc) bay ra. Số mol muối cacbonat trong hỗn hợp trên là
A. 0,2. B. 0,02. C. 0,1. D. 0,01.
Đáp án: D
Bảo toàn C: nHCO3- + nCO32- = nCO2 = 0,03 mol
Gọi kim loại hóa trị I là R: R2CO3 (x mol); RHCO3 (y mol)
Ta có x + y = 0,03 mol (1)
mmuối = (2R + 60)x + (R + 61)y = 3,38 gam (2)
R + 61 < 3,38/(x + y) < 2R + 60
26 < R < 51 ⇒ R = 39 (K)
Với R = 39, giải hệ (1)(2) ⇒ x = 0,01
Câu 30: Hấp thu hoàn toàn 2,24 lít CO2 (đktc) cào 100 ml dung dịch gồm K2CO3 0,2M và KOH x mol/lit, sau khi phản ứng xảy ra hoàn toàn thu được dung dịch Y. Cho toàn bộ Y tác dụng với dung dịch BaCl2 (dư), thu được 11,82 gam kết tủa. Giá trị của x là
A. 1,6. B. 1,2. C. 1,0. D. 1,4.
Đáp án: D
nCO32- ban đầu = 0,02 mol
nBaCO3 = 0,06 mol ⇒ nCO32- thêm = 0,04 mol
nCO2 = 0,1 mol > nCO32- thêm ⇒ trong Y có 2 muối HCO3- và CO32-
CO2 (0,04) + 2OH- (0,08) → CO32- (0,04 mol) + H2O
→ nCO2 tạo muối axit = 0,1 – 0,04 = 0,06
CO2 (0,06) + OH- (0,06 mol) → HCO3-
⇒ nOH- = 0,08 + 0,06 = 0,14 mol ⇒ x = 1,4
Thi online Hóa 11 KNTTThi online Hóa 11 CDThi online Hóa 11 CTST
Xem thêm Bài tập & Câu hỏi trắc nghiệm Hóa học 11 có đáp án khác:
- 15 bài tập trắc nghiệm Nitơ (có đáp án)
- 16 bài tập trắc nghiệm Amoniac và muối amoni (có đáp án)
- 16 bài tập trắc nghiệm Axit nitric và muối nitrat (có đáp án)
- 15 bài tập trắc nghiệm Photpho (có đáp án)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 11 Global Success
- Giải sgk Tiếng Anh 11 Smart World
- Giải sgk Tiếng Anh 11 Friends Global
- Lớp 11 - Kết nối tri thức
- Soạn văn 11 (hay nhất) - KNTT
- Soạn văn 11 (ngắn nhất) - KNTT
- Giải sgk Toán 11 - KNTT
- Giải sgk Vật Lí 11 - KNTT
- Giải sgk Hóa học 11 - KNTT
- Giải sgk Sinh học 11 - KNTT
- Giải sgk Lịch Sử 11 - KNTT
- Giải sgk Địa Lí 11 - KNTT
- Giải sgk Giáo dục KTPL 11 - KNTT
- Giải sgk Tin học 11 - KNTT
- Giải sgk Công nghệ 11 - KNTT
- Giải sgk Hoạt động trải nghiệm 11 - KNTT
- Giải sgk Giáo dục quốc phòng 11 - KNTT
- Giải sgk Âm nhạc 11 - KNTT
- Lớp 11 - Chân trời sáng tạo
- Soạn văn 11 (hay nhất) - CTST
- Soạn văn 11 (ngắn nhất) - CTST
- Giải sgk Toán 11 - CTST
- Giải sgk Vật Lí 11 - CTST
- Giải sgk Hóa học 11 - CTST
- Giải sgk Sinh học 11 - CTST
- Giải sgk Lịch Sử 11 - CTST
- Giải sgk Địa Lí 11 - CTST
- Giải sgk Giáo dục KTPL 11 - CTST
- Giải sgk Hoạt động trải nghiệm 11 - CTST
- Giải sgk Âm nhạc 11 - CTST
- Lớp 11 - Cánh diều
- Soạn văn 11 Cánh diều (hay nhất)
- Soạn văn 11 Cánh diều (ngắn nhất)
- Giải sgk Toán 11 - Cánh diều
- Giải sgk Vật Lí 11 - Cánh diều
- Giải sgk Hóa học 11 - Cánh diều
- Giải sgk Sinh học 11 - Cánh diều
- Giải sgk Lịch Sử 11 - Cánh diều
- Giải sgk Địa Lí 11 - Cánh diều
- Giải sgk Giáo dục KTPL 11 - Cánh diều
- Giải sgk Tin học 11 - Cánh diều
- Giải sgk Công nghệ 11 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 11 - Cánh diều
- Giải sgk Giáo dục quốc phòng 11 - Cánh diều
- Giải sgk Âm nhạc 11 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

