Hãy phân tích để xác định dung lượng phối trí của các phối tử OH− Cl− NH3 CH3NH2
Giải Chuyên đề Hóa 12 Bài 6: Một số khái niệm cơ bản về phức chất - Chân trời sáng tạo
Luyện tập trang 36 Chuyên đề Hóa học 12: Hãy phân tích để xác định dung lượng phối trí của các phối tử OH−, Cl−, NH3, CH3NH2.
Lời giải:
- Mỗi ion OH− có 2 cặp electron hoá trị:
Tuy nhiên, khi tạo phức chất, mỗi phối tử OH− chỉ có dung lượng phối trí bằng 1 (do chỉ có thể hình thành một liên kết σ với nguyên tử trung tâm trong phức chất).
- Mỗi ion Cl− có 4 cặp electron hoá trị:
Tuy nhiên, khi tạo phức chất, mỗi phối tử Cl− chỉ có dung lượng phối trí bằng 1 (do chỉ có thể hình thành một liên kết σ với nguyên tử trung tâm trong phức chất).
- Mỗi phân tử NH3 có một cặp electron hoá trị , có thể cho nguyên tử trung tâm để hình thành một liên kết σ với nguyên tử trung tâm trong phức chất nên mỗi phối tử NH3 có dung lượng phối trí bằng 1.
- Mỗi phân tử CH3NH2 có một cặp electron hoá trị , có thể cho nguyên tử trung tâm để hình thành một liên kết σ với nguyên tử trung tâm trong phức chất nên mỗi phối tử CH3NH2 có dung lượng phối trí bằng 1.
Lời giải bài tập Chuyên đề Hóa 12 Bài 6: Một số khái niệm cơ bản về phức chất hay khác:
Xem thêm lời giải bài tập Chuyên đề học tập Hóa học 12 Chân trời sáng tạo hay, chi tiết khác:
Xem thêm các tài liệu học tốt lớp 12 hay khác:
- Giải Chuyên đề học tập Hóa 12 Kết nối tri thức
- Giải Chuyên đề học tập Hóa 12 Chân trời sáng tạo
- Giải Chuyên đề học tập Hóa 12 Cánh diều
- Giải lớp 12 Kết nối tri thức (các môn học)
- Giải lớp 12 Chân trời sáng tạo (các môn học)
- Giải lớp 12 Cánh diều (các môn học)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 12 Global Success
- Giải sgk Tiếng Anh 12 Smart World
- Giải sgk Tiếng Anh 12 Friends Global
- Lớp 12 Kết nối tri thức
- Soạn văn 12 (hay nhất) - KNTT
- Soạn văn 12 (ngắn nhất) - KNTT
- Giải sgk Toán 12 - KNTT
- Giải sgk Vật Lí 12 - KNTT
- Giải sgk Hóa học 12 - KNTT
- Giải sgk Sinh học 12 - KNTT
- Giải sgk Lịch Sử 12 - KNTT
- Giải sgk Địa Lí 12 - KNTT
- Giải sgk Giáo dục KTPL 12 - KNTT
- Giải sgk Tin học 12 - KNTT
- Giải sgk Công nghệ 12 - KNTT
- Giải sgk Hoạt động trải nghiệm 12 - KNTT
- Giải sgk Giáo dục quốc phòng 12 - KNTT
- Giải sgk Âm nhạc 12 - KNTT
- Giải sgk Mĩ thuật 12 - KNTT
- Lớp 12 Chân trời sáng tạo
- Soạn văn 12 (hay nhất) - CTST
- Soạn văn 12 (ngắn nhất) - CTST
- Giải sgk Toán 12 - CTST
- Giải sgk Vật Lí 12 - CTST
- Giải sgk Hóa học 12 - CTST
- Giải sgk Sinh học 12 - CTST
- Giải sgk Lịch Sử 12 - CTST
- Giải sgk Địa Lí 12 - CTST
- Giải sgk Giáo dục KTPL 12 - CTST
- Giải sgk Tin học 12 - CTST
- Giải sgk Hoạt động trải nghiệm 12 - CTST
- Giải sgk Âm nhạc 12 - CTST
- Lớp 12 Cánh diều
- Soạn văn 12 Cánh diều (hay nhất)
- Soạn văn 12 Cánh diều (ngắn nhất)
- Giải sgk Toán 12 Cánh diều
- Giải sgk Vật Lí 12 - Cánh diều
- Giải sgk Hóa học 12 - Cánh diều
- Giải sgk Sinh học 12 - Cánh diều
- Giải sgk Lịch Sử 12 - Cánh diều
- Giải sgk Địa Lí 12 - Cánh diều
- Giải sgk Giáo dục KTPL 12 - Cánh diều
- Giải sgk Tin học 12 - Cánh diều
- Giải sgk Công nghệ 12 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 12 - Cánh diều
- Giải sgk Giáo dục quốc phòng 12 - Cánh diều
- Giải sgk Âm nhạc 12 - Cánh diều

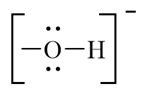





 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

