Chuyên đề Hóa học 10 trang 33 Chân trời sáng tạo
Với lời giải Chuyên đề Hóa học 10 trang 33 trong Bài 5: Sơ lược về phản ứng cháy và nổ Chuyên đề học tập Hóa học 10 Chân trời sáng tạo hay nhất, chi tiết sẽ giúp học sinh dễ dàng trả lời các câu hỏi & làm bài tập Chuyên đề Hóa học 10 trang 33.
Chuyên đề Hóa học 10 trang 33 Chân trời sáng tạo
Mở đầu trang 33 Chuyên đề Hóa học 10: Cháy, nổ là các hiện tượng thường gặp trong đời sống. Các hiện tượng này đã được các nhà khoa học quan tâm, nghiên cứu để phục vụ cho cuộc sống, đồng thời hạn chế những thiệt hại do chúng gây ra. Vậy phản ứng cháy, nổ là gì? Chúng có đặc điểm như thế nào? Khi nào phản ứng cháy, nổ xảy ra?
Lời giải:
Phản ứng cháy là phản ứng oxi hóa – khử giữa chất cháy và chất oxi hóa, có tỏa nhiệt và phát ra ánh sáng.
Điều kiện cần và đủ để phản ứng cháy xảy ra:
+ Điều kiện cần: (1) Chất cháy; (2) Chất oxi hóa; (3) Nguồn nhiệt.
+ Điều kiện đủ:
(1) Nồng độ oxygen trong không khí phải lớn hơn 14% thể tích (ngoại trừ đối với một số chất dễ cháy, gây nổ mạnh);
(2) Nguồn nhiệt phải đạt tới giới hạn bắt cháy của chất cháy;
(3) Thời gian tiếp xúc của 3 điều kiện cần phải đủ lâu để xuất hiện sự cháy.
Phản ứng nổ là phản ứng xảy ra với tốc độ rất lớn kèm theo sự tăng thể tích đột ngột và tỏa lượng nhiệt lớn.
Phản ứng nổ vật lí xảy ra do vật chất bị nén dưới áp suất cao trong một thể tích, làm thể tích được giải phóng đột ngột, gây ra tiếng nổ.
Phản ứng nổ hóa học xảy ra do sự giải phóng năng lượng đột ngột và rất nhanh trong một phản ứng hóa học (có đủ điều kiện của một phản ứng cháy), làm hỗn hợp khí xung quanh giãn nở nhanh chóng dưới áp suất lớn, sinh công và gây nổ.
Câu hỏi 1 trang 33 Chuyên đề Hóa học 10: Quan sát Hình 5.1, nêu hiện tượng và viết phương trình hóa học xảy ra. Xác định vai trò của các chất trong các phản ứng hóa học này và cho biết đây là loại phản ứng hóa học nào.
Lời giải:
a) Magnesium cháy trong không khí
- Hiện tượng: Phản ứng xảy ra mãnh liệt, tỏa nhiệt mạnh, phát ra ánh sáng chói.
- Phương trình hóa học: 2Mg + O2 → 2MgO
- Sự thay đổi số oxi hóa của các chất trong phản ứng:
+ Phản ứng này thuộc loại phản ứng oxi hóa khử.
+ Mg là chất khử (số oxi hóa tăng từ 0 lên +2)
+ O2 là chất oxi hóa (số oxi hóa giảm từ 0 xuống -2)
b) Than đá (carbon) cháy trong không khí
- Hiện tượng: Phản ứng tỏa nhiệt mạnh, phát ra ánh sáng đỏ.
- Phương trình hóa học: C + O2 → CO2
- Sự thay đổi số oxi hóa của các chất trong phản ứng:
+ Phản ứng này thuộc loại phản ứng oxi hóa khử.
+ C là chất khử (số oxi hóa tăng từ 0 lên +4)
+ O2 là chất oxi hóa (số oxi hóa giảm từ 0 xuống -2)
c) Gas (thành phần chính là C3H8 và C4H10) cháy trong không khí
- Hiện tượng: Khí gas cháy với ngọn lửa màu xanh, tỏa nhiệt mạnh.
- Phương trình hóa học:
C3H8 + 5O2 → 3CO2 + 4H2O
C4H10 + O2 → 4CO2 + 5H2O
- Các phản ứng này thuộc loại phản ứng oxi hóa khử vì số oxi hóa của oxi ở dạng đơn chất (O2) bằng 0 giảm xuống -2 (trong hợp chất CO2, H2O)
⇒ O2 là chất oxi hóa; C3H8 và C4H10 là chất khử.
Câu hỏi 2 trang 33 Chuyên đề Hóa học 10: Các phản ứng cháy nêu trên có những đặc điểm chung nào?
Lời giải:
Các phản ứng cháy nêu trên có những đặc điểm chung là:
- Hiện tượng: Đều có tỏa nhiệt và phát sáng.
- Loại phản ứng: Đều là phản ứng oxi hóa – khử.
- Chất oxi hóa đều là O2.
- Phản ứng xảy ra với tốc độ nhanh.
Luyện tập trang 33 Chuyên đề Hóa học 10: Nêu một số ví dụ về phản ứng cháy.
Lời giải:
Một số ví dụ về phản ứng cháy:
- Đốt than, củi để đun nấu, sưởi ấm.
- Đốt dầu để thắp sáng đèn.
- Khí gas cháy để đun nấu.
- Đốt vàng mã.
- Đốt đèn cồn để làm thí nghiệm.
- Đốt cồn để nướng mực
Lời giải bài tập Chuyên đề Hóa 10 Bài 5: Sơ lược về phản ứng cháy và nổ hay khác:
- Chuyên đề Hóa học 10 trang 34
- Chuyên đề Hóa học 10 trang 35
- Chuyên đề Hóa học 10 trang 36
- Chuyên đề Hóa học 10 trang 37
Xem thêm lời giải bài tập Chuyên đề học tập Hóa học 10 Chân trời sáng tạo hay, chi tiết khác:
Chuyên đề Hóa học 10 Bài 6: Điểm chớp cháy, nhiệt độ tự bốc cháy và nhiệt độ cháy
Chuyên đề Hóa học 10 Bài 10: Tính tham số cấu trúc và năng lượng
Xem thêm các tài liệu học tốt lớp 10 hay khác:
- Giải Chuyên đề Hóa học 10 Kết nối tri thức
- Giải Chuyên đề Hóa học 10 Chân trời sáng tạo
- Giải Chuyên đề Hóa học 10 Cánh diều
- Giải lớp 10 Kết nối tri thức (các môn học)
- Giải lớp 10 Chân trời sáng tạo (các môn học)
- Giải lớp 10 Cánh diều (các môn học)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 10 Global Success
- Giải Tiếng Anh 10 Friends Global
- Giải sgk Tiếng Anh 10 iLearn Smart World
- Giải sgk Tiếng Anh 10 Explore New Worlds
- Lớp 10 - Kết nối tri thức
- Soạn văn 10 (hay nhất) - KNTT
- Soạn văn 10 (ngắn nhất) - KNTT
- Soạn văn 10 (siêu ngắn) - KNTT
- Giải sgk Toán 10 - KNTT
- Giải sgk Vật lí 10 - KNTT
- Giải sgk Hóa học 10 - KNTT
- Giải sgk Sinh học 10 - KNTT
- Giải sgk Địa lí 10 - KNTT
- Giải sgk Lịch sử 10 - KNTT
- Giải sgk Kinh tế và Pháp luật 10 - KNTT
- Giải sgk Tin học 10 - KNTT
- Giải sgk Công nghệ 10 - KNTT
- Giải sgk Hoạt động trải nghiệm 10 - KNTT
- Giải sgk Giáo dục quốc phòng 10 - KNTT
- Lớp 10 - Chân trời sáng tạo
- Soạn văn 10 (hay nhất) - CTST
- Soạn văn 10 (ngắn nhất) - CTST
- Soạn văn 10 (siêu ngắn) - CTST
- Giải Toán 10 - CTST
- Giải sgk Vật lí 10 - CTST
- Giải sgk Hóa học 10 - CTST
- Giải sgk Sinh học 10 - CTST
- Giải sgk Địa lí 10 - CTST
- Giải sgk Lịch sử 10 - CTST
- Giải sgk Kinh tế và Pháp luật 10 - CTST
- Giải sgk Hoạt động trải nghiệm 10 - CTST
- Lớp 10 - Cánh diều
- Soạn văn 10 (hay nhất) - Cánh diều
- Soạn văn 10 (ngắn nhất) - Cánh diều
- Soạn văn 10 (siêu ngắn) - Cánh diều
- Giải sgk Toán 10 - Cánh diều
- Giải sgk Vật lí 10 - Cánh diều
- Giải sgk Hóa học 10 - Cánh diều
- Giải sgk Sinh học 10 - Cánh diều
- Giải sgk Địa lí 10 - Cánh diều
- Giải sgk Lịch sử 10 - Cánh diều
- Giải sgk Kinh tế và Pháp luật 10 - Cánh diều
- Giải sgk Tin học 10 - Cánh diều
- Giải sgk Công nghệ 10 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 10 - Cánh diều
- Giải sgk Giáo dục quốc phòng 10 - Cánh diều


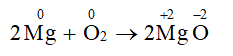
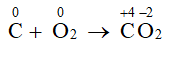











 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

