Giải Vở bài tập Hóa 9 Bài 17 trang 49, 50
Bài 17: Dãy hoạt động hóa học của kim loại
Bài 1. (Trang 49 VBT Hóa học 9 ) Dãy các kim loại nào sau đây được sắp xếp đúng theo chiều hoạt động hoá học tăng dần ?
a) K, Mg, Cu, Al, Zn, Fe ;
b) Fe, Cu, K, Mg, Al, Zn ;
c) Cu, Fe, Zn, Al, Mg, K ;
d) Zn, K, Mg, Cu, Al, Fe ;
e) Mg, K, Cu, Al, Fe.
Lời giải:
Dãy các kim loại được sắp xếp theo đúng chiều hoạt động hóa học tăng dần là:
Cu, Fe, Zn, Al, Mg, K
Bài 2. (Trang 49 VBT Hóa học 9 ) Dung dịch ZnSO4 có lẫn tạp chất là CuSO4. Dùng kim loại nào sau đây để làm sạch dung dịch ZnSO4 ? Hãy giải thích và viết phương trình hoá học.
a) Fe; b) Zn; c) Cu; d) Mg.
Lời giải:
Trong các kim loại Fe, Zn, Cu, Mg, kim loại dùng làm sạch dung dịch ZnSO4 có lẫn tạp chất CuSO4 là: Zn
Giải thích: kim loại kẽm đẩy Cu ra khỏi dung dịch, sau phản ứng lọc bỏ kim loại Cu thu được ZnSO4 tinh khiết.
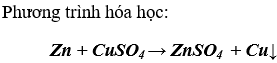
Bài 3. (Trang 49 VBT Hóa học 9 ) Viết các phương trình hoá học :
a) Điều chế CuSO4 từ Cu.
b) Điều chế MgCl2 từ mỗi chất sau : Mg, MgSO4, MgO, MgCO3.
Lời giải:
Phương trình hóa học:
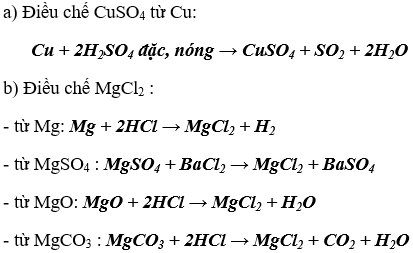
Bài 4. (Trang 49 VBT Hóa học 9 ) Hãy cho biết hiện tượng xảy ra khi cho
a) kẽm vào dung dịch đồng clorua.
b) đồng vào dung dịch bạc nitrat.
c) kẽm vào dung dịch magie clorua.
d) nhôm vào dung dịch đồng clorua.
Viết các phương trình hoá học, nếu có.
Lời giải:
Hiện tượng xảy ra khi cho:
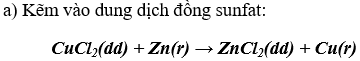
Hiện tượng: Chất rắn màu đỏ bám vào kẽm, dung dịch màu xanh nhạt dần
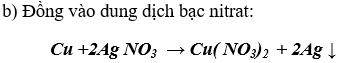
Hiện tượng: Chất rắn màu trắng bám vào đồng, màu xanh lam xuất hiện trong dung dịch
c) Kẽm vào dung dịch magie clorua:
Không có hiện tượng xảy ra và không có phản ứng.
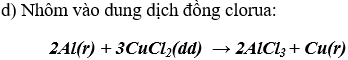
Hiện tượng: Có chất rắn màu đỏ bám vào nhôm, màu xanh của dung dịch nhạt dần.
Bài 5. (Trang 50 VBT Hóa học 9 ) Cho 10,5 gam hỗn hợp 2 kim loại Cu, Zn vào dung dịch H2SO4 loãng dư, người ta thu được 2,24 lít khí (đktc).
a) Viết phương trình hoá học.
b) Tính khối lượng chất rắn còn lại sau phản ứng.
Lời giải:
Số mol khí H2 thoát ra 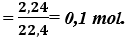
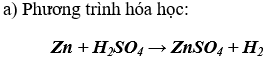
b) Theo phương trình: số mol Zn phản ứng = 0,1 mol , hay 6,5 gam
Khối lượng chất rắn (Cu) còn lại sau phản ứng = 10,5 - 0,1 . 65 = 4 gam.
Xem thêm các bài Giải bài tập Vở bài tập Hóa học 9 hay khác:
Học theo Sách giáo khoa
Bài tập bổ sung
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Giải vở bài tập Hóa học 9 hay, chi tiết của chúng tôi được biên soạn bám sát nội dung sách Vở bài tập Hóa học lớp 9.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 9 Global Success
- Giải sgk Tiếng Anh 9 Smart World
- Giải sgk Tiếng Anh 9 Friends plus
- Lớp 9 Kết nối tri thức
- Soạn văn 9 (hay nhất) - KNTT
- Soạn văn 9 (ngắn nhất) - KNTT
- Giải sgk Toán 9 - KNTT
- Giải sgk Khoa học tự nhiên 9 - KNTT
- Giải sgk Lịch Sử 9 - KNTT
- Giải sgk Địa Lí 9 - KNTT
- Giải sgk Giáo dục công dân 9 - KNTT
- Giải sgk Tin học 9 - KNTT
- Giải sgk Công nghệ 9 - KNTT
- Giải sgk Hoạt động trải nghiệm 9 - KNTT
- Giải sgk Âm nhạc 9 - KNTT
- Giải sgk Mĩ thuật 9 - KNTT
- Lớp 9 Chân trời sáng tạo
- Soạn văn 9 (hay nhất) - CTST
- Soạn văn 9 (ngắn nhất) - CTST
- Giải sgk Toán 9 - CTST
- Giải sgk Khoa học tự nhiên 9 - CTST
- Giải sgk Lịch Sử 9 - CTST
- Giải sgk Địa Lí 9 - CTST
- Giải sgk Giáo dục công dân 9 - CTST
- Giải sgk Tin học 9 - CTST
- Giải sgk Công nghệ 9 - CTST
- Giải sgk Hoạt động trải nghiệm 9 - CTST
- Giải sgk Âm nhạc 9 - CTST
- Giải sgk Mĩ thuật 9 - CTST
- Lớp 9 Cánh diều
- Soạn văn 9 Cánh diều (hay nhất)
- Soạn văn 9 Cánh diều (ngắn nhất)
- Giải sgk Toán 9 - Cánh diều
- Giải sgk Khoa học tự nhiên 9 - Cánh diều
- Giải sgk Lịch Sử 9 - Cánh diều
- Giải sgk Địa Lí 9 - Cánh diều
- Giải sgk Giáo dục công dân 9 - Cánh diều
- Giải sgk Tin học 9 - Cánh diều
- Giải sgk Công nghệ 9 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 9 - Cánh diều
- Giải sgk Âm nhạc 9 - Cánh diều
- Giải sgk Mĩ thuật 9 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

