Tính chất của Ancol (tính chất hóa học, tính chất vật lí, danh pháp, điều chế, ứng dụng)
Bài viết Tính chất của Ancol gồm tính chất hóa học, tính chất vật lí, danh pháp, điều chế, ứng dụng hay, chi tiết giúp bạn nắm vứng kiến thức trọng tâm về Ancol.
Tính chất của Ancol (tính chất hóa học, tính chất vật lí, danh pháp, điều chế, ứng dụng)
Thi online Hóa 11 KNTTThi online Hóa 11 CDThi online Hóa 11 CTST
Bài giảng: Bài 40 : Ancol - Cô Nguyễn Thị Nhàn (Giáo viên VietJack)
I. Định nghĩa, phân loại, đồng phân và danh pháp
1. Định nghĩa
Ancol là những hợp chất hữu cơ mà phân tử có nhóm hidroxyl (OH) liên kết trực tiếp với nguyên tử cacbon no.
Công thức tổng quát của ancol: R(OH)n (n ≥ 1), với R là gốc hydrocarbon.
- Công thức của ancol no mạch thẳng, đơn chức: CnH2n+1OH hay CnH2n+2O (với n ≥ 1).
2. Phân loại
- Gốc R có thể là mạch hở no hay chưa no hoặc mạch vòng.
Ví dụ: CH3-OH; CH2=CH-CH2-OH; C6H5-CH2-OH.
- Nhóm OH- có thể dính vào cacbon bậc 1, bậc 2, bậc 3 tạo thành ancol tương ứng bậc 1, bậc 2, bậc 3.
Lưu ý: Bậc của ancol bằng bậc của nguyên tử cacbon liên kết với nhóm OH.
Ví dụ:
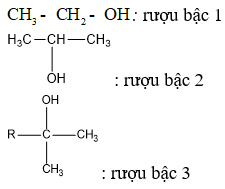
Bảng phân loại ancol
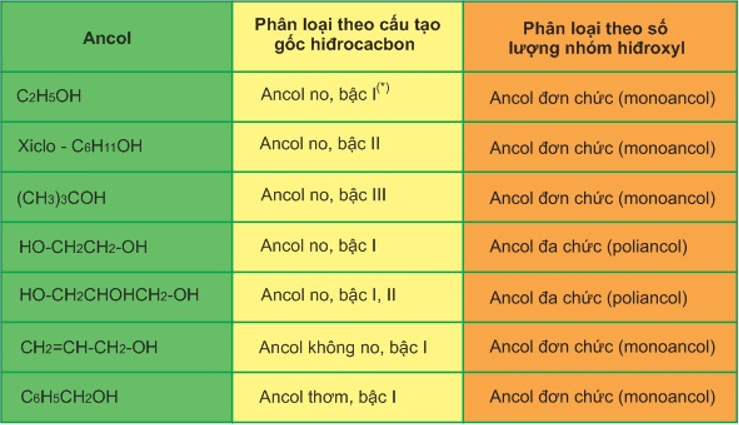
- Ancol không bền khi:
+ Nhiều nhóm –OH cùng đính vào một nguyên tử cacbon.
+ Nhóm –OH đính vào nguyên tử cacbon có nối đôi.
Ví dụ:
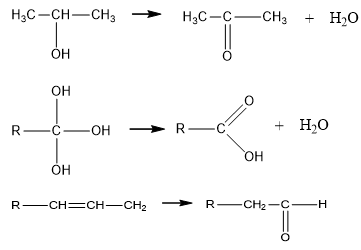
3. Đồng phân và danh pháp
a. Đồng phân
- Mạch cacbon khác nhau.
- Vị trí của các nhóm –OH khác nhau.
- Ngoài ra ancol đơn chức có đồng phân là ete: R-O-R’.
Ví dụ: Viết đồng phân của C3H8O.
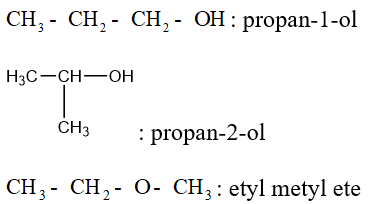
b. Danh pháp
- Tên thông thường: Tên ancol = tên gốc hydrocarbon no tương ứng + ic.
Ví dụ:
CH3-CH2-OH: ethyl alcohol.
CH3-OH: methyl alcohol.
- Tên thay thế: Tên ancol = tên gốc hydrocarbon no tương ứng + ol.
Ví dụ:
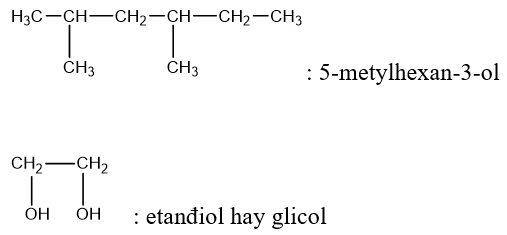
II. Tính chất vật lý
- Các ancol có nhiệt độ sôi cao hơn các hiđcacbon có cùng phân tử khối hoặc đồng phân ete của nó là do giữa các phân tử ancol có liên kết hiđro → Ảnh hưởng đến độ tan.
- Từ C1 đến C12 ancol ở thể lỏng (khối lượng riêng d < 1), từ C13 trở lên ở thể rắn.
- C1 đến C3 tan vô hạn trong nước vì có liên kiết H với nước.
- Độ rượu = (Vancol nguyên chất/Vdd ancol).100
- Các poli như ethylene glycol, glycerol thường sánh, nặng hơn nước và có vị ngọt.
III. Tính chất hóa học
1. Phản ứng thế nguyên tử hiđro của nhóm OH ancol (phản ứng đặc trưng của Ancol)
- Tính chất chung của ancol:
2ROH + Na → 2RONa + H2↑
- Tính chất đặc trưng của glycerol:
2C3H5(OH)3 + Cu(OH)2 → [C3H5(OH)2O]2Cu + H2O
(ĐK: muốn tác dụng với Cu(OH)2 phải có 2 nhóm -OH trở lên liền kề nhau)
→ Phản ứng này dùng để phân biệt ancol đơn chức với ancol đa chức có 2 nhóm OH cạnh nhau trong phân tử.
2. Phản ứng thế nhóm OH
- Phản ứng với axit vô cơ:
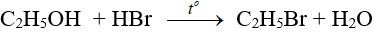
- Phản ứng tạo dien: dùng sản xuất cao su buna.
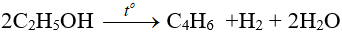
(ĐK: phải có xúc tác là Al2O3 + MgO hoặc ZnO/500ºC)
3. Phản ứng tách nước (phản ứng đêhidrat hoá)
Chú ý:
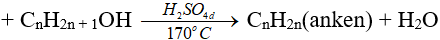
(ĐK n ≥ 2, theo quy tắc Zai-xép)
(ancol bậc càng cao thì càng dễ khử nước tạo alkene)
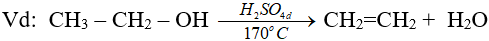
(phải là rượu no, đơn chức)
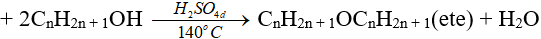
(ancol bậc càng thấp thì càng dễ khử nước tạo ete)
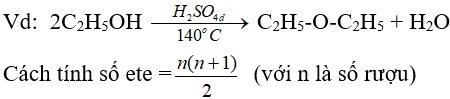
4. Phản ứng oxi hoá
- Phản ứng oxi hoá hoàn toàn:
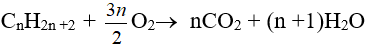
- Phản ứng oxi hoá không hoàn toàn:
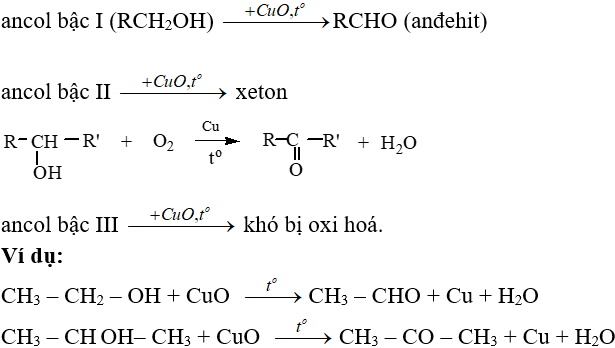
IV. Ứng dụng và điều chế
1. Ứng dụng
2. Điều chế
a. Phương pháp tổng hợp
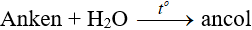
Ví dụ: Điều chế ethanol từ etilen CH2=CH2 + H2O → CH3CH2OH
b. Phương pháp sinh hoá: từ tinh bột, đường, ...
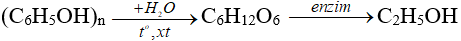
c. Điều chế methanol trong công nghiệp
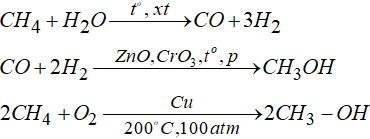
* Giới thiệu một số rượu
a. methyl alcohol (CH3OH)
- Là chất lỏng, không màu, nhẹ hơn nước, tan vô hạn trong nước, có mùi đặc trưng, nhiệt độ sôi 65oC.
- Rất độc: nếu uống phải dễ mù mắt, uống nhiều có thể gây tử vong.
- Dùng để điều chế formic aldehyde, tổng hợp chất dẻo, làm dung môi.
- Điều chế:
+ Tổng hợp trực tiếp:
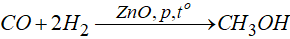
+ Bằng cách trưng gỗ.
b. ethylic alcohol (C2H5OH)
- Là chất lỏng, nhẹ hơn nước, tan vô hạn trong nước, có mùi thơm, nhiệt độ sôi 78oC.
- Có ứng dụng rất lớn trong thực tế: để chế tạo cao su và một số chất tổng hợp khác như ester, acetic acid, ete, … Để làm dung môi hòa tan vecni, dược phẩm, nước hoa.
c. Rượu butylic (C4H9OH)
- Có 4 đồng phân. Là những chất lỏng, ít tan trong nước hơn 3 chất đầu dãy đồng đẳng. Có mùi đặc trưng.
d. Rượu allylic (CH2=CH-CH2OH)
- Là chất lỏng không màu, mùi xốc, nhiệt độ sôi 97oC.
- Được dùng để sản xuất chất dẻo.
- Khi oxi hóa ở vị trí nối đôi tạo thành glycerol.
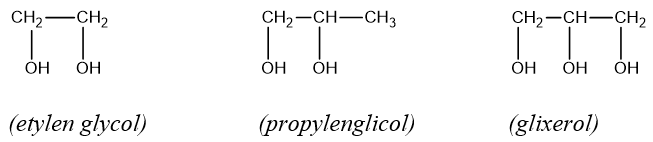
e. Một số rượu đa chức
Thi online Hóa 11 KNTTThi online Hóa 11 CDThi online Hóa 11 CTST
Xem thêm các phần Lý thuyết Hóa học lớp 11 ôn thi Tốt nghiệp THPT hay khác:
- Lý thuyết Dẫn xuất halogen của hydrocarbon?/b>
- Lý thuyết Phenol
- Lý thuyết Luyện tập Dẫn xuất halogen, ancol, phenol
- Dạng 1: Bài tập lý thuyết về dẫn xuất halogen, ancol, phenol
- Dạng 2: Cách viết đồng phân, gọi tên dẫn xuất halogen
- Dạng 3: Cách viết đồng phân, gọi tên Ancol, Phenol
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 11 Global Success
- Giải sgk Tiếng Anh 11 Smart World
- Giải sgk Tiếng Anh 11 Friends Global
- Lớp 11 - Kết nối tri thức
- Soạn văn 11 (hay nhất) - KNTT
- Soạn văn 11 (ngắn nhất) - KNTT
- Giải sgk Toán 11 - KNTT
- Giải sgk Vật Lí 11 - KNTT
- Giải sgk Hóa học 11 - KNTT
- Giải sgk Sinh học 11 - KNTT
- Giải sgk Lịch Sử 11 - KNTT
- Giải sgk Địa Lí 11 - KNTT
- Giải sgk Giáo dục KTPL 11 - KNTT
- Giải sgk Tin học 11 - KNTT
- Giải sgk Công nghệ 11 - KNTT
- Giải sgk Hoạt động trải nghiệm 11 - KNTT
- Giải sgk Giáo dục quốc phòng 11 - KNTT
- Giải sgk Âm nhạc 11 - KNTT
- Lớp 11 - Chân trời sáng tạo
- Soạn văn 11 (hay nhất) - CTST
- Soạn văn 11 (ngắn nhất) - CTST
- Giải sgk Toán 11 - CTST
- Giải sgk Vật Lí 11 - CTST
- Giải sgk Hóa học 11 - CTST
- Giải sgk Sinh học 11 - CTST
- Giải sgk Lịch Sử 11 - CTST
- Giải sgk Địa Lí 11 - CTST
- Giải sgk Giáo dục KTPL 11 - CTST
- Giải sgk Hoạt động trải nghiệm 11 - CTST
- Giải sgk Âm nhạc 11 - CTST
- Lớp 11 - Cánh diều
- Soạn văn 11 Cánh diều (hay nhất)
- Soạn văn 11 Cánh diều (ngắn nhất)
- Giải sgk Toán 11 - Cánh diều
- Giải sgk Vật Lí 11 - Cánh diều
- Giải sgk Hóa học 11 - Cánh diều
- Giải sgk Sinh học 11 - Cánh diều
- Giải sgk Lịch Sử 11 - Cánh diều
- Giải sgk Địa Lí 11 - Cánh diều
- Giải sgk Giáo dục KTPL 11 - Cánh diều
- Giải sgk Tin học 11 - Cánh diều
- Giải sgk Công nghệ 11 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 11 - Cánh diều
- Giải sgk Giáo dục quốc phòng 11 - Cánh diều
- Giải sgk Âm nhạc 11 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

