Giải Khoa học tự nhiên 7 trang 44 Chân trời sáng tạo
Với lời giải KHTN 7 trang 44 trong Bài 6: Giới thiệu về liên kết hóa học Khoa học tự nhiên 7 Chân trời sáng tạo hay nhất, ngắn gọn sẽ giúp học sinh lớp 7 dễ dàng trả lời các câu hỏi & làm bài tập KHTN 7 trang 44.
Giải Khoa học tự nhiên 7 trang 44 Chân trời sáng tạo
Luyện tập trang 44 Khoa học tự nhiên 7: Kết quả thử nghiệm tính chất của 2 chất A và B được trình bày ở bảng bên. Em hãy cho biết chất nào là chất cộng hóa trị, chất nào là chất ion?
Tính chất |
Chất A |
Chất B |
Thể (25oC) |
Rắn |
Lỏng |
Nhiệt độ sôi (oC) |
1500 |
64,7 |
Nhiệt độ nóng chảy (oC) |
770 |
-97,6 |
Khả năng dẫn điện của dung dịch |
Có |
Không |
Trả lời:
Dựa vào kết quả được trình bày ở bảng trên ta thấy: Chất A có nhiệt độ sôi và nhiệt độ nóng chảy cao hơn rất nhiều so với chất B, chất A tồn tại ở thể rắn và dẫn điện được.
⇒ Chất A là chất ion, chất B là chất cộng hóa trị.
Vận dụng trang 44 Khoa học tự nhiên 7: Khi cơ thể bị mất nước do tiêu chảy, nôn mửa, …người ta thường cho bệnh nhân uống dung dịch oresol. Tìm hiểu qua sách báo và internet, hãy cho biết thành phần của oresol có các loại chất nào (chất ion, chất cộng hóa trị)?
Trong trường hợp không có oresol thì có thể thay thế bằng cách nào khác không? Giải thích.
Trả lời:
Thành phần chính của oresol:
- Sodium chloride (NaCl): Chất ion
- Sodium hydrogen carbonate (NaHCO3): Chất ion
- Potassium chloride (KCl): Chất ion
- Glucose: Chất cộng hóa trị
Oresol được sử dụng bằng cách pha trực tiếp với nước và uống. Công dụng chính là bổ sung nước và các chất điện giải cho cơ thể. Do các chất ion có trong thành phần của oresol khi tan trong các dịch cơ thể tạo ra các ion âm và dương. Các ion này vai trò quan trọng trong quá trình trao đổi chất. Chúng sẽ điều chỉnh và kiểm soát sự cân bằng của dịch cơ thể đồng thời thúc đẩy các quá trình khác trong cơ thể để hoạt động hiệu quả hơn.
Trong trường hợp không có oresol thì có thể thay thế bằng:
- Nước muối đường: Có thành phần tương tự như oresol. Pha theo tỷ lệ 1 thìa cà phê muối, 8 thìa đường và 1 lít nước.
- Nước cháo muối (1,2 lít nước, 1 thìa muối, 1 nắm gạo), đồng thời uống bổ sung nước dừa, nước cam, ăn thêm chuối để bổ sung thêm potassium.
- Nước dừa muối: 1 lít nước dừa, 1 thìa muối.
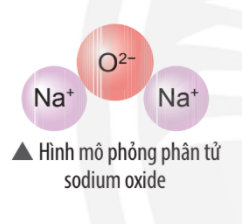
Bài 1 trang 44 Khoa học tự nhiên 7: Hãy vẽ sơ đồ và mô tả quá trình tạo thành liên kết trong phân tử sodium oxide (hình bên).
Trả lời:
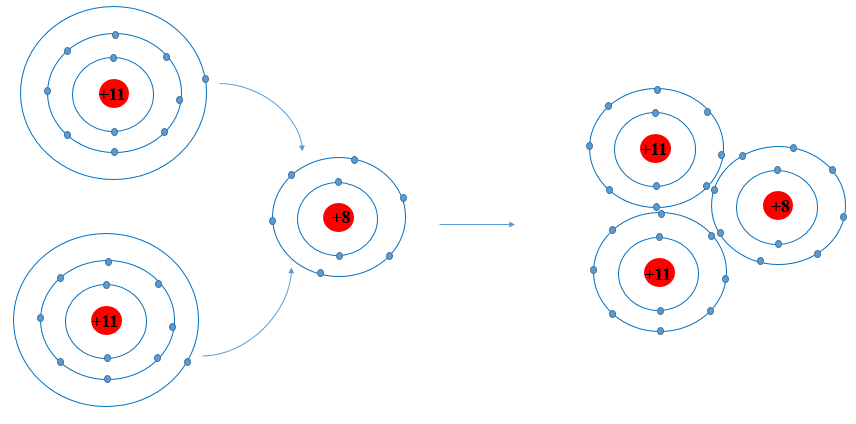
Sự tạo thành liên kết trong phân tử sodium oxide (Na2O)
Khi nguyên tử sodum (Na) kết hợp với nguyên tử oxygen (O), 2 nguyên tử sodium mỗi nguyên tử nhường 1 electron tạo thành ion dương, kí hiệu là Na+, đồng thời nguyên tử oxygen (O) nhận 2 electron từ nguyên tử Na tạo thành ion âm, kí hiệu O2-. Hai ion Na+ và O2- hút nhau tạo phân tử sodium oxide (Na2O).
Bài 2 trang 44 Khoa học tự nhiên 7: Cho biết vị trí trong bảng tuần hoàn, số electron lớp ngoài cùng của nguyên tử mỗi nguyên tố N, C, O và vẽ sơ đồ hình thành liên kết trong các phân tử ở hình sau:
Trả lời:
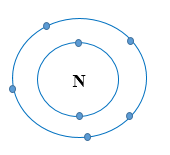
- Nguyên tử N thuộc ô số 7, chu kì 2, nhóm VA trong bảng tuần hoàn.
Nguyên tử N có 5 electron lớp ngoài cùng.
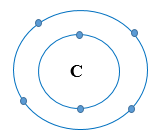
- Nguyên tử C thuộc ô số 6, chu kì 2, nhóm IVA trong bảng tuần hoàn.
Nguyên tử C có 4 electron lớp ngoài cùng.
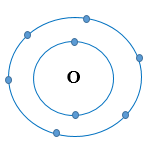
- Nguyên tử O thuộc số số 8, chu kì 2, nhóm VIA trong bảng tuần hoàn.
Nguyên tử O có 6 electron lớp ngoài cùng.
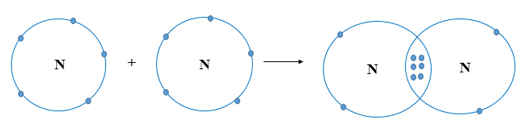
Sự tạo thành liên kết trong phân tử nitrogen:
+ Nguyên tử N có 7 electron, trong đó có 5 electron lớp ngoài cùng, cần thêm 3 electron để có lớp vỏ bền vững tương tự khí hiếm.
+ Khi hai nguyên tử N liên kết với nhau, mỗi nguyên tử góp chung 3 electron để tạo ra 3 cặp electron dùng chung.
+ Hạt nhân của hai nguyên tử N cùng hút các đôi electron dùng chung và liên kết với nhau tạo thành phân tử nitrogen.
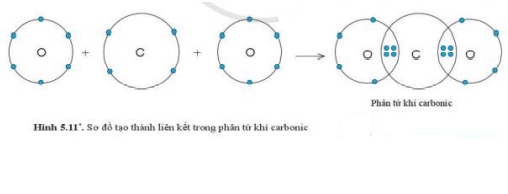
Sự tạo thành liên kết trong phân tử carbon dioxide
+ Nguyên tử C có 4 electron ở lớp ngoài cùng và cần thêm 4 electron để đạt được lớp vỏ bền vững tương tự khí hiếm Ne.
+ Trong phân tử khí carbon dioxide, nguyên tử C góp 4 electron, mỗi nguyên tử O góp 2 electron. Như vậy, giữa nguyên tử C và O có hai đôi electron dùng chung.
+ Hạt nhân nguyên tử C và O cùng hút đôi electron dùng chung, liên kết với nhau tạo thành phân tử khí carbon dioxide.
Bài 3 trang 44 Khoa học tự nhiên 7: Potassium chloride là hợp chất có nhiều ứng dụng trong đời sống. Trong nông nghiệp, nó được dùng làm phân bón. Trong công nghiệp, potassium chloride được dùng làm nguyên liệu để sản xuất potassium hydroxide và kim loại potassium. Trong y học, potassium chloride được dùng để bào chế thuốc điều trị bệnh thiếu kali trong máu. potassium chloride rất cần thiết cho cơ thể, trong các chức năng hoạt động của hệ tiêu hóa, tim, thận, cơ và cả hệ thần kinh.
Hợp chất potassium chloride có loại liên kết gì trong phân tử? Vẽ sơ đồ hình thành liên kết có trong phân tử này.
Trả lời:
Hợp chất potassium chloride (KCl) có liên kết ion trong phân tử.
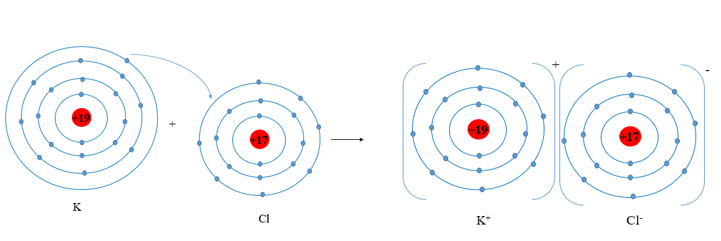
Sự hình thành liên kết trong phân tử potassium chloride
+ Nguyên tử K cho đi 1 electron ở lớp ngoài cùng trở thành ion mang điện tích dương, kí hiệu là K+.
+ Nguyên tử Cl nhận 1 electron từ nguyên tử K trở thành ion mang một điện tích âm, kí hiệu là Cl-.
Các ion K+ và Cl- hút nhau tạo thành liên kết trong phân tử potassium chloride.
Lời giải bài tập Khoa học tự nhiên 7 Bài 6: Giới thiệu về liên kết hóa học hay khác:
- Giải KHTN 7 trang 37
- Giải KHTN 7 trang 38
- Giải KHTN 7 trang 39
- Giải KHTN 7 trang 40
- Giải KHTN 7 trang 41
- Giải KHTN 7 trang 42
- Giải KHTN 7 trang 43
Xem thêm lời giải bài tập Khoa học tự nhiên 7 Chân trời sáng tạo hay, chi tiết khác:
Xem thêm các tài liệu học tốt lớp 7 hay khác:
- Giải sgk Khoa học tự nhiên 7 Chân trời sáng tạo
- Giải SBT Khoa học tự nhiên 7 Chân trời sáng tạo
- Giải lớp 7 Chân trời sáng tạo (các môn học)
- Giải lớp 7 Kết nối tri thức (các môn học)
- Giải lớp 7 Cánh diều (các môn học)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Giải bài tập Khoa học tự nhiên lớp 7 của chúng tôi được biên soạn bám sát nội dung sgk Khoa học tự nhiên lớp 7 bộ sách Chân trời sáng tạo (NXB Giáo dục).
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Soạn văn 7 (hay nhất) - CTST
- Soạn văn 7 (ngắn nhất) - CTST
- Giải sgk Toán 7 - CTST
- Giải Tiếng Anh 7 Global Success
- Giải Tiếng Anh 7 Friends plus
- Giải sgk Tiếng Anh 7 Smart World
- Giải Tiếng Anh 7 Explore English
- Giải sgk Khoa học tự nhiên 7 - CTST
- Giải sgk Lịch Sử 7 - CTST
- Giải sgk Địa Lí 7 - CTST
- Giải sgk Giáo dục công dân 7 - CTST
- Giải sgk Công nghệ 7 - CTST
- Giải sgk Tin học 7 - CTST
- Giải sgk Hoạt động trải nghiệm 7 - CTST
- Giải sgk Âm nhạc 7 - CTST

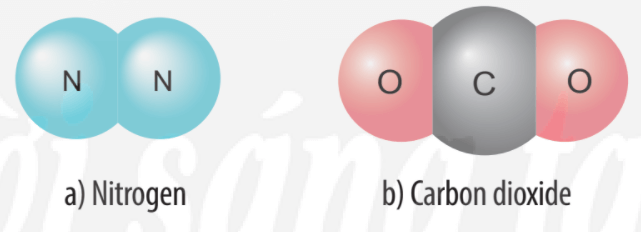





 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

