Lý thuyết Tách kim loại và việc sử dụng hợp kim (KHTN 9 Kết nối tri thức Bài 20)
Với tóm tắt lý thuyết Khoa học tự nhiên 9 Bài 20: Tách kim loại và việc sử dụng hợp kim sách Kết nối tri thức hay nhất, ngắn gọn sẽ giúp học sinh lớp 9 nắm vững kiến thức trọng tâm, ôn luyện để học tốt môn KHTN 9.
Lý thuyết Tách kim loại và việc sử dụng hợp kim (KHTN 9 Kết nối tri thức Bài 20)
(199k) Xem Khóa học KHTN 9 KNTT
I. Phương pháp tách kim loại
- Trong tự nhiên, kim loại chủ yếu tồn tại ở trong quặng dưới dạng hợp chất như oxide, muối,… Ví dụ: Aluminium oxide là thành phần chủ yếu trong quặng bauxite; iron (III) oxide là thành phần chủ yếu trong quặng hematite,… Một số kim loại quý như vàng có thể tồn tại dưới dạng đơn chất.
- Các bước cơ bản trong quy trình tách kim loại từ quặng:
+ Từ quặng, người ta làm giàu quặng bằng cách loại bỏ các tạp chất như đất, cát, đá,… thu được hợp chất chứa kim loại.
+ Sau đó, tuỳ thuộc vào mức độ hoạt động hoá học của kim loại, có thể lựa chọn phương pháp hoá học phù hợp để tách kim loại ra khỏi hợp chất.
- Một số phương pháp hoá học thường để tách kim loại:
+ Phương pháp điện phân nóng chảy được áp dụng để tách các kim loại hoạt động hoá học mạnh như Na, Ca, Mg, Al,…
+ Phương pháp nhiệt luyện thường được dùng để tách các kim loại hoạt động hoá học trung bình như Fe, Zn,…; có thể dùng các chất như C, CO, H2, Al,… tác dụng với oxide kim loại ở nhiệt độ cao, thu được kim loại.
+ Phương pháp thuỷ luyện để tách các kim loại hoạt động hoá học yếu như Ag, Au,….
II. Quá trình tách một số kim loại có nhiều ứng dụng
1. Tách nhôm ra khỏi aluminium oxide bằng phản ứng điện phân
- Nguyên liệu: quặng bauxite (thành phần chính là Al2O3).
- Quá trình điện phân nóng chảy: Trong công nghiệp, nhôm được sản xuất bằng phương pháp điện phân nóng chảy aluminium oxide nóng chảy, theo phản ứng sau:
2. Tách sắt ra khỏi iron (III) oxide
Ở nhiệt độ cao, sắt được tách ra khỏi iron (III) oxide bởi carbon monoxide:
3. Tách kẽm ra khỏi zinc sulfide
- Quặng chứa zinc sulfide (ZnS) được đốt trong không khí để chuyển zinc sulfide thành zinc oxide (ZnO):
- Tiếp theo, kẽm được tách ra khỏi zinc oxide bởi carbon:
Mở rộng:
Phương pháp thuỷ luyện: Các hợp chất hoặc hỗn hợp các kim loại hoạt động hoá học yếu như bạc,… được chuyển thành muối tan. Sau đó, dùng kim loại hoạt động hoá học mạnh hơn đẩy kim loại bạc ra khỏi muối, tách chúng ra khỏi dung dịch.
II. Hợp kim
1. Khái niệm hợp kim
Hợp kim là vật liệu kim loại có chứa ít nhất một kim loại cơ bản và một số kim loại hoặc phi kim khác.
Kim loại cơ bản là kim loại chiếm thành phần chính trong hợp kim.
Ví dụ: thép có kim loại cơ bản là sắt, đuy-ra (duralumin) có kim loại cơ bản là nhôm,…
2. Ưu điểm của hợp kim
Hợp kim thường có nhiều ưu điểm vượt trội so với kim loại nguyên chất về độ cứng, độ bền, khả năng chống ăn mòn và gỉ sét, phù hợp với nhiều ứng dụng nên được sử dụng phổ biến trong đời sống và trong công nghiệp.
3. Một số hợp kim phổ biến
- Gang và thép là hai hợp kim của sắt với carbon và một số nguyên tố khác (carbon chiếm hàm lượng từ 2% đến 5% trong gang và dưới 2% trong thép). Thép có nhiều ưu điểm hơn sắt về độ cứng, độ đàn hồi, khả năng chịu lực nên được sử dụng rộng rãi trong các công trình xây dựng, giao thông. Gang cứng và giòn hơn thép, thường được dùng để đúc các chi tiết máy, ống dẫn nước, nắp cống,…
- Inox là một loại thép đặc biệt, ngoài sắt và carbon còn các nguyên tố khác như chromium, nickel. Inox cứng và khó bị gỉ, được sử dụng làm đồ gia dụng, thiết bị y tế,…
- Đuy-ra (duralumin) là hợp kim của nhôm với đồng, manganese, magnesium,… Đuy-ra nhẹ tương đương nhôm nhưng bền và cứng hơn nhiều, được dùng làm vật liệu chế tạo máy bay, ô tô,…
III. Sản xuất gang, thép
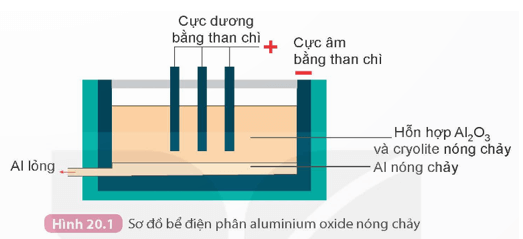
1. Sản xuất gang từ nguồn quặng chứa iron (III) oxide
- Nguyên liệu: quặng sắt (thường là quặng hematite với thành phần chính là Fe2O3), than cốc và chất tạo xỉ như CaCO3, SiO2,…
- Các giai đoạn chính:
+ Tạo thành khí CO:
+ Khí CO phản ứng với các oxide của sắt có trong quặng:
Sắt nóng chảy hoà tan một lượng nhỏ carbon cùng một số nguyên tố khác tạo thành gang lỏng.
+ Tạo xỉ, tách xỉ thu được gang:
Lưu ý:
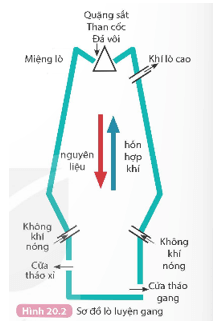
+ Xỉ nhẹ, nổi lên trên gang lỏng, được đưa ra ngoài cửa tháo xỉ.
+ Khí thải tạo thành trong lò cao được đưa ra ngoài qua cửa ở gần miệng lò.
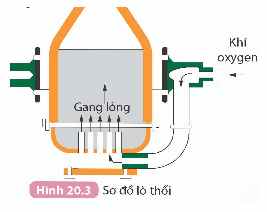
2. Sản xuất thép
- Nguyên liệu chính: Gang (hoặc thép phế liệu) và khí oxygen.
- Quá trình sản xuất thép: Làm giảm các tạp chất C, Si, Mn,… trong gang bằng cách chuyển chúng thành các oxide và loại bỏ chúng để thu được thép.
(199k) Xem Khóa học KHTN 9 KNTT
Xem thêm tóm tắt lý thuyết Khoa học tự nhiên lớp 9 Kết nối tri thức hay khác:
Xem thêm các tài liệu học tốt lớp 9 hay khác:
- Giải sgk Khoa học tự nhiên 9 Kết nối tri thức
- Giải SBT Khoa học tự nhiên 9 Kết nối tri thức
- Giải lớp 9 Kết nối tri thức (các môn học)
- Giải lớp 9 Chân trời sáng tạo (các môn học)
- Giải lớp 9 Cánh diều (các môn học)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Giải sgk KHTN 9 của chúng tôi được biên soạn bám sát nội dung sgk Khoa học tự nhiên 9 Kết nối tri thức (NXB Giáo dục).
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Soạn văn 9 (hay nhất) - KNTT
- Soạn văn 9 (ngắn nhất) - KNTT
- Giải sgk Toán 9 - KNTT
- Giải Tiếng Anh 9 Global Success
- Giải sgk Tiếng Anh 9 Smart World
- Giải sgk Tiếng Anh 9 Friends plus
- Giải sgk Khoa học tự nhiên 9 - KNTT
- Giải sgk Lịch Sử 9 - KNTT
- Giải sgk Địa Lí 9 - KNTT
- Giải sgk Giáo dục công dân 9 - KNTT
- Giải sgk Tin học 9 - KNTT
- Giải sgk Công nghệ 9 - KNTT
- Giải sgk Hoạt động trải nghiệm 9 - KNTT
- Giải sgk Âm nhạc 9 - KNTT
- Giải sgk Mĩ thuật 9 - KNTT

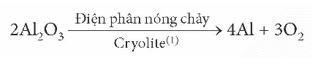





 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

