15 bài tập trắc nghiệm Phản ứng trao đổi ion trong dung dịch các chất điện li (có đáp án)
Với 15 bài tập & câu hỏi trắc nghiệm Phản ứng trao đổi ion trong dung dịch các chất điện li lớp 11 có đáp án và lời giải chi tiết đầy đủ các mức độ nhận biết, thông hiểu, vận dụng sẽ giúp học sinh ôn trắc nghiệm Hóa học 11.
15 bài tập trắc nghiệm Phản ứng trao đổi ion trong dung dịch các chất điện li (có đáp án)
Thi online Hóa 11 KNTTThi online Hóa 11 CDThi online Hóa 11 CTST
Câu 1: Chất nào sau đây không tạo kết tủa khi cho vào dung dịch AgNO3
A. KBr B. K3PO4
C. HCl D. H3PO4
Đáp án: D
Câu 2: Cho dung dịch chứa các ion sau : Na+ ,Ca2+ ,Mg2+ ,Ba2+ , H+ , NO3-. Muốn tách được nhiều cation ra khỏi dung dịch mà không đưa ion lạ vào dung dịch người ta dùng :
A. dung dịch K2CO3vừa đủ . B. dung dịch Na2SO4 vừa đủ.
C. dung dịch KOH vừa đủ. D. dung dịch Na2SO3 vừa đủ.
Đáp án: D
Câu 3: Trong các cặp chất sau đây, cặp chất nào cùng tồn tại trong dung dịch ?
A. AlCl3 và Na2CO3 B. HNO3 và NaHCO3
C. NaAlO2 và KOH D. NaCl và AgNO3
Đáp án: C
Câu 4: Phản ứng hóa học nào sau đây có phương trình ion thu gọn là H+ + OH- → H2O ?
A. HCl + NaOH → H2O + NaCl
B. NaOH + NaHCO3 → H2O + Na2CO3
C. H2SO4 + BaCl2 → 2HCl + BaSO4
D. H2SO4 +Ba(OH)2 → 2 H2O + BaSO4
Đáp án: A
Câu 5: Cho 4 dung dịch trong suốt, mỗi dung dịch chỉ chứa một loại cation và một loại anion trong các ion sau : Ba2+ ,Al3+ , Na+, Ag+ ,CO32 ,NO3- ,Cl- ,SO42- . Các dung dịch đó là :
A. BaCl2,Al2(SO4)3,Na2CO3,AgNO3.
B. Ba(NO3)2, Al2(SO4)3,Na2CO3, AgCl.
C. BaCl2, Al2(SO4)3,Na2CO3,AgNO3.
D. Ba(NO3)2, Al2(SO4)3,NaCl, Ag2CO3.
Đáp án: A
Câu 6: Cho 26,8 gam hỗn hợp X gồm CaCO3 và MgCO3 vào dung dịch HCl vừa đủ, thoát ra 6,72 lít khí (đktc) và dung dịch Y chứa m gam muối clorua. Giá trị của m là
A. 30,1. B. 31,7. C. 69,4. D. 64,0.
Đáp án: A
2H+ + CO32- → CO2 + H2O
nCl- = nH+ = 2nCO2 = 0,6 mol
m = mX – mCO32- + mCl- = 26,8 – 0,3.60 + 0,6.35,5 = 30,1 gam
Câu 7: Cho 47 gam K2O vào m gam dung dịch KOH 14%, thu được dung dịch KOH 21%. Giá trị của m là
A. 353. B. 659. C. 753. D. 800.
Đáp án: B
nK2O = 0,5 mol ⇒ nKOH tạo ra = 1 mol;
Dung dịch KOH 21% ⇒
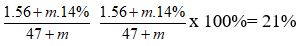
⇒ m = 659 gam
Câu 8: Để pha được 1 lít dung dịch chứa Na2SO4 0,04M, K2SO4 0,05 M và KNO3 0,08M cần lấy
A. 12,15 gam K2SO4 và 10,2 gam NaNO3.
B. 8,08 gam KNO3 và 12,78 gam Na2SO4.
C. 15,66 gam K2SO4 và 6,8 gam NaNO3.
D. 9,09 gam KNO3 và 5,68 gam Na2SO4.
Đáp án: C
Trong 1 lít dung dịch cần pha có:
nNa+ = 0,08 mol, nK+ = 0,18 mol, nSO42- = 0,09 mol, nNO3- = 0,08 mol
⇒ Ban đầu có 0,08 mol NaNO3 và 0,09 mol K2SO4
⇒ Cần phải thêm lấy 6,8 gam NaNO3 và 15,66 gam K2SO4
Câu 9: Hòa tan một hỗn hợp 7,2 gam gồm hai muối sunfat của kim loại A và B vào nước được dung dịch X. Thêm vào dung dịch X môt lượng vừa đủ BaCl2 đã kết tủa ion SO42-, thu được 11,65 gam BaSO4 và dung dịch Y. Tổng khối lượng hai muối clorua trong dung dịch Y là
A. 5,95 gam. B. 6,5 gam.
C. 7,0 gam. D. 8,2 gam.
Đáp án: A
M2(SO4)n + nBaCl2 → 2MCln + nBaSO4
⇒ nBaSO4 = 0,05 mol = nBaCl2
Theo bảo toàn khối lượng: mM2(SO4)n + mBaCl2 = mMCln + mBaSO4
⇒ mMCln = 5,95g
Câu 10: Cho 1 lít dung dịch gồm Na2CO3 0,1M và (NH4)2CO3 0,25M tác dụng với 43 gam hỗn hợp rắn Y gồm BaCl2 và CaCl2. Sau khi phản ứng kết thúc, thu được 39,7 gam kết tủa. Tỉ lệ khối lượng của BaCl2 trong Y là
A. 24,19%. B. 51,63%.
C. 75,81%. D. 48,37%
Đáp án: D
nBaCl2 = x mol; nCaCl2 = y mol
Y:
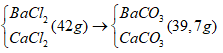
mgiảm = 42 - 39,7 = mCl- - mCO32-
⇒ 71(x + y) – 60(x + y) = 3,3 gam
x + y = 0,3 mol (1)
mkết tủa = 39,7 ⇒ 197x + 100y = 39,7 (2)
Từ (1)(2) ⇒ x = 0,1; y = 0,2
%m BaCl2 = [(208. 0,1)/43]. 100% = 48,37%
Câu 11: Cho dung dịch Fe2(SO4)3 phản ứng với dung dịch Na2CO3 thì sản phẩm tạo ra là:
A. Fe2(CO3)3 và Na2SO4
B. Na2SO4; CO2 và Fe(OH)3
C. Fe2O3; CO2; Na2SO4 và CO2
D. Fe(OH)3; CO2; Na2SO4; CO2
Đáp án: B
Fe2(SO4)3 + 3Na2CO3 → Fe2(CO3)3 + 3Na2SO4
Tuy nhiên Fe2(CO3)3 không bền bị thủy phân:
Fe2(CO3)3 + 3H2O → 2Fe(OH)3 + 3CO2
→ Fe2(SO4)3 + 3Na2CO3 + H2O → 2Fe(OH)3 + 3CO2 + 3Na2SO4
Câu 12: Phương trình ion rút gọn của phản ứng cho biết
A. Những ion nào tồn tại trong dung dịch.
B. Nồng độ những ion nào trong dung dịch lớn nhất.
C. Bản chất của phản ứng trong dung dịch các chất điện li.
D. Không tồn tại phân tử trong dung dịch các chất điện li.
Đáp án: C
Câu 13: Các ion nào sau không thể cùng tồn tại trong một dung dịch
A. Na+, Mg2+, NO3-, SO42-.
B. Ba2+, Al3+, Cl-, HSO4-.
C. Cu2+, Fe3+, SO42-, Cl-.
D. K+, NH4+, OH-, PO43-.
Đáp án: B
Câu 14: Các ion có thể tồn tại trong cùng một dung dịch là:
A. Na+, NH4+, SO42-, Cl-.
B. Mg2+, Al3+, NO3-, CO32-.
C. Ag+, Mg2+, NO3-, Br-.
D. Fe2+, Ag+, NO3-, CH3COO-.
Đáp án: A
Câu 15: Dung dịch X có chứa 0,07 mol Na+, 0,02 mol SO42-, và x mol OH-. Dung dịch Y có chứa ClO4-, NO3- và y mol H+; tổng số mol ClO4-, NO3- là 0,04 mol. Trộn X và T được 100 ml dung dịch Z. Dung dịch Z có pH (bỏ qua sự điện li của H2O) là :
A. 1. B. 12.
C. 13. D. 2.
Đáp án: A
Áp dụng bảo toàn điện tích cho các dung dịch X và Y ta có:
1.nNa+ = 2.nSO42- + 1.nOH- ⇒ 0,07 = 0,02.2 + x ⇒ x = 0,03
1.nClO4- + 1.nNO3- = 1.nH+ ⇒ y = 0,04
Phương trình phản ứng:
H+ + OH- → H2O
⇒ nH+ dư = 0,01 ⇒ [H+] = 0,1 ⇒ pH = 1.
Thi online Hóa 11 KNTTThi online Hóa 11 CDThi online Hóa 11 CTST
Xem thêm Bài tập & Câu hỏi trắc nghiệm Hóa học 11 có đáp án khác:
- 16 bài tập trắc nghiệm Axit, bazơ và muối, Phản ứng trao đổi ion trong dung dịch các chất điện li (có đáp án)
- 5 bài tập trắc nghiệm Tính axit, bazơ (có đáp án)
- Đề kiểm tra 1 tiết Hóa học 11 Học kì 1 có đáp án (Bài số 1)
- 15 bài tập trắc nghiệm Nitơ (có đáp án)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 11 Global Success
- Giải sgk Tiếng Anh 11 Smart World
- Giải sgk Tiếng Anh 11 Friends Global
- Lớp 11 - Kết nối tri thức
- Soạn văn 11 (hay nhất) - KNTT
- Soạn văn 11 (ngắn nhất) - KNTT
- Giải sgk Toán 11 - KNTT
- Giải sgk Vật Lí 11 - KNTT
- Giải sgk Hóa học 11 - KNTT
- Giải sgk Sinh học 11 - KNTT
- Giải sgk Lịch Sử 11 - KNTT
- Giải sgk Địa Lí 11 - KNTT
- Giải sgk Giáo dục KTPL 11 - KNTT
- Giải sgk Tin học 11 - KNTT
- Giải sgk Công nghệ 11 - KNTT
- Giải sgk Hoạt động trải nghiệm 11 - KNTT
- Giải sgk Giáo dục quốc phòng 11 - KNTT
- Giải sgk Âm nhạc 11 - KNTT
- Lớp 11 - Chân trời sáng tạo
- Soạn văn 11 (hay nhất) - CTST
- Soạn văn 11 (ngắn nhất) - CTST
- Giải sgk Toán 11 - CTST
- Giải sgk Vật Lí 11 - CTST
- Giải sgk Hóa học 11 - CTST
- Giải sgk Sinh học 11 - CTST
- Giải sgk Lịch Sử 11 - CTST
- Giải sgk Địa Lí 11 - CTST
- Giải sgk Giáo dục KTPL 11 - CTST
- Giải sgk Hoạt động trải nghiệm 11 - CTST
- Giải sgk Âm nhạc 11 - CTST
- Lớp 11 - Cánh diều
- Soạn văn 11 Cánh diều (hay nhất)
- Soạn văn 11 Cánh diều (ngắn nhất)
- Giải sgk Toán 11 - Cánh diều
- Giải sgk Vật Lí 11 - Cánh diều
- Giải sgk Hóa học 11 - Cánh diều
- Giải sgk Sinh học 11 - Cánh diều
- Giải sgk Lịch Sử 11 - Cánh diều
- Giải sgk Địa Lí 11 - Cánh diều
- Giải sgk Giáo dục KTPL 11 - Cánh diều
- Giải sgk Tin học 11 - Cánh diều
- Giải sgk Công nghệ 11 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 11 - Cánh diều
- Giải sgk Giáo dục quốc phòng 11 - Cánh diều
- Giải sgk Âm nhạc 11 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

