Bài 24.9 trang 58 SBT Hóa học 10
Bài 24: Sơ lược về hợp chất có oxi của clo
Bài 24.9 trang 58 Sách bài tập Hóa học 10: Cho 17,4 gam MnO2 tác dụng hết với dung dịch HCl. Toàn bộ khí cu sinh ra được hấp thụ hết vào 145,8 gam dung dịch NaOH 20% ở nhiệt độ thường tạo ra dung dịch A. Hỏi dung dịch A có chứa những chất tan nào ? Tính nồng độ % của từng chất tan đó.
Lời giải:
MnO2 + HCl → MnCl2 + Cl2 + 2H2O
Cl2 + 2NaOH → NaCl + NaClO + H2O
nMnO2 = 0,2 mol; nNaOH = 0,729 mol
Theo phương trình (1) ta có: nCl2 = nMnO2 = 0,2 mol
Theo phương trình (2) ta có: 2nCl2 < nNaOH ⇒ NaOH dư
Dung dịch A gồm: nNaCl = nNaClO = nCl2 = 0,2 mol
nNaOH dư = 0,729 – 2.0,2 = 0,329 mol
mdd A = mCl2 + mdd NaOH = 0,2.71 + 145,8 = 160g
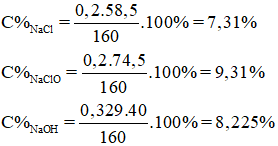
Các bài giải sách bài tập Hóa học 10 (SBT Hóa học 10) khác:
- Bài 24.1, 24.2, 24.3, 24.4 trang 56 Sách bài tập Hóa học 10: Nước Gia-ven là hỗn hợp ....
- Bài 24.5 trang 57 Sách bài tập Hóa học 10: Viết PTHH của các ....
- Bài 24.6 trang 57 Sách bài tập Hóa học 10: Viết PTHH của các ....
- Bài 24.7 trang 57 Sách bài tập Hóa học 10: Tại sao có thể ....
- Bài 24.8 trang 58 Sách bài tập Hóa học 10: Đưa một bình cầu ....
- Bài 24.9 trang 58 Sách bài tập Hóa học 10: Cho 17,4g MnO2 ....
- Bài 24.10 trang 58 Sách bài tập Hóa học 10: Trong phòng thí nghiệm ....
Để học tốt lớp 10 các môn học sách mới:
- Giải bài tập Lớp 10 Kết nối tri thức
- Giải bài tập Lớp 10 Chân trời sáng tạo
- Giải bài tập Lớp 10 Cánh diều
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 10 Global Success
- Giải Tiếng Anh 10 Friends Global
- Giải sgk Tiếng Anh 10 iLearn Smart World
- Giải sgk Tiếng Anh 10 Explore New Worlds
- Lớp 10 - Kết nối tri thức
- Soạn văn 10 (hay nhất) - KNTT
- Soạn văn 10 (ngắn nhất) - KNTT
- Soạn văn 10 (siêu ngắn) - KNTT
- Giải sgk Toán 10 - KNTT
- Giải sgk Vật lí 10 - KNTT
- Giải sgk Hóa học 10 - KNTT
- Giải sgk Sinh học 10 - KNTT
- Giải sgk Địa lí 10 - KNTT
- Giải sgk Lịch sử 10 - KNTT
- Giải sgk Kinh tế và Pháp luật 10 - KNTT
- Giải sgk Tin học 10 - KNTT
- Giải sgk Công nghệ 10 - KNTT
- Giải sgk Hoạt động trải nghiệm 10 - KNTT
- Giải sgk Giáo dục quốc phòng 10 - KNTT
- Lớp 10 - Chân trời sáng tạo
- Soạn văn 10 (hay nhất) - CTST
- Soạn văn 10 (ngắn nhất) - CTST
- Soạn văn 10 (siêu ngắn) - CTST
- Giải Toán 10 - CTST
- Giải sgk Vật lí 10 - CTST
- Giải sgk Hóa học 10 - CTST
- Giải sgk Sinh học 10 - CTST
- Giải sgk Địa lí 10 - CTST
- Giải sgk Lịch sử 10 - CTST
- Giải sgk Kinh tế và Pháp luật 10 - CTST
- Giải sgk Hoạt động trải nghiệm 10 - CTST
- Lớp 10 - Cánh diều
- Soạn văn 10 (hay nhất) - Cánh diều
- Soạn văn 10 (ngắn nhất) - Cánh diều
- Soạn văn 10 (siêu ngắn) - Cánh diều
- Giải sgk Toán 10 - Cánh diều
- Giải sgk Vật lí 10 - Cánh diều
- Giải sgk Hóa học 10 - Cánh diều
- Giải sgk Sinh học 10 - Cánh diều
- Giải sgk Địa lí 10 - Cánh diều
- Giải sgk Lịch sử 10 - Cánh diều
- Giải sgk Kinh tế và Pháp luật 10 - Cánh diều
- Giải sgk Tin học 10 - Cánh diều
- Giải sgk Công nghệ 10 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 10 - Cánh diều
- Giải sgk Giáo dục quốc phòng 10 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

