Giải Hóa học 10 trang 31 Chân trời sáng tạo
Với Giải Hóa học 10 trang 31 trong Bài 4: Cấu trúc lớp vỏ electron của nguyên tử Hóa học 10 Chân trời sáng tạo hay nhất, chi tiết sẽ giúp học sinh dễ dàng trả lời các câu hỏi & làm bài tập Hóa 10 trang 31.
Giải Hóa học 10 trang 31 Chân trời sáng tạo
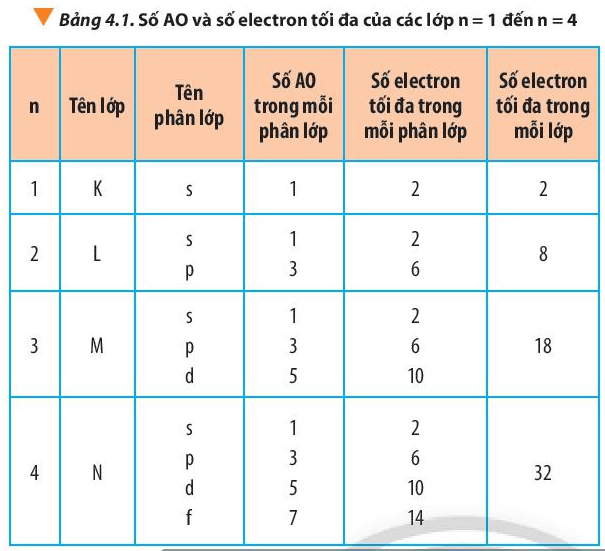
Câu hỏi 11 trang 31 Hóa học 10: Từ Bảng 4.1, hãy chỉ ra mối quan hệ giữa số thứ tự lớp và số electron tối đa trong mỗi lớp.
Lời giải:
Mối quan hệ: lớp n có tối đa 2n2 electron (với n ≤ 4).
Luyện tập trang 31 Hóa học 10: Nguyên tử nitrogen có 2 lớp electron trong đó có 2 phân lớp s và 1 phân lớp p. Các phân lớp s đều chứa số electron tố đa, còn phân lớp p chỉ chứa một nửa số electron tối đa. Nguyên tử nitrogen có bao nhiêu electron.
Lời giải:
Cách 1: Số electron tối đa trong phân lớp p là 6.
Phân lớp 2p chỉ chứa một nửa số electron tối đa ⇒ 2p3
Nguyên tử nitrogen có 2 lớp electron trong đó có 2 phân lớp s và 1 phân lớp p
⇒ Cấu hình electron của nguyên tử nitrogen là: 1s22s22p3
Nguyên tử nitrogen có 7 electron.
Cách 2:Số electron tối đa trong phân lớp p là 6.
Trong nguyên tử nitrogen, phân lớp 2p chỉ chứa một nửa số electron tối đa ⇒ phân lớp 2 p chứa 3 electron.
Nitrogen có 2 phân lớp s đều chứa electron tối đa ⇒ tổng số các electron trên các phân lớp s là 2 × 2 = 4.
Nguyên tử nitrogen có 3 + 4 = 7 electron.
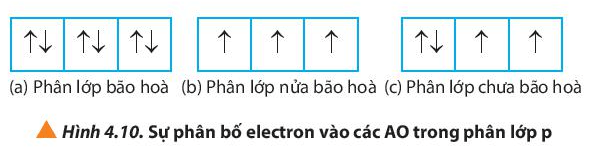
Câu hỏi 12 trang 31 Hóa học 10: Quan sát Hình 4.10, hãy nhận xét số lượng electron độc thân ở mỗi trường hợp.
Lời giải:
Trường hợp a) không có electron độc thân
Trường hợp b) có 3 electron độc thân
Trường hợp hợp c) có 2 electron độc thân
Nhận xét:
Phân lớp bão hòa chứa đủ số electron tối đa.
Phân lớp nửa bão hòa chứa một nửa số electron tối đa.
Phân lớp chưa bão hòa chưa đủ số electron tối đa.
Câu hỏi 13 trang 31 Hóa học 10: Hãy đề nghị cách phân bố electron vào các orbial để số electron độc thân là tối đa.
Lời giải:
Trong một orbital, electron đầu tiên được biểu diễn bằng mũi tên quay lên, electron thứ 2 được biểu diễn bằng mũi tên quay xuống. Electron được điền vào các orbital theo thứ tự từ trái sang phải.
Cách phân bố electron vào các orbial để số electron độc thân là tối đa:
Biểu diễn các electron bằng mũi tên đi lên vào lần lượt các orbital trước, sau đó mới quay lại biểu diễn các electron bằng mũi tên đi xuống vào các orbital.
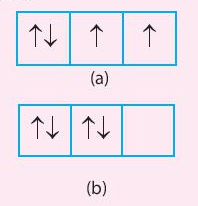
Luyện tập trang 31 Hóa học 10: Trong các trường hợp (a) và (b) dưới đây, trường hợp nào có sự phân bố electron vào các orbital tuân theo và không tuân theo quy tắc Hund
Lời giải:
Trường hợp (a) tuân theo quy tắc Hund vì số electron độc thân đã tối đa.
Trường hợp (b) không tuân theo quy tắc Hund vì số electron độc thân chưa tối đa.
Lời giải bài tập Hóa học 10 Bài 4: Cấu trúc lớp vỏ electron của nguyên tử hay khác:
Xem thêm lời giải bài tập Hóa học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Xem thêm các tài liệu học tốt lớp 10 hay khác:
- Giải sgk Hóa học 10 Chân trời sáng tạo
- Giải Chuyên đề Hóa học 10 Chân trời sáng tạo
- Giải SBT Hóa học 10 Chân trời sáng tạo
- Giải lớp 10 Chân trời sáng tạo (các môn học)
- Giải lớp 10 Kết nối tri thức (các môn học)
- Giải lớp 10 Cánh diều (các môn học)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Soạn văn 10 (hay nhất) - CTST
- Soạn văn 10 (ngắn nhất) - CTST
- Soạn văn 10 (siêu ngắn) - CTST
- Giải Toán 10 - CTST
- Giải Tiếng Anh 10 Global Success
- Giải Tiếng Anh 10 Friends Global
- Giải sgk Tiếng Anh 10 iLearn Smart World
- Giải sgk Tiếng Anh 10 Explore New Worlds
- Giải sgk Vật lí 10 - CTST
- Giải sgk Hóa học 10 - CTST
- Giải sgk Sinh học 10 - CTST
- Giải sgk Địa lí 10 - CTST
- Giải sgk Lịch sử 10 - CTST
- Giải sgk Kinh tế và Pháp luật 10 - CTST
- Giải sgk Hoạt động trải nghiệm 10 - CTST






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

