Giải Hóa học 10 trang 33 Kết nối tri thức
Với Giải Hóa học 10 trang 33 trong Bài 5: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học Hóa học 10 Kết nối tri thức hay nhất, chi tiết sẽ giúp học sinh dễ dàng trả lời các câu hỏi & làm bài tập Hóa học 10 trang 33.
Giải Hóa học 10 trang 33 Kết nối tri thức
Câu hỏi 3 trang 33 Hóa học 10: Ô nguyên tố trong bảng tuần hoàn cho ta biết những thông tin gì? Lấy ví dụ minh họa.
Lời giải:
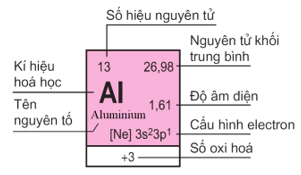
Tùy theo từng loại bảng tuần hoàn, ô nguyên tố có thể cho biết số hiệu nguyên tử, kí hiệu nguyên tố, tên nguyên tố, nguyên tử khối trung bình, …
Ví dụ: Ô nguyên tố số 13
Câu hỏi 4 trang 33 Hóa học 10: Dựa vào bảng tuần hoàn, hãy cho biết cấu hình electron và số electron hóa trị của các nguyên tố: C, Mg và Cl.
Lời giải:
Dựa vào bảng tuần hoàn, ta xác định được:
- Nguyên tố C có cấu hình electron là 1s2 2s2 2p2. C thuộc nhóm A, lớp ngoài cùng có 4 electron nên số electron hóa trị bằng 4.
- Nguyên tố Mg có cấu hình electron là 1s2 2s2 2p6 3s2. Mg thuộc nhóm A, lớp ngoài cùng có 2 electron nên số electron hóa trị bằng 2.
- Nguyên tố Cl có cấu hình electron là 1s2 2s2 2p6 3s2 3p5. Cl thuộc nhóm A, lớp ngoài cùng có 7 electron nên số electron hóa trị bằng 7.
Câu hỏi 5 trang 33 Hóa học 10: Dựa vào bảng tuần hoàn, hãy cho biết: thuộc loại nguyên tố nào sau đây.
a) s, p, d hay f?
b) phi kim, kim loại hay khí hiếm?
Lời giải:
a) Dựa vào bảng tuần, các nguyên tố lần lượt thuộc loại nguyên tố s, p, d, p.
Giải thích:
Mg thuộc nhóm IIA nên là nguyên tố s.
P thuộc nhóm VA, Ar thuộc nhóm VIIIA nên là nguyên tố p.
Fe thuộc nhóm VIIIB nên là nguyên tố d.
b) Dựa vào bảng tuần hoàn, xác định: nguyên tố Mg, Fe là kim loại; nguyên tố P là phi kim; nguyên tố Ar là khí hiếm.
Câu hỏi 6 trang 33 Hóa học 10: Nguyên tố phosphorus có Z = 15, có trong thành phần của một loại phân bón, diêm, pháo hoa; nguyên tố calcium có Z = 20, đóng vai trò rất quan trọng đối với cơ thể, đặc biệt là xương và răng. Xác định vị trí của hai nguyên tố trên trong bảng tuần hoàn và cho biết chúng thuộc loại nguyên tố s, p hay d; là kim loại, phi kim hay khí hiếm.
Lời giải:
- Nguyên tố phosphorus (P) có Z = 15 nên nguyên tử có 15 electron.
⇒ Cấu hình electron nguyên tử là 1s2 2s2 2p6 3s2 3p3.
⇒ Nguyên tử P có 3 lớp electron và electron lớp ngoài cùng là 5.
⇒ Nguyên tố phosphorus là phi kim, thuộc ô thứ 15, chu kì 3, nhóm VA, nguyên tố p.
- Nguyên tố calcium (Ca) có Z = 20 nên nguyên tử có 20 electron.
⇒ Cấu hình electron nguyên tử Ca là 1s2 2s2 2p6 3s2 3p6 4s2.
⇒ Nguyên tử có 4 lớp electron và electron lớp ngoài cùng là 2.
⇒ Nguyên tố calcium là kim loại, thuộc ô thứ 20, chu kì 4, nhóm IIA, nguyên tố s.
Câu hỏi 7 trang 33 Hóa học 10: Sulfur (lưu huỳnh) là chất rắn, xốp, màu vàng nhạt ở điều kiện thường. Sulfur và hợp chất của nó được sử dụng trong acquy, bột giặt, thuốc diệt nấm; do dễ cháy nên sulfur còn được dùng để sản xuất các loại diêm, thuốc súng, pháo hoa, … Trong bảng tuần hoàn, nguyên tố sulfur nằm ở chu kì 3, nhóm VIA.
a) Nguyên tử của nguyên tố sulfur có bao nhiêu electron thuộc lớp ngoài cùng?
b) Các electron lớp ngoài cùng thuộc những phân lớp nào?
c) Viết cấu hình electron nguyên tử của sulfur.
d) Sulfur là nguyên tố kim loại hay phi kim?
Lời giải:
a) Trong bảng tuần hoàn, nguyên tố sulfur nằm ở chu kì 3, nhóm VIA.
⇒ Nguyên tử của nguyên tố sulfur có 6 electron thuộc lớp ngoài cùng (lớp thứ 3).
b) Sự phân bố electron lớp ngoài cùng là 3s2 3p4.
⇒ Các electron lớp ngoài cùng thuộc phân lớp 3s và 3p.
c) Cấu hình electron nguyên tử của sulfur là 1s2 2s2 2p6 3s2 3p4.
d) Lớp ngoài cùng có 6 electron nên sulfur là phi kim.
Em có thể trang 33 Hóa học 10: Xác định được vị trí các nguyên tố hóa học trong bảng tuần hoàn và phân loại được thành phần nguyên tố s, p, d, f hay nguyên tố kim loại, phi kim, khí hiếm.
Lời giải:
- Để xác định được vị trí các nguyên tố hóa học trong bảng tuần hoàn cần biết:
+ Số electron của nguyên tử ⇒ xác định được ô nguyên tố.
+ Số lớp electron của nguyên tử ⇒ xác định được chu kì.
+ Số electron hóa trị ⇒ xác định được nhóm.
- Phân loại thành phần nguyên tố: các nguyên tố s, p, d, f là những nguyên tố mà nguyên tử có electron cuối cùng được điền vào phân lớp s, p, d, f tương ứng.
- Dựa vào đặc điểm về cấu hình electron lớp ngoài cùng để dự đoán tính chất hóa học cơ bản của nguyên tố:
+ Nguyên tố mà nguyên tử đủ 8 electron lớp ngoài cùng là khí hiếm (trừ He).
+ Nguyên tố mà nguyên tử có 1, 2, 3 electron lớp ngoài cùng thường là nguyên tố kim loại.
+ Nguyên tố mà nguyên tử có 5, 6, 7 electron lớp ngoài cùng thường là nguyên tố phi kim.
Lời giải bài tập Hóa học 10 Bài 5: Cấu tạo của bảng tuần hoàn các nguyên tố hóa học hay khác:
Xem thêm lời giải bài tập Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác:
Hóa 10 Bài 6: Xu hướng biến đổi một số tính chất của nguyên tử các nguyên tố trong một nhóm
Hóa 10 Bài 7: Xu hướng biến đổi thành phần và một số tính chất của hợp chất trong một chu kì
Hóa 10 Bài 8: Định luật tuần hoàn. Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
Xem thêm các tài liệu học tốt lớp 10 hay khác:
- Giải sgk Hóa học 10 Kết nối tri thức
- Giải Chuyên đề Hóa học 10 Kết nối tri thức
- Giải SBT Hóa học 10 Kết nối tri thức
- Giải lớp 10 Kết nối tri thức (các môn học)
- Giải lớp 10 Chân trời sáng tạo (các môn học)
- Giải lớp 10 Cánh diều (các môn học)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Soạn văn 10 (hay nhất) - KNTT
- Soạn văn 10 (ngắn nhất) - KNTT
- Soạn văn 10 (siêu ngắn) - KNTT
- Giải sgk Toán 10 - KNTT
- Giải Tiếng Anh 10 Global Success
- Giải Tiếng Anh 10 Friends Global
- Giải sgk Tiếng Anh 10 iLearn Smart World
- Giải sgk Tiếng Anh 10 Explore New Worlds
- Giải sgk Vật lí 10 - KNTT
- Giải sgk Hóa học 10 - KNTT
- Giải sgk Sinh học 10 - KNTT
- Giải sgk Địa lí 10 - KNTT
- Giải sgk Lịch sử 10 - KNTT
- Giải sgk Kinh tế và Pháp luật 10 - KNTT
- Giải sgk Tin học 10 - KNTT
- Giải sgk Công nghệ 10 - KNTT
- Giải sgk Hoạt động trải nghiệm 10 - KNTT
- Giải sgk Giáo dục quốc phòng 10 - KNTT






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

