Giải SBT Hóa học 10 trang 83 Chân trời sáng tạo
Với Giải SBT Hóa học 10 trang 83 trong Ôn tập chương 7 Hóa học lớp 10 Chân trời sáng tạo hay nhất, chi tiết sẽ giúp học sinh dễ dàng trả lời các câu hỏi & làm bài tập Hóa học 10 trang 83.
- Bài OT 7.1 trang 83 SBT Hóa học 10
- Bài OT 7.2 trang 83 SBT Hóa học 10
- Bài OT 7.3 trang 83 SBT Hóa học 10
- Bài OT 7.4 trang 83 SBT Hóa học 10
- Bài OT 7.5 trang 83 SBT Hóa học 10
- Bài OT 7.6 trang 83 SBT Hóa học 10
- Bài OT 7.7 trang 83 SBT Hóa học 10
- Bài OT 7.8 trang 83 SBT Hóa học 10
- Bài OT 7.9 trang 83 SBT Hóa học 10
Giải SBT Hóa học 10 trang 83 Chân trời sáng tạo
Bài OT 7.1 trang 83 SBT Hóa học 10: Cấu hình electron nào của nguyên tử halogen?
A.
B.
C.
D.
Lời giải:
Đáp án đúng là: C.
Nguyên tử halogen có 7 electron ở lớp ngoài cùng.
Vậy cấu hình 1s22s22p63s23p5 của halogen.
Bài OT 7.2 trang 83 SBT Hóa học 10: Dung dịch AgNO3 không tác dụng với dung dịch:
A. NaI
B. NaF
C. NaCl
D. NaBr
Lời giải:
Đáp án đúng là: B
NaF không tác dụng với AgNO3.
Bài OT 7.3 trang 83 SBT Hóa học 10: Phương trình hóa học nào viết sai?
A.
B.
C.
D.
Lời giải:
Đáp án đúng là: D
D sai vì 2Fe + 3Cl2 → 2FeCl3.
Bài OT 7.4 trang 83 SBT Hóa học 10: Nước chlorine có tính tẩy màu là do:
A. HCl có tính acid mạnh
B. Cl2 vừa có tính khử vừa có tính oxi hóa.
C. HClO có tính oxi hóa mạnh.
D. Cl2 có tính oxi hóa mạnh.
Lời giải:
Đáp án đúng là: C
Nước chlorine có tính tẩy màu là do HClO có tính oxi hóa mạnh.
Bài OT 7.5 trang 83 SBT Hóa học 10: Halogen không có tính khử là
A. fluorine
B. bromine
C. iodine
D. chlorine
Lời giải:
Đáp án đúng là: A.
Fluorine chỉ có tính oxi hóa.
Bài OT 7.6 trang 83 SBT Hóa học 10: Phương trình hóa học của 2 phản ứng như sau:
So sánh tính khử của các ion halide qua 2 phản ứng. Giải thích.
Lời giải:
Trong phản ứng oxi hoá - khử:
Chất khử mạnh + chất oxi hoá mạnh → Chất oxi hoá yếu + chất khử yếu
(Tính khử: Br- > Cl-)
(Tính khử: I- > Br-)
Vậy, tính khử của các ion được sắp xếp như sau: I- > Br- > Cl-.
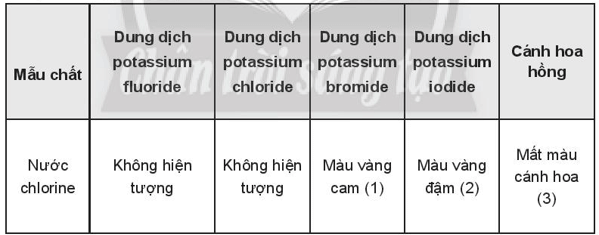
Bài OT 7.7 trang 83 SBT Hóa học 10: Ghi hiện tượng vào các ô trống trong bảng và viết phương trình hóa học của phản ứng (nếu có)
Lời giải:
Ghi hiện tượng vào các ô trống trong bảng và viết phương trình hoá họccủa phản ứng (nếu có)
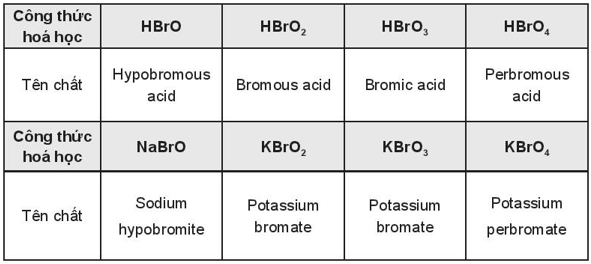
Bài OT 7.8 trang 83 SBT Hóa học 10: Chlorine tạo được các acid có oxygen trong thành phần phân tử. Tên và công thức của các acid có oxygen của chlorine theo bảng:
Acid có hậu tố -ous thì tạo muối có hậu tố -ite; acid có hậu tố -ic tạo muối có hậu tố -ate; acid có mức oxi hóa của nguyên tố trung tâm thấp nhất có tiền tố hypo-; acid có mức oxi hóa của nguyên tố trung tâm cao nhất có tiền tố per-. Áp dụng quy tắc trên, đọc tên các chất sau: HBrO; HBrO2; HBrO3; HBrO4; NaBrO; KBrO2; KBrO3 và KBrO4.
Lời giải:
Cách gọi tên theo bảng:
Bài OT 7.9 trang 83 SBT Hóa học 10: Nghiền mịn 10 g một mẫu đá vôi trong tự nhiên, hòa tan trong lượng dư dung dịch HCl thu được 4 g khí carbonic. Tính hàm lượng calcium carbonate trong mẫu đá vôi.
Lời giải:
Phương trình hoá học của phản ứng:
Từ hệ số cân bằng, ta có:
(mol)
Khối lượng CaCO3 trong mẫu đá vôi:
= 0,091 × 100 = 9,1 (g)
Hàm lượng CaCO3 trong mẫu đá vôi:
%CaCO3 =
Xem thêm lời giải sách bài tập Hóa học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
SBT Hóa 10 Bài 15: Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng
SBT Hóa 10 Bài 16: Các yếu tố ảnh hưởng đến tốc độ phản ứng hóa học
SBT Hóa 10 Bài 17: Tính chất vật lí và hóa học các đơn chất nhóm VIIA
SBT Hóa 10 Bài 18: Hydrogen halide và một số phản ứng của ion halide
Xem thêm các tài liệu học tốt lớp 10 hay khác:
- Giải sgk Hóa học 10 Chân trời sáng tạo
- Giải Chuyên đề Hóa học 10 Chân trời sáng tạo
- Giải SBT Hóa học 10 Chân trời sáng tạo
- Giải lớp 10 Chân trời sáng tạo (các môn học)
- Giải lớp 10 Kết nối tri thức (các môn học)
- Giải lớp 10 Cánh diều (các môn học)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Soạn văn 10 (hay nhất) - CTST
- Soạn văn 10 (ngắn nhất) - CTST
- Soạn văn 10 (siêu ngắn) - CTST
- Giải Toán 10 - CTST
- Giải Tiếng Anh 10 Global Success
- Giải Tiếng Anh 10 Friends Global
- Giải sgk Tiếng Anh 10 iLearn Smart World
- Giải sgk Tiếng Anh 10 Explore New Worlds
- Giải sgk Vật lí 10 - CTST
- Giải sgk Hóa học 10 - CTST
- Giải sgk Sinh học 10 - CTST
- Giải sgk Địa lí 10 - CTST
- Giải sgk Lịch sử 10 - CTST
- Giải sgk Kinh tế và Pháp luật 10 - CTST
- Giải sgk Hoạt động trải nghiệm 10 - CTST







 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

