Giải SBT Hóa học 10 trang 50 Kết nối tri thức
Với Giải SBT Hóa học 10 trang 50 trong Bài 18: Ôn tập chương 5 Sách bài tập Hóa 10 Kết nối tri thức hay nhất, chi tiết sẽ giúp học sinh dễ dàng trả lời các câu hỏi & làm bài tập Hóa học 10 trang 50.
Giải SBT Hóa học 10 trang 50 Kết nối tri thức
Bài 18.8 trang 50 SGK Hóa học 10: Cho phương trình nhiệt hóa học sau:
H2(g) + I2(g) → 2HI(g) ∆H = +11,3 kJ.
Phát biểu nào sau đây về sự trao đổi năng lượng của phản ứng trên là đúng?
A. Phản ứng giải phóng nhiệt lượng 11,3 kJ khi 2 mol HI được tạo thành.
B. Tổng nhiệt phá vỡ liên kết của chất phản ứng lớn hơn nhiệt tỏa ra khi tạo thành sản phẩm.
C. Năng lượng chứa trong H2 và I2 cao hơn trong HI.
D. Phản ứng xảy ra với tốc độ chậm.
Lời giải:
Đáp án đúng là: B
Phát biểu A sai: ∆H = +11,3 kJ > 0 ⇒ phản ứng thu nhiệt.
Phát biểu B đúng: phản ứng thu nhiệt nên tổng nhiệt cần cung cấp để phá vỡ liên kết lớn hơn nhiệt giải phóng khi tạo sản phẩm.
Phát biểu C sai: phân tử H2 và I2 có liên kết bền hơn HI, nghĩa là mức năng lượng thấp hơn.
Phát biểu D không nói về sự trao đổi năng lượng của phản ứng.
Bài 18.9 trang 50 SGK Hóa học 10: Làm các thí nghiệm tương tự nhau: Cho 0,05 mol mỗi kim loại Mg, Zn, Fe vào ba bình đựng 100 mL dung dịch CuSO4 0,5M.
Nhiệt độ tăng lên cao nhất ở mỗi bình lần lượt là ∆T1, ∆T2, ∆T3. Sự sắp xếp nào sau đây là đúng?
A. ∆T1 < ∆T2 < ∆T3
B. ∆T3 < ∆T1 < ∆T2
C. ∆T2 < ∆T3 < ∆T1
D. ∆T3 < ∆T2 < ∆T1
Lời giải:
Đáp án đúng là: D
Cả ba kim loại Mg, Zn, Fe đều tác dụng với CuSO4 với cùng tỉ lệ mol 1 : 1, kim loại càng mạnh thì càng tỏa nhiều nhiệt.
Do Mg > Zn > Fe nên nhiệt độ tăng cao nhất ở bình có Mg, rồi đến Zn, Fe.
Bài 18.10 trang 50 SGK Hóa học 10: Cho 0,5 g bột iron vào bình đựng 25 mL dung dịch CuSO4 0,2M ở 32oC. Khuấy đều dung dịch, quan sát nhiệt kế thấy nhiệt độ lên cao nhất là 39oC. Tính nhiệt của phản ứng. (Giả thiết nhiệt lượng của phản ứng tỏa ra được dung dịch hấp thụ hết, nhiệt dung của dung dịch loãng bằng nhiệt dung của nước (4,2 J/g.K)).
Lời giải:
Nhiệt lượng tỏa ra là:
Q = m.c. ∆T = 25.4,2.(39 – 32) = 735 (J)
Phản ứng xảy ra:
Fe(s) + CuSO4 (aq) → FeSO4(aq) + Cu(s)
Số mol Fe = > số mol CuSO4 =
0,005 mol CuSO4 phản ứng tỏa ra 735 J nhiệt lượng
→ 1 mol CuSO4 phản ứng tỏa ra nhiệt lượng là ∆H
⇒ ∆H = = 147000 J = 147 (kJ).
Bài 18.11 trang 50 SGK Hóa học 10: Để làm nóng khẩu phần ăn, người ta dùng phản ứng giữa CaO với H2O:
CaO(s) + H2O(l) → Ca(OH)2(aq) ∆H = -105 kJ
Cần cho bao nhiêu gam CaO vào 250g H2O để nâng nhiệt độ từ 20oC lên 80oC?
Lời giải:
Q = m.c. ∆T = 250.4,2.(80 – 20) = 63 000 J = 63 (kJ)
1 mol CaO tương đương 56 gam CaO phản ứng tỏa ra nhiệt lượng là 105 kJ
Số gam CaO cần để tỏa ra nhiệt lượng 63 kJ là
⇒ mCaO =
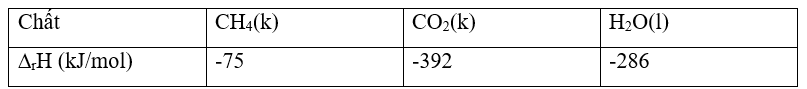
Bài 18.12 trang 50 SGK Hóa học 10: Tính nhiệt tỏa ra khi đốt cháy hoàn toàn 12 kg khí methane (CH4), biết nhiệt tạo thành của các chất như sau:
Lời giải:
CH4(k) + 2O2(k) → CO2(k) + 2H2O(k)
= (CO2) + 2.(H2O) - (CH4) – 2. (O2)
= (-392) + 2.(-286) – (-75) – 2.0 = -889 (kJ)
Đốt cháy hoàn toàn 1 mol ~ 16 gam khí methane (CH4) tỏa ra một lượng nhiệt là 889 (kJ).
⇒ Khi đốt cháy hoàn toàn 12 kg khí methane (CH4) tỏa ra
Lời giải SBT Hóa 10 Bài 18: Ôn tập chương 5 hay khác:
Xem thêm lời giải Sách bài tập Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác:
- SBT Hóa 10 Bài 19: Tốc độ phản ứng
- SBT Hóa 10 Bài 20: Ôn tập chương 6
- SBT Hóa 10 Bài 21: Nhóm halogen
- SBT Hóa 10 Bài 22: Hydrogen halide. Muối halide
- SBT Hóa 10 Bài 23: Ôn tập chương 7
Xem thêm các tài liệu học tốt lớp 10 hay khác:
- Giải sgk Hóa học 10 Kết nối tri thức
- Giải Chuyên đề Hóa học 10 Kết nối tri thức
- Giải SBT Hóa học 10 Kết nối tri thức
- Giải lớp 10 Kết nối tri thức (các môn học)
- Giải lớp 10 Chân trời sáng tạo (các môn học)
- Giải lớp 10 Cánh diều (các môn học)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Soạn văn 10 (hay nhất) - KNTT
- Soạn văn 10 (ngắn nhất) - KNTT
- Soạn văn 10 (siêu ngắn) - KNTT
- Giải sgk Toán 10 - KNTT
- Giải Tiếng Anh 10 Global Success
- Giải Tiếng Anh 10 Friends Global
- Giải sgk Tiếng Anh 10 iLearn Smart World
- Giải sgk Tiếng Anh 10 Explore New Worlds
- Giải sgk Vật lí 10 - KNTT
- Giải sgk Hóa học 10 - KNTT
- Giải sgk Sinh học 10 - KNTT
- Giải sgk Địa lí 10 - KNTT
- Giải sgk Lịch sử 10 - KNTT
- Giải sgk Kinh tế và Pháp luật 10 - KNTT
- Giải sgk Tin học 10 - KNTT
- Giải sgk Công nghệ 10 - KNTT
- Giải sgk Hoạt động trải nghiệm 10 - KNTT
- Giải sgk Giáo dục quốc phòng 10 - KNTT






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

