Đề kiểm tra 1 tiết Hóa học 10 Học kì 1 có đáp án (Bài kiểm tra số 2) (có đáp án)
Đề kiểm tra 1 tiết Hóa học 10 Học kì 1 có đáp án (Bài kiểm tra số 2)
Thi online Hóa 10 KNTTThi online Hóa 10 CDThi online Hóa 10 CTST
Câu 1: Cho các nguyên tố X, Y, Z, T với số hiệu nguyên tử lần lượt là 3, 4, 11, 19. Thứ tự giảm dần tính kim loại của các nguyên tố này là
A. X < Y < Z < T
B. T < X < Y < Z
C. Y < X < Z < T
D. Y < Z < T < X
Đáp án: C
Câu 2: Cho các dãy nguyên tố mà mỗi nguyên tố được biểu diễn bằng số hiệu nguyên tử tương ứng. Dãy nào sau đây gồm các nguyên tố thuộc cùng một chu kì trong bảng tuần hoàn?
A. 3, 7, 15
B. 17, 20, 21
C. 11, 13, 18
D. 18, 19, 20
Đáp án: C
Câu 3: Cho các dãy nguyên tố mà mỗi nguyên tố được biểu diễn bằng số hiệu nguyên tử tương ứng. Dãy nào sau đây gồm các nguyên tố thuộc cùng một nhóm A trong bảng tuần hoàn?
A. 12, 20, 30
B. 8, 16, 24
C. 5, 13, 31
D. 9, 17, 25
Đáp án: C
Câu 4: Nguyên tử của nguyên tố Z có 4 lớp electron, lớp ngoài cùng có 6 electron. Số hiệu nguyên tử của Z là
A. 24 B. 34 C. 36 D. 16
Đáp án: B
Cấu hình electron của Z là: 1s22s22p63s23p63d104s24p4
Số hiệu nguyên tử của Z là 34.
Câu 5: Nguyên tử của nguyên tố T có cấu hình electron như sau:
1s22s22p63s23p63d104s2.
Phát biểu nào sau đây không đúng?
A. T là nguyên tố kim loại.
B. T là nguyên tố thuộc nhóm IIA.
C. Ion T2+ có cấu hình electron là [Ar]3d10.
D. Hợp chất hidroxit của T có công thức hóa học T(OH)2.
Đáp án: B
Câu 6: Một nguyên tử X có 21 electron. Hóa trị cao nhất của X trong hợp chất với oxi là
A. I B. II C. III D. IV
Đáp án: C
Cấu hình electron nguyên tử của X là 1s22s22p63s23p63d14s2
X ở nhóm IIIB. Hóa trị cao nhất của X với oxi là III.
Câu 7: Cho các nguyên tố X, Y, Z, T với số hiệu nguyên tử lần lượt là 11, 14, 19, 20. Nguyên tố nào tạo với oxi hợp chất trong đó nó có hóa trị cao nhất?
A. X B. Y C. Z D. T
Đáp án: B
Y tạo được oxit dạng YO2. Hóa trị của Y là IV.
Câu 8: Phát biểu nào sau đây không đúng?
A. Nguyên tử có bán kính nhỏ nhất có Z = 1.
B. Kim loại yếu nhất trong nhóm IA có Z = 3.
C. Nguyên tố có độ âm điện lớn nhất có Z = 9.
D. Phi kim mạnh nhất trong nhóm VA có Z = 7.
Đáp án: A
Nguyên tử có bán kính nhỏ nhất có Z = 2(He)
Câu 9: Nguyên tố Z đứng ở ô thứ 17 của bảng tuần hoàn. Có các phát biểu sau:
(1) Z có độ âm điện lớn.
(2) Z là một phi kim mạnh.
(3) Z có thể tạo thành ion bền có dạng Z+.
(4) Hợp chất của X với oxi có công thức hóa học X2O5.
Trong các phát biểu trên, số phát biểu đúng là
A. 1 B. 2 C. 3 D. 4
Đáp án: B
Phát biểu 1, 2 đúng.
Câu 10: Một nguyên tử X có bán kính rất lớn. Phát biểu nào sau đây về X là đúng?
A. Độ âm điện của X rất lớn và X là phi kim.
B. Độ âm điện của X rất nhỏ và X là phi kim.
C. Độ âm điện của X rất lớn và X là kim loại.
D. Độ âm điện của X rất nhỏ và X là kim loại.
Đáp án: D
Câu 11: Nguyên tố Y thuộc chu kì 4, nhóm IA của bảng tuần hoàn. Phát biểu nào sau đây về Y là đúng?
A. Y có độ âm điện lớn nhất và bán kính nguyên tử lớn nhất so với các nguyên tố trong cùng chu kì.
B. Y có độ âm điện lớn nhất và bán kính nguyên tử nhỏ nhất so với các nguyên tố trong cùng chu kì.
C. Y có độ âm điện nhỏ nhất và bán kính nguyên tử lớn nhất so với các nguyên tố trong cùng chu kì.
D. Y có độ âm điện nhỏ nhất và bán kính nguyên tử nhỏ nhất so với các nguyên tố trong cùng chu kì.
Đáp án: C
Câu 12: Cho các phát biểu sau:
(1) Mỗi ô của bảng tuần hoàn chỉ chứa một nguyên tố hóa học.
(2) Các đồng vị của một nguyên tố hóa học được xếp vào cùng một ô.
(3) Các nguyên tố trong cùng một nhóm A có cùng số electron lớp ngoài cùng.
(4) Các nguyên tố được xếp trong cùng một chu kì có tính chất vật lí và hóa học tương tự.
Trong các phát biểu trên, số phát biểu đúng là
A. 1 B. 2 C. 3 D. 4
Đáp án: C
Các phát biểu 1, 2, 3 đúng.
Câu 13: Trong các phát biểu sau về quy luạt của bảng tuần hoàn, phát biểu nào không đúng?
A. Khi bán kính nguyên tử tăng dần thì độ âm điện giảm dần.
B. Trong một chu kì, khí hiếm có bán kính nguyên tử nhỏ nhất.
C. Trong một chu kì, độ âm điện của kim loại kiềm là nhỏ nhất.
D. Trong một nhóm A, khi số hiệu nguyên tử tăng thì độ âm điện tăng dần.
Đáp án: D
Câu 14: Cho biết vị trí của các nguyên tố X, Y, Z trong bảng tuần hoàn và hidroxit tương ứng của chúng trong bảng sau:
| Nguyên tố | Vị trí trong bảng tuần hoàn | Hidroxit tương ứng |
| X | 15 | X’ |
| Y | 16 | Y’ |
| Z | 33 | Z’ |
Thứ tự tăng dần tính axit của X’, Y’, Z’ là
A. X’ < Y’ < Z’
B. X’ < Z’ < Y’
C. Z’ < Y’ < X’
D. Z’ < X’ < Y’
Đáp án: D
Câu 15: Cho biết vị trí của các nguyên tố Q, R, T trong bảng tuần hoàn và hidroxit tương ứng của chúng trong bảng sau:
| Nguyên tố | Vị trí trong bảng tuần hoàn | Hidroxit tương ứng |
| Q | 12 | Q’ |
| R | 13 | R’ |
| T | 38 | T’ |
Thứ tự tăng dần tính bazơ của Q’, R’, T’ là
A. R’ < Q’ < T’
B. Q’ < T’ < R’
C. T’ < Q’ < R’
D. T’ < R’ < Q’
Đáp án: A
T là nguyên tố nhóm IIB.
Câu 16: Trong nguyên tử X, lớp electron có mức năng lượng cao nhất là M. Ở lớp M, phân lớp p có 4 electron. Số electron của nguyên tố X là
A. 6 B. 16 C. 18 D. 14
Đáp án: B
Câu 17: Nguyên tố Z thuôc chu kì 6, nhóm IA của bảng tuần hoàn. Phát biểu nào sau đây về Z là không đúng?
A. Trong số các nguyên tố bền, Z là kim loại mạnh nhất.
B. Ion Z+ có cấu hình của khí hiếm.
C. Nguyên tử Z có bán kính lớn và độ âm điện lớn.
D. Z tạo được hidroxit có công thức hóa học ROH.
Đáp án: C
Câu 18: Một nguyên tố A thuộc chu kì 3, nhóm IIIA của bảng tuần hoàn. Có những phát biểu sau đây về nguyên tố A:
(1) Nguyên tố này tạo được hợp chất khí có công thức hóa học AH3.
(2) Oxit tương ứng với hóa trị cao nhất của A có công thức hóa học A2O3.
(3) Hợp chất hidroxit của A có công thức hóa học A(OH)3.
(4) Hidroxit của A có tính bazơ mạnh.
Trong các phát biểu trên, số phát biểu đúng là
A. 1 B. 2 C. 3 D. 4
Đáp án: B
Các phát biểu 2, 3 đúng.
Câu 19: Phát biểu nào sau đây là sai?
A. Nguyên tử có Z = 11 có bán kính nhỏ hơn nguyên tử có Z = 19.
B. Nguyên tử có Z = 12 có bán kính lớn hơn nguyên tử có Z = 10.
C. Nguyên tử có Z = 11 có bán kính nhỏ hơn nguyên tử có Z = 13.
D. Các nguyên tố kim loại kiềm có bán kính nguyên tử lớn nhất so với các nguyên tố trong cùng một chu kì.
Đáp án:
Câu 20: Nguyên tố M thuộc chu kì II, nhóm VIIA của bảng tuần hoàn. Phát biểu nào sau đây về M đúng?
A. Nguyên tử M có bán kính nhỏ nhất trong chu kì II.
B. M là nguyên tố có độ âm điện lớn nhất trong bảng tuần hoàn.
C. Oxit ứng với hóa trị cao nhất của M có công thức hóa học M2O7.
D. Hidroxit của M có công thức hóa học HMO4 là một oxit mạnh.
Đáp án: B
Câu 21: Nguyên tử của nguyên tố A có 4 lớp electron và tạo được hợp chất khí với hidroxit có công thức hóa học HX. Số hiệu nguyên tử của A là
A. 19 B. 21 C. 35 D. 17
Đáp án: C
Câu 22: Nguyên tố Z thuộc nhóm A của bảng tuần hoàn. Oxit ứng với hóa trị cao nhất của Z có công thức hóa học ZO3. Số electron ở lớp ngoài cùng của A là
A. 8 B. 6 C. 3 D. 2
Đáp án: B
Câu 23: Nguyên tố X thuộc nhóm B của bảng tuần hoàn. Oxit ứng với hóa trị cao nhất của X có công thức hóa học X2O5.. Biết rằng nguyên tử của nguyên tố X có 4 lớp electron. Cấu hình electron nguyên tử của X là
A. [Ar]3d34s2
B. [Ar]3d54s2
C. [Ar]3d104s24p3
D. [Ar]3d104s24p5
Đáp án: A
X nằm ở nhóm VB của bảng tuần hoàn.
Câu 24: Nguyên tố Q tạo được với hidro hợp chất khi có công thức hóa học H2Q, trong đó Q chiếm 94,12% về khối lượng. Trong oxit tương ứng với hóa trị cao nhất của Q, phần tram khối lượng của oxi là
A. 33,3% B. 50,0% C. 42,9% D. 60,0%
Đáp án: D
Q là nguyên tố lưu huỳnh.
Oxit ứng với hóa trị cao nhất của S là SO3, %mO = 48.100%/80 = 60%
Câu 25: Nguyên tố R thuộc nhóm IIA của bảng tuần hoàn. Khi cho 8,70 gam hidroxit của R tác dụng với HCl dư thu được 14,25 gam muối. Phân tử khối của R là
A. 24 B. 40 C. 65 D. 27
Đáp án: A
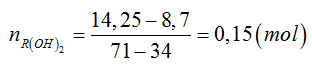
⇒ R + 34 = 58 ⇒ R = 24 (Mg)
Câu 26: Hòa tan 26,8 gam hỗn hợp hai muối cacbonat của hai kim loại (cùng thuộc nhóm IIA và ở hai chu kì lien tiếp của bảng tuần hoàn) tan trong dung dichh HCl vừa đủ. Sau phản ứng thu được 6,72 lít khí (đktc). Thành phần phần trăm khối lượng của muối cacbonat có phân tử khối nhỏ hơn là
A. 56,2% B. 62,69% C. 29,6% D. 25,3 %
Đáp án: B
nCO32- = nCO2 = 0,3 (mol) ⇒ M = 89,33
⇒ Hai muối là MgCO3 (a mol), CaCO3 (b mol)
Ta có: a + b = 0,3; 84a + 100b = 26,8 ⇒ a = 0,2; b = 0,1
⇒ %mMgCO3= 62,69%
Câu 27: Hỗn hợp X gồm hai kim loại A, B nằm kế tiếp nhau trong cùng một nhóm A của bảng tuần hoàn, MA < MB. Lấy 6,2 gam X hòa tan hoàn toàn vào nước thu được 2,24 lít khí hidro (đktc). Kim loại B là
A. K B. Rb C. Ba D. Sr
Đáp án: B
Đặt công thức chung của 2 kim loại là X, hóa trị n
X + nH2O → X(OH)n + n/2 H2
Ta có: aX = 6,2 và 0,5an = 0,1 ⇒ X/n = 62
Với n = 1: tính được X = 62. Hai kim loại A, B lần lượt là K và Rb
Với n = 2: tính được X = 31. Hai kim loại A, B lần lượt là Mg và Ca
Trường hợp này loại vì Mg không tan trong nước.
Câu 28: X và Y là hai nguyên tố thuộc cùng một nhóm ở hai chu kì liên tiếp, biết rằng X đứng trước Y trong bảng tuần hoàn. Tổng các hạt mang điện trong nguyên tử X và Y là 52. Số hiệu nguyên tử của X là
A. 22 B. 17 C. 9 D. 5
Đáp án: C
Tổng số hạt mang điện của X và Y = 52
⇒ 2pX + 2pY = 52 ⇒ pX + pY = 26
X,Y thuộc 2 chu kì liên tiếp ⇒ pY - pX = 8 ( TH pY - pX = 18 loại)
⇒ pX = 9 ⇒ ZX =9
Câu 29: Cho 0,99 gam hỗn hợp hai kim loại kiềm A và kali vào nước. Để trung hòa dung dịch thu được cần 500 ml dung dich HCl 0,1M. Thành phần phần tram khối lượng của A trong hỗn hợp trên là
A. 21,21% B. 14,14% C. 39,39% D. 69,69%
Đáp án: A
Gọi CTTB của hai kim loại là M
nMOH = nHCl = 0,05 mol
nM = 0,05 ⇒ M = 0,99 : 0,05 = 19,8 ⇒ A: Li (7 < 19,8); do K = 39 > 19,8
Gọi nLi = x mol; nK = y mol
7x + 39y = 0,99; x + y = 0,05
x = 0,03 ⇒ %mLi = (0,03.7/0,99). 100% = 21,21%
Câu 30: Hai nguyên tố X và Y nằm ở hai nhóm A kế tiếp và thuộc cùng một chu kì. Chúng có thể tạo được hợp chất có công thức X2Y, trong đó tổng số proton là 23. X có số hiệu nguyên tử là
A. 7 B. 8 C. 9 D. 11
Đáp án: B
X2Y có tổng số proton = 22 ⇒ 2pX + pY = 22
X, Y thuộc cùng chu kì và ở hai nhóm A kế tiếp ⇒ pX + 1 = pY
⇒ pX = 7; pY = 8
Thi online Hóa 10 KNTTThi online Hóa 10 CDThi online Hóa 10 CTST
Xem thêm Bài tập & Câu hỏi trắc nghiệm Hóa học 10 cực hay có đáp án khác:
- 15 bài tập trắc nghiệm Liên kết ion; Tinh thể ion (có đáp án)
- 15 bài tập trắc nghiệm Liên kết cộng hóa trị (có đáp án)
- 15 bài tập trắc nghiệm Tinh thể nguyên tử và tinh thể phân tử (có đáp án)
- 15 bài tập trắc nghiệm Hóa trị và số oxi hóa (có đáp án)
- 15 bài tập ôn tập Liên kết hóa học (có đáp án)
Để học tốt lớp 10 các môn học sách mới:
- Giải bài tập Lớp 10 Kết nối tri thức
- Giải bài tập Lớp 10 Chân trời sáng tạo
- Giải bài tập Lớp 10 Cánh diều
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 10 Global Success
- Giải Tiếng Anh 10 Friends Global
- Giải sgk Tiếng Anh 10 iLearn Smart World
- Giải sgk Tiếng Anh 10 Explore New Worlds
- Lớp 10 - Kết nối tri thức
- Soạn văn 10 (hay nhất) - KNTT
- Soạn văn 10 (ngắn nhất) - KNTT
- Soạn văn 10 (siêu ngắn) - KNTT
- Giải sgk Toán 10 - KNTT
- Giải sgk Vật lí 10 - KNTT
- Giải sgk Hóa học 10 - KNTT
- Giải sgk Sinh học 10 - KNTT
- Giải sgk Địa lí 10 - KNTT
- Giải sgk Lịch sử 10 - KNTT
- Giải sgk Kinh tế và Pháp luật 10 - KNTT
- Giải sgk Tin học 10 - KNTT
- Giải sgk Công nghệ 10 - KNTT
- Giải sgk Hoạt động trải nghiệm 10 - KNTT
- Giải sgk Giáo dục quốc phòng 10 - KNTT
- Lớp 10 - Chân trời sáng tạo
- Soạn văn 10 (hay nhất) - CTST
- Soạn văn 10 (ngắn nhất) - CTST
- Soạn văn 10 (siêu ngắn) - CTST
- Giải Toán 10 - CTST
- Giải sgk Vật lí 10 - CTST
- Giải sgk Hóa học 10 - CTST
- Giải sgk Sinh học 10 - CTST
- Giải sgk Địa lí 10 - CTST
- Giải sgk Lịch sử 10 - CTST
- Giải sgk Kinh tế và Pháp luật 10 - CTST
- Giải sgk Hoạt động trải nghiệm 10 - CTST
- Lớp 10 - Cánh diều
- Soạn văn 10 (hay nhất) - Cánh diều
- Soạn văn 10 (ngắn nhất) - Cánh diều
- Soạn văn 10 (siêu ngắn) - Cánh diều
- Giải sgk Toán 10 - Cánh diều
- Giải sgk Vật lí 10 - Cánh diều
- Giải sgk Hóa học 10 - Cánh diều
- Giải sgk Sinh học 10 - Cánh diều
- Giải sgk Địa lí 10 - Cánh diều
- Giải sgk Lịch sử 10 - Cánh diều
- Giải sgk Kinh tế và Pháp luật 10 - Cánh diều
- Giải sgk Tin học 10 - Cánh diều
- Giải sgk Công nghệ 10 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 10 - Cánh diều
- Giải sgk Giáo dục quốc phòng 10 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

