Lý thuyết Sulfuric acid và muối sulfate (Hóa 11 Kết nối tri thức Bài 8)
Với tóm tắt lý thuyết Hóa 11 Bài 8: Sulfuric acid và muối sulfate sách Kết nối tri thức hay nhất, chi tiết sẽ giúp học sinh lớp 11 nắm vững kiến thức trọng tâm, ôn luyện để học tốt môn Hóa học 11.
Lý thuyết Sulfuric acid và muối sulfate (Hóa 11 Kết nối tri thức Bài 8)
(199k) Xem Khóa học Hóa 11 KNTT
I. Sulfuric acid
1. Cấu tạo phân tử
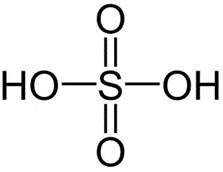
Phân tử sulfuric acid (H2SO4) có công thức cấu tạo:
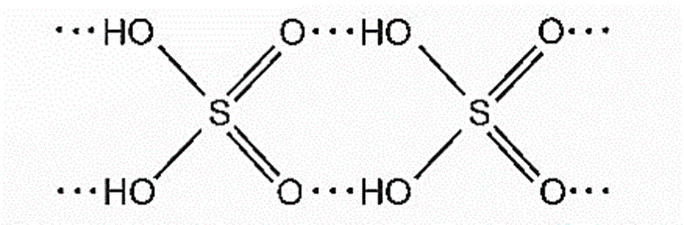
Với cấu tạo gồm các nguyên tử hydrogen linh động và các nguyên tử oxygen có độ âm điện lớn, giữa các phân tử sulfuric acid hình thành nhiều liên kết hydrogen:
2. Tính chất vật lí
Ở điều kiện thường, sulfuric acid là chất lỏng sánh như dầu, không màu, không bay hơi, có tính hút ẩm mạnh.
Dung dịch sulfuric acid 98% có khối lượng riêng 1,84 g/cm3, nặng gần gấp hai lần nước.
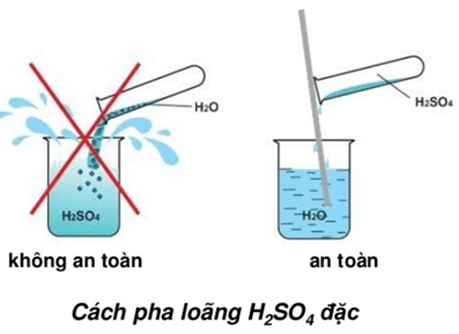
Sulfuric acid tan vô hạn trong nước và toả rất nhiều nhiệt. Do vậy, tuyệt đối không tự ý pha loãng sulfuric acid. Khi pha loãng dung dịch sulfuric acid đặc, để đảm bảo an toàn phải rót từ từ dung dịch sulfuric acid đặc vào nước, vừa rót vừa khuấy (không làm ngược lại).
3. Quy tắc an toàn
a) Bảo quản
Sulfuric acid được bảo quản trong chai, lọ có nút đậy chặt, đặt ở vị trí chắc chắn.
Đặt chai, lọ đựng dung dịch sulfuric acid đặc cách xa các lọ chứa chất dễ gây cháy, nổ như chlorate, perchlorate, permanganate, dichromate.
b) Sử dụng
Sulfuric acid gây bỏng khi rơi vào da, do vậy khi sử dụng cần tuân thủ các nguyên tắc:
(1) Sử dụng găng tay, đeo kính bảo hộ, mặc áo thí nghiệm.
(2) Cầm dụng cụ chắc chắn, thao tác cẩn thận.
(3) Không tì, đè chai đựng acid lên miệng cốc, ống đong khi rót acid.
(4) Sử dụng lượng acid vừa phải, lượng acid còn thừa phải thu hồi vào lọ đựng.
(5) Không được đổ nước vào dung dịch acid đặc.
c) Sơ cứu khi bỏng acid
Khi bị bỏng sulfuric acid cần thực hiện sơ cứu theo các bước sau:
(1) Nhanh chóng rửa ngay với nước lạnh nhiều lần để làm giảm lượng acid bám trên da. Nếu bị bỏng ở vùng mặt nhưng acid chưa bắn vào mắt thì nhắm chặt mắt khi ngâm rửa. Nếu acid đã bắn vào mắt thì úp mặt vào chậu nước sạch, mở mắt và chớp nhiều lần để rửa acid.
(2) Sau khi ngâm rửa bằng nước, cần tiến hành trung hoà acid bằng dung dịch NaHCO3
loãng (khoảng 2%).
(3) Băng bó tạm thời vết bỏng bằng băng sạch, cho người bị bỏng uống bù nước điện giải rồi đưa đến cơ sở y tế gần nhất.
4. Tính chất hoá học
a) Dung dịch sulfuric acid loãng
Dung dịch sulfuric acid loãng có đầy đủ tính chất của một acid mạnh.
- Làm đổi màu quỳ tím thành đỏ;
- Tác dụng với nhiều kim loại (Mg, Al, Zn, Fe,...) tạo thành muối sulfate và giải phóng khí hydrogen.
Ví dụ:
H2SO4 (loãng) + Mg → MgSO4 + H2
3H2SO4 (loãng) + 2Al → Al2(SO4)3 + 3H2
Chú ý: Các kim loại Hg, Cu, Ag, Au, Pt …không tác dụng với H2SO4 loãng.
Khi Fe tác dụng với H2SO4 loãng, sản phẩm thu được là muối iron(II).
H2SO4 (loãng) + Fe → FeSO4 + H2
-Tác dụng với base tạo thành muối sulfate và nước.
Ví dụ:
H2SO4 + Cu(OH)2 → CuSO4 + 2H2O
H2SO4 + 2KOH → K2SO4 + 2H2O
-Tác dụng với basic oxide tạo thành muối sulfate và nước.
Ví dụ:
H2SO4 + CuO → CuSO4 + H2O
H2SO4 + Na2O → Na2SO4 + H2O
- Tác dụng với một số muối tạo thành muối sulfate và acid mới
Ví dụ:
MgCO3 + H2SO4 → MgSO4 + CO2 + H2O
b) Dung dịch sulfuric acid đặc
- Tính acid
Dung dịch sulfuric acid đặc có tính acid mạnh và khó bay hơi, được sử dụng để điều chế một số acid dễ bay hơi.
Ví dụ: Dung dịch sulfuric acid đặc được dùng trong công nghiệp để điều chế HF bằng cách tác dụng với quặng fluorite.
CaF2 + H2SO4 →250oCCaSO4 + 2HF
- Tính oxi hoá
Dung dịch sulfuric acid đặc thể hiện tính oxi hoá mạnh, nhất là khi đun nóng, kèm theo sự giảm số oxi hoá của nguyên tử sulfur:
S+6+2e→S+4;S+6+6e→S0;S+6+8e→S-2;
Dung dịch sulfuric acid đặc, nóng oxi hoá được nhiều kim loại, phi kim và hợp chất.
Ví dụ:
Cu + 2H2SO4 →toCuSO4 + SO2 + 2H2O
C + 2H2SO4 →to CO2 + 2SO2 + 2H2O
2KBr + 2H2SO4 →to Br2 + SO2 + 2H2O + K2SO4
- Tính háo nước
Dung dịch sulfuric acid đặc có khả năng lấy nước từ hợp chất carbohydrate và khiến chúng hoá đen (hiện tượng than hoá).
H2SO4 đặc tác dụng với đường.
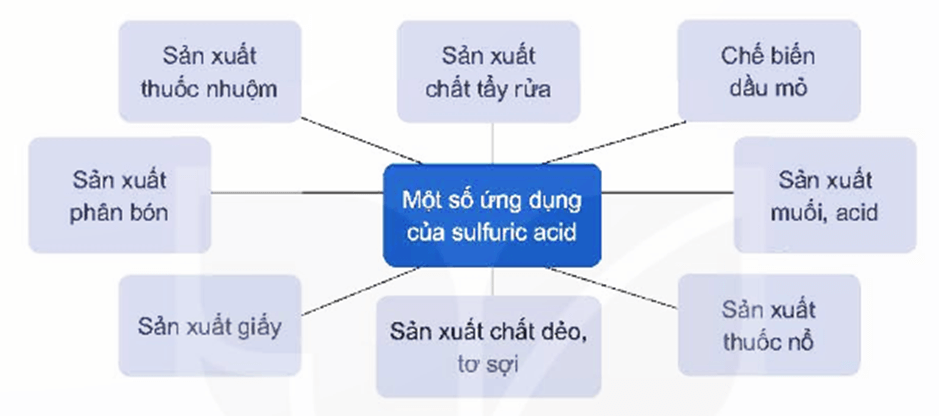
5. Ứng dụng
Một số ứng dụng của sulfuric acid được thể hiện trong sơ đồ sau:
6. Sản xuất
Trong công nghiệp, sulfuric acid chủ yếu được sản xuất bằng phương pháp tiếp xúc, đi từ nguyên liệu chính là sulfur, quặng pyrite (chứa FeS2).
Phương pháp tiếp xúc gồm ba giai đoạn chính.
Giai đoạn 1: Sản xuất sulfur dioxide
Tuỳ thuộc vào nguồn nguyên liệu, sulfur dioxide được sản xuất bằng cách đốt cháy sulfur, pyrite hoặc quặng sulfide trong lò đốt bằng không khí.
S(g) + O2(g) →to SO2(g)
4FeS2(s) + 11O2(g) →to 2Fe2O3(s) + 8SO2(g)
Giai đoạn 2: Sản xuất sulfur trioxide
Oxi hoá sulfur dioxide bằng không khí dư ở nhiệt độ khoảng 450 oC, áp suất 1 – 2 bar, xúc tác vanadium(V) oxide (V2O5), hiệu suất đạt trên 98%:
2SO2(g) + O2(g) ⇌V2O5,to2SO3(g)
Giai đoạn 3: Hấp thụ sulfur trioxide bằng sulfuric acid đặc, tạo ra oleum (hỗn hợp các acid có công thức chung dạng H2SO4.nSO3). Sau đó, pha loãng oleum vào nước thu được dung dịch sulfuric acid loãng.
II. Muối sulfate
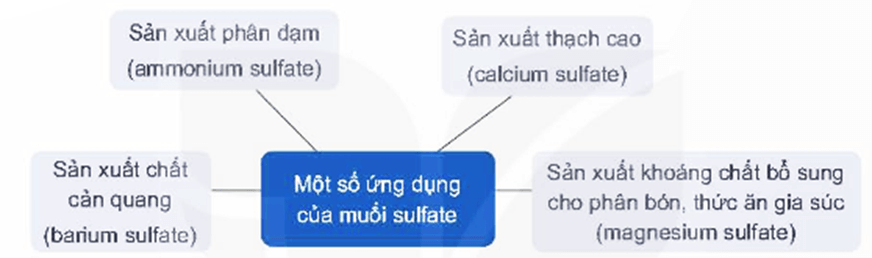
1. Ứng dụng
Một số ứng dụng của muối sulfate được thể hiện trong sơ đồ sau:
2. Nhận biết
Thuốc thử nhận biết ion sulfate là dung dịch muối barium hoặc dung dịch Ba(OH)2. Sản phẩm phản ứng là barium sulfate BaSO4 kết tủa trắng, không tan trong acid.
H2SO4 + BaCl2 →BaSO4↓ + 2HCl
Na2SO4 + Ba(OH)2 →BaSO4↓ + 2NaOH
Kết tủa trắng BaSO4
(199k) Xem Khóa học Hóa 11 KNTT
Xem thêm tóm tắt lý thuyết Hóa học lớp 11 Kết nối tri thức hay khác:
Xem thêm các tài liệu học tốt lớp 11 hay khác:
- Giải sgk Hóa học 11 Kết nối tri thức
- Giải Chuyên đề học tập Hóa 11 Kết nối tri thức
- Giải SBT Hóa học 11 Kết nối tri thức
- Giải lớp 11 Kết nối tri thức (các môn học)
- Giải lớp 11 Chân trời sáng tạo (các môn học)
- Giải lớp 11 Cánh diều (các môn học)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Soạn văn 11 (hay nhất) - KNTT
- Soạn văn 11 (ngắn nhất) - KNTT
- Giải sgk Toán 11 - KNTT
- Giải Tiếng Anh 11 Global Success
- Giải sgk Tiếng Anh 11 Smart World
- Giải sgk Tiếng Anh 11 Friends Global
- Giải sgk Vật Lí 11 - KNTT
- Giải sgk Hóa học 11 - KNTT
- Giải sgk Sinh học 11 - KNTT
- Giải sgk Lịch Sử 11 - KNTT
- Giải sgk Địa Lí 11 - KNTT
- Giải sgk Giáo dục KTPL 11 - KNTT
- Giải sgk Tin học 11 - KNTT
- Giải sgk Công nghệ 11 - KNTT
- Giải sgk Hoạt động trải nghiệm 11 - KNTT
- Giải sgk Giáo dục quốc phòng 11 - KNTT
- Giải sgk Âm nhạc 11 - KNTT








 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

