Lý thuyết về Thành phần nguyên tử (đầy đủ, chi tiết nhất)
Bài viết Lý thuyết về Thành phần nguyên tử hay, chi tiết giúp bạn nắm vững kiến thức trọng tâm về Thành phần nguyên tử.
Lý thuyết về Thành phần nguyên tử (đầy đủ, chi tiết nhất)
Thi online Hóa 10 KNTTThi online Hóa 10 CDThi online Hóa 10 CTST
Bài giảng: Bài 3: Luyện tập: Thành phần nguyên tử - Cô Phạm Thu Huyền (Giáo viên VietJack)
1/ Cấu tạo nguyên tử
Nguyên tử có cấu taọ phức tạp gồm hai phần: Vỏ và Hạt nhân.
a) Vỏ nguyên tử: gồm các hạt electron mang điện âm (kí hiệu là e) chuyển động rất nhanh xung quanh hạt nhân không theo một quỹ đạo xác định nào.
b) Hạt nhân nguyên tử: gồm neutron và proton.
qe = 1-; qp = 1+; qn = 0
Điện tích của hạt nhân nguyên tử chỉ phụ thuộc vào số proton có trong hạt nhân của nguyên tử ⇒ Hạt nhân mang điện dương.
2/ Kích thước: nguyên tử có dạng hình cầu → rất nhỏ.
Đơn vị đo: Nanomet (nm) và Angstrom (Å).
1nm = 10-9m và 1Å = 10-10m ⇒ 1nm = 10Å
3/ Khối lượng: Rất nhỏ
1 amu hay 1u = 1/12 . m12C = 1,6605.10-27 không gian.
Khối lượng e rất nhỏ có thể bỏ qua – vậy khối lượng nguyên tử tập trung vào hạt nhân.
4/ Trong nguyên tử:
- Số Electron = Số Proton.
- Số khối: A = Z + N.
- Số đơn vị ĐTHN nguyên tử của một nguyên tố được coi là số hiệu nguyên tố đó.
SHNT (Z) = Số đơn vị ĐTHN = số proton = số electron
5/ Kí hiệu nguyên tử
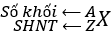
6/ Đồng vị
Đồng vị là những nguyên tử của cùng một nguyên tố hóa học có cùng số proton (hay ĐTHN Z) nhưng khác nhau về số neutron (hay số khối A).
Công thức tính nguyên tử khối trung bình của một nguyên tố có nhiều đồng vị:
A1X (x%), A2X (y%), A3X (z%)…
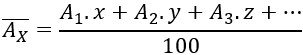
7/ Obitan nguyên tử
- Khu vực xung quanh hạt nhân mà tại đó xác suất có mặt của electron là lớn nhất được goi là obitan nguyên tử.
- Obitan s có dạng hình cầu, obitan p có dạng hình số 8 nổi, obitan d, f có hình phức tạp.
Thi online Hóa 10 KNTTThi online Hóa 10 CDThi online Hóa 10 CTST
Xem thêm các phần Lý thuyết Hóa học lớp 10 ôn thi Tốt nghiệp THPT khác:
Để học tốt lớp 10 các môn học sách mới:
- Giải bài tập Lớp 10 Kết nối tri thức
- Giải bài tập Lớp 10 Chân trời sáng tạo
- Giải bài tập Lớp 10 Cánh diều
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 10 Global Success
- Giải Tiếng Anh 10 Friends Global
- Giải sgk Tiếng Anh 10 iLearn Smart World
- Giải sgk Tiếng Anh 10 Explore New Worlds
- Lớp 10 - Kết nối tri thức
- Soạn văn 10 (hay nhất) - KNTT
- Soạn văn 10 (ngắn nhất) - KNTT
- Soạn văn 10 (siêu ngắn) - KNTT
- Giải sgk Toán 10 - KNTT
- Giải sgk Vật lí 10 - KNTT
- Giải sgk Hóa học 10 - KNTT
- Giải sgk Sinh học 10 - KNTT
- Giải sgk Địa lí 10 - KNTT
- Giải sgk Lịch sử 10 - KNTT
- Giải sgk Kinh tế và Pháp luật 10 - KNTT
- Giải sgk Tin học 10 - KNTT
- Giải sgk Công nghệ 10 - KNTT
- Giải sgk Hoạt động trải nghiệm 10 - KNTT
- Giải sgk Giáo dục quốc phòng 10 - KNTT
- Lớp 10 - Chân trời sáng tạo
- Soạn văn 10 (hay nhất) - CTST
- Soạn văn 10 (ngắn nhất) - CTST
- Soạn văn 10 (siêu ngắn) - CTST
- Giải Toán 10 - CTST
- Giải sgk Vật lí 10 - CTST
- Giải sgk Hóa học 10 - CTST
- Giải sgk Sinh học 10 - CTST
- Giải sgk Địa lí 10 - CTST
- Giải sgk Lịch sử 10 - CTST
- Giải sgk Kinh tế và Pháp luật 10 - CTST
- Giải sgk Hoạt động trải nghiệm 10 - CTST
- Lớp 10 - Cánh diều
- Soạn văn 10 (hay nhất) - Cánh diều
- Soạn văn 10 (ngắn nhất) - Cánh diều
- Soạn văn 10 (siêu ngắn) - Cánh diều
- Giải sgk Toán 10 - Cánh diều
- Giải sgk Vật lí 10 - Cánh diều
- Giải sgk Hóa học 10 - Cánh diều
- Giải sgk Sinh học 10 - Cánh diều
- Giải sgk Địa lí 10 - Cánh diều
- Giải sgk Lịch sử 10 - Cánh diều
- Giải sgk Kinh tế và Pháp luật 10 - Cánh diều
- Giải sgk Tin học 10 - Cánh diều
- Giải sgk Công nghệ 10 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 10 - Cánh diều
- Giải sgk Giáo dục quốc phòng 10 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

