Cách giải bài tập về Độ rượu, Điều chế, nhận biết Ancol (hay, chi tiết)
Bài viết Cách giải bài tập về Độ rượu, Điều chế, nhận biết Ancol với phương pháp giải chi tiết giúp học sinh ôn tập, biết cách làm bài tập Độ rượu, Điều chế, nhận biết Ancol.
Cách giải bài tập về Độ rượu, Điều chế, nhận biết Ancol (hay, chi tiết)
Thi online Hóa 11 KNTTThi online Hóa 11 CDThi online Hóa 11 CTST
A. Phương pháp giải & Ví dụ minh họa
- Độ rượu (ancol) là thể tích (cm3, ml) của ancol nguyên chất trong 100 thể tích (cm3, ml) dung dịch ancol.
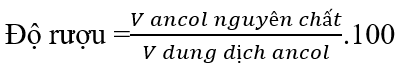
- Muốn tăng độ rượu: thêm ancol nguyên chất vào dung dịch; muốn giảm độ rượu: thêm nước vào dung dịch ancol.
- Nhận biết glycerol bằng copper hydroxide tạo phức màu xanh.
- Điều chế ancol: đi từ dẫn xuất halogen hoặc alkene hợp nước.
Ví dụ minh họa
Bài 1: Cho 20ml cồn tác dụng với Na dư thì thu được 0,16 g H2 (khối lượng riêng của ethyl alcohol là 0,8 g/ml). Độ rượu trong loại cồn trên là bao nhiêu?
Lời giải:
Phương trình phản ứng: C2H5OH + Na → C2H5ONa + 1/2 H2
Số mol H2 sinh ra: nH2 = 0,16/2 = 0,08 mol
Số mol ancol là: nancol = 0,08.2 = 0,16 mol
Khối lượng ancol: mancol = 0,16.46 = 7,36 g
Thể tích dung dịch ethyl alcohol: Vancol = 7,36/0,8 = 9,2 ml
Độ rượu trong loại cồn trên là:
Độ rượu = 9,2.100/20 = 46º
Bài 2: Tính khối lượng glucose cần lấy để điều chế a lit ethyl alcohol 45º biết D = 0,8g/ml và hiệu suất phản ứng điều chế là 75%. Lượng khí CO2 sinh ra hấp thụ hoàn toàn vào 1 lit dd Ca(OH)2 1M thu được 60 gam kết tủa. Tính a?
Lời giải:
Phương trình phản ứng: C6H12O6 −lên men→ 2CO2 + 2C2H5OH
nCa(OH)2 = 1 mol ; nCaCO3 = 0,6 mol ⇒ nCa(HCO3)2 = 1-0,6 = 0,4 mol
Vậy số mol CO2 sinh ra từ phản ứng lên men là: nCO2 = 0,6 + 0,4.2 = 1,4 mol
Theo phương trình phản ứng: nancol = nCO2 = 1,4 mol
Khối lượng ancol: mancol = 1,4 .46 = 64,4 g
⇒ Vancol = 64,4/0,8 = 80,5 ml
Giá trị của a: a = 80,5.100/45 = 178,9 ml
Khối lượng glucose cần lấy là:
mglucose = 1,4.100.180/75.2 = 168 g
B. Bài tập trắc nghiệm
Bài 1: Để phân biệt ethyl alcohol nguyên chất và ethyl alcohol có lẫn nước, người ta thường dùng thuốc thử là chất nào sau đây ?
A. CuSO4 khan. B. Na kim loại. C. benzene. D. CuO.
Lời giải:
Đáp án: A
Bài 2: ethyl alcohol 40º có nghĩa là
A. trong 100 gam dung dịch ancol có 40 gam ancol C2H5OH nguyên chất.
B. trong 100ml dung dịch ancol có 60 gam nước.
C. trong 100ml dung dịch ancol có 40ml C2H5OH nguyên chất.
D. trong 100 gam ancol có 60ml nước.
Lời giải:
Đáp án: C
Bài 3: ethyl alcohol được tạo ra khi
A. Thuỷ phân saccharose B. lên men glucose
C. Thuỷ phân đường maltose D. thuỷ phân tinh bột.
Lời giải:
Đáp án: B
Bài 4: Phương pháp nào điều chế ethyl alcohol dưới đây chỉ dùng trong phòng thí nghiệm
A. Lên men tinh bột.
B. Thuỷ phân Ethyl bromua trong dung dịch kiềm khi đun nóng.
C. Hiđrat hoá etilen xúc tác axit.
D. Phản ứng khử aldehyde acetic bằng H2 xúc tác Ni đun nóng.
Lời giải:
Đáp án: B
Bài 5: Đem hòa tan ethylic alcohol vào nước được 215,06 ml dung dịch rượu có nồng độ 27,6%, khối lượng riêng của dung dịch rượu là 0,93 g/ml, khối lượng riêng của ethylic alcohol nguyên chất là 0,8 g/ml. Dung dịch trên có độ rượu là:
A. 27,6º B. 22º C. 32º D. Đáp án khác.
Lời giải:
Đáp án: D
mancol = 215,06.0,93.27,6/100 = 55,2 g ⇒ Vancol = 55,2/0,8 = 69 ml ⇒ Độ rượu = 69/215,06.100 = 32º
Bài 6: Đun nóng V ml ethylic alcohol 95º với H2SO4 đặc ở 180ºC thu được 3,36 lít etilen đktc. Biết hiệu suất phản ứng là 60% và khối lượng riêng của rượu là 0,8 gam/ml. Giá trị của V là
A.10,18 ml B.15,13 ml C.8,19 ml D.12 ml
Lời giải:
Đáp án: B
netilen = 0,15 mol ⇒ nrượu = 0,15.100/60 = 0,25 mol ⇒ Vancol = 0,25.46/0,8 = 14,375 ml ⇒ Vdd rượu = 14,375.100/95 = 15,13 ml
Bài 7: Cho m gam tinh bột lên men thành C2H5OH với hiệu suất 81%, hấp thụ hết lượng CO2 sinh ra vào dung dịch Ca(OH)2 được 55 gam kết tủa và dung dịch X. Đun nóng dung dịch X lại có 10 gam kết tủa nữa. Giá trị m là
A. 75 gam. B. 125 gam. C. 150 gam. D. 225 gam.
Lời giải:
Đáp án: C
C6H12O6 −lên men→ 2CO2 + 2C2H5OH
Ca(OH)2 + CO2 → CaCO3 + 2H2O
nCaCO3 = 0,55 mol ; nCa(HCO3)2 = 0,1 mol ⇒ nCO2 = 0,75 mol ⇒ ntinh bột = 0,75.100/81 = 0,925 mol ⇒ m = 0,925.162 = 150 g
Bài 8: Lên men hoàn toàn m gam glucose thành ethyl alcohol. Toàn bộ khí CO2 sinh ra trong quá trình này được hấp thụ hết vào dung dịch Ca(OH)2 dư tạo ra 40 gam kết tủa. Nếu hiệu suất của quá trình lên men là 75% thì giá trị của m là
A. 60. B. 58. C. 30. D. 48.
Lời giải:
Đáp án: D
C6H12O6 −lên men→ 2CO2 + 2C2H5OH
Ca(OH)2 + CO2 → CaCO3 + 2H2O
nCO2 = nCaCO3 = 0,4 mol ⇒ nglucose = .0,4.100/75.2 = 4/15 mol ⇒ m = (4/15).180 = 48 g.
Thi online Hóa 11 KNTTThi online Hóa 11 CDThi online Hóa 11 CTST
Xem thêm các dạng bài tập Hóa học lớp 11 có trong đề thi Tốt nghiệp THPT khác:
- Dạng 1: Bài tập lý thuyết về dẫn xuất halogen, ancol, phenol
- Dạng 2: Cách viết đồng phân, gọi tên dẫn xuất halogen
- Dạng 3: Cách viết đồng phân, gọi tên Ancol, Phenol
- Dạng 4: Bài tập về dẫn xuất halogen
- Dạng 5: Ancol phản ứng với kim loại kiềm
- Dạng 6: Phenol phản ứng với kim loại kiềm và dung dịch kiềm
- Dạng 7: Phản ứng tách nước của Ancol
- Dạng 8: Phản ứng oxi hóa ancol
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 11 Global Success
- Giải sgk Tiếng Anh 11 Smart World
- Giải sgk Tiếng Anh 11 Friends Global
- Lớp 11 - Kết nối tri thức
- Soạn văn 11 (hay nhất) - KNTT
- Soạn văn 11 (ngắn nhất) - KNTT
- Giải sgk Toán 11 - KNTT
- Giải sgk Vật Lí 11 - KNTT
- Giải sgk Hóa học 11 - KNTT
- Giải sgk Sinh học 11 - KNTT
- Giải sgk Lịch Sử 11 - KNTT
- Giải sgk Địa Lí 11 - KNTT
- Giải sgk Giáo dục KTPL 11 - KNTT
- Giải sgk Tin học 11 - KNTT
- Giải sgk Công nghệ 11 - KNTT
- Giải sgk Hoạt động trải nghiệm 11 - KNTT
- Giải sgk Giáo dục quốc phòng 11 - KNTT
- Giải sgk Âm nhạc 11 - KNTT
- Lớp 11 - Chân trời sáng tạo
- Soạn văn 11 (hay nhất) - CTST
- Soạn văn 11 (ngắn nhất) - CTST
- Giải sgk Toán 11 - CTST
- Giải sgk Vật Lí 11 - CTST
- Giải sgk Hóa học 11 - CTST
- Giải sgk Sinh học 11 - CTST
- Giải sgk Lịch Sử 11 - CTST
- Giải sgk Địa Lí 11 - CTST
- Giải sgk Giáo dục KTPL 11 - CTST
- Giải sgk Hoạt động trải nghiệm 11 - CTST
- Giải sgk Âm nhạc 11 - CTST
- Lớp 11 - Cánh diều
- Soạn văn 11 Cánh diều (hay nhất)
- Soạn văn 11 Cánh diều (ngắn nhất)
- Giải sgk Toán 11 - Cánh diều
- Giải sgk Vật Lí 11 - Cánh diều
- Giải sgk Hóa học 11 - Cánh diều
- Giải sgk Sinh học 11 - Cánh diều
- Giải sgk Lịch Sử 11 - Cánh diều
- Giải sgk Địa Lí 11 - Cánh diều
- Giải sgk Giáo dục KTPL 11 - Cánh diều
- Giải sgk Tin học 11 - Cánh diều
- Giải sgk Công nghệ 11 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 11 - Cánh diều
- Giải sgk Giáo dục quốc phòng 11 - Cánh diều
- Giải sgk Âm nhạc 11 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

