Bài tập về Hợp chất của cacbon (có lời giải)
Tài liệu Bài tập về Hợp chất của cacbon có lời giải Hóa học lớp 9 với đầy đủ phương pháp giải chi tiết, các bài tập tự luyện đa dạng ở nhiều mức độ giúp bạn biết cách giải các dạng bài tập môn Hóa học lớp 9 từ đó ôn tập và đạt điểm cao trong bài thi môn Hóa học 9.
Bài tập về Hợp chất của cacbon (có lời giải)
Thi online KHTN 9 KNTTThi online KHTN 9 CDThi online KHTN 9 CTST
I – LÝ THUYẾT VÀ PHƯƠNG PHÁP GIẢI
Để làm được các bài tập về hợp chất của cacbon, học sinh cần nắm được các tính chất hóa học của một số hợp chất của cacbon như sau:
1. Carbon monoxide (CO)
a) CO là oxit trung tính
Ở điều kiện thường không phản ứng với nước, kiềm và axit.
b) CO là chất khử
- Ở nhiệt độ cao, cacbon oxit khử được nhiều oxit kim loại
Ví dụ:
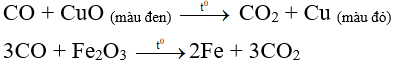
- CO cháy trong oxi hoặc trong không khí với ngọn lửa màu xanh, tỏa nhiều nhiệt.
Phương trình hóa học:
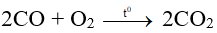
2. Carbon dioxide (CO2)
CO2 là một acidic oxide.
a) Tác dụng với nước tạo thành carbonic acid
Phương trình hóa học: CO2 + H2O ⇄ H2CO3
Chú ý: CO2 phản ứng với nước tạo thành dung dịch axit, làm quỳ tím chuyển sang màu đỏ. H2CO3 không bền, dễ phân hủy thành CO2 và nước, khi đun nóng dung dịch thu được sẽ lại làm quỳ màu đỏ chuyển sang màu tím.
b) Tác dụng với dung dịch bazơ
Khí CO2 tác dụng với dung dịch bazơ tạo thành muối và nước. Tùy theo tỉ lệ số mol giữa CO2 và dung dịch bazơ mà có thể tạo ra muối trung hòa, muối axit hay hỗn hợp hai muối.
Ví dụ:
CO2 + 2NaOH → Na2CO3 + H2O
1 mol 2 mol
CO2 + NaOH → NaHCO3
1 mol 1 mol
c) Tác dụng với basic oxide
CO2 tác dụng với basic oxide (tan) tạo thành muối.
Ví dụ:
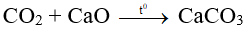
3. Muối carbonate
a) Tác dụng với axit:
Muối carbonate tác dụng với dung dịch axit mạnh hơn carbonic acid (như HCl, HNO3, H,SO4,...) tạo thành muối mới và giải phóng CO2.
Ví dụ:
NaHCO3 + HCl → NaCl + CO2↑ + H2O
CaCO3 + H2SO4 → CaSO4 + CO2 ↑+ H2O
b) Tác dụng với dung dịch bazơ
Một số dung dịch muối carbonate tác dụng với dung dịch bazơ tạo thành muối carbonate không tan và bazơ mới.
Ví dụ:
K2CO3 + Ca(OH)2 → 2KOH + CaCO3 ↓
Muối hydrocarbon?t tác dụng với dung dịch kiềm tạo thành muối trung hòa và nước
Ví dụ:
KHCO3 + KOH → K2CO3 + H2O
Ba(HCO3)2 + Ba(OH)2 → 2BaCO3↓ + 2H2O
c) Tác dụng với dung dịch muối
Dung dịch muối carbonate tác dụng với một số dung dịch muối tạo thành 2 muối mới
Ví dụ:
Na2CO3 + CaCl2 → 2NaCl + CaCO3↓
d) Muối carbonate bị nhiệt phân hủy
Nhiều muối carbonate (trừ muối carbonate trung hòa của kim loại kiềm) dễ bị nhiệt phân hủy giải phóng khí CO2
Ví dụ:
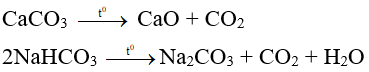
II – MỘT SỐ VÍ DỤ MINH HỌA
Ví dụ 1: Khử hoàn toàn 4,8 gam copper (II) oxide bằng khí CO. Thể tích khí CO cần dùng (đktc) là
A. 1,344 lít.
B. 1,12 lít.
C. 6,72 lít.
D. 4,48 lít.
Hướng dẫn giải:
Đáp án A
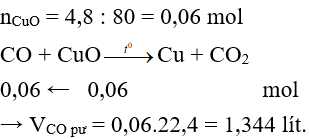
Ví dụ 2: Người ta dùng 22 gam CO2 hấp thụ vào dung dịch chứa 20 gam NaOH. Khối lượng muối tạo thành là
A. 45 gam.
B. 44 gam.
C. 43 gam.
D. 42 gam.
Hướng dẫn giải
Đáp án D
Ta có:
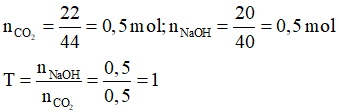
Phương trình hóa học xảy ra:
NaOH + CO2→ NaHCO3
0,5 0,5 → 0,5 mol
→ mmuối = 0,5.84 = 42 gam.
Ví dụ 3: Nung hoàn toàn hỗn hợp 2 muối CaCO3 và MgCO3 thu được 76 gam hai oxit và 33,6 lít CO2 (đktc). Khối lượng hỗn hợp muối ban đầu là
A. 142 gam.
B. 124 gam.
C. 141 gam.
D. 140 gam.
Hướng dẫn giải
Đáp án A
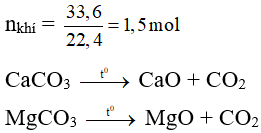
Bảo toàn khối lượng có: mmuối = moxit + mkhí = 76 + 1,5.44 = 142 gam.
III – Bài tập tự luyện
Bài 1. Khử hoàn toàn 3,2 gam Fe2O3 bằng khí CO dư. Sản phẩm khí thu được cho vào bình đựng nước vôi trong dư được a gam kết tủa màu trắng. Giá trị của a là
A. 5,0.
B. 6,0.
C. 4,0.
D. 3,0.
Lời giải:
Đáp án B
Số mol Fe2O3 là 3,2 : 160 = 0,02 mol
Phương trình hóa học:
3CO + Fe2O3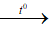 2Fe + 3CO2
2Fe + 3CO2
0,02 → 0,06 mol
CO2 + Ca(OH)2 (dư) → CaCO3 ↓ + H2O
0,06 → 0,06 mol
Vậy a = 0,06.100 = 6 gam.
Bài 2. Nung 13,4g hỗn hợp muối carbonate của hai kim loại hóa trị II. Sau khi phản ứng xảy ra hoàn toàn thu được 6,8g chất rắn và khí X. Lượng khí X sinh ra cho hấp thụ vào 75 ml dung dịch NaOH 1M thu được dung dịch chứa m gam muối. Tính m?
A. 4,2g.
B. 5,8g.
C. 6,3g.
D. 6,5g.
Lời giải:
Đáp án C
Khí X là CO2.
Bảo toàn khối lượng: mX = 13,4 – 6,8 = 6,6 gam
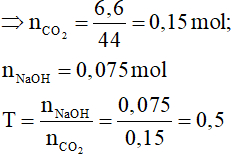
Vậy sau phản ứng chỉ thu được NaHCO3 và CO2 dư.
CO2 + NaOH → NaHCO3
0,15 0,075 → 0,075 mol
Vậy mmuối = 0,075.84 = 6,3 gam.
Bài 3: Sục 1,12 lít CO2 (đktc) vào 200ml dung dịch Ba(OH)2 0,2M. Khối lượng kết tủa thu được là
A. 5,91g.
B. 19,7g.
C. 78,8g.
D. 98,5g.
Lời giải:
Đáp án A
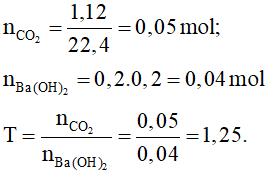
Vậy sau phản ứng thu được hai muối.
Phương trình hóa học:
CO2 + Ba(OH)2 → BaCO3↓ + H2O
x……..x…………..x mol
2CO2 + Ba(OH)2 → Ba(HCO3)2
2y…….y………….y mol
Ta có hệ phương trình:
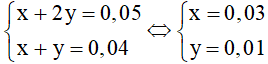
Kết tủa là BaCO3: 0,03 mol vậy m↓ = 0,03.197 = 5,91 gam.
Bài 4: Hấp thụ hoàn toàn 0,16 mol CO2 vào 2 lít dung dịch Ca(OH)2 0,05M được kết tủa X và dung dịch Y. Khi đó khối lượng dung dịch Y so với khối lượng dung dịch Ca(OH)2 ban đầu sẽ là
A. tăng 3,04g.
B. tăng 7,04g.
C. giảm 3,04g.
D. giảm 7,04g.
Lời giải:
Đáp án A
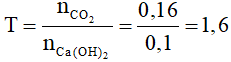
Vậy sau phản ứng thu được 2 muối. Phương trình hóa học:
CO2 + Ca(OH)2 → CaCO3↓ + H2O
x………x…………..x mol
2CO2 + Ca(OH)2 → Ca(HCO3)2
2y…….y……………y mol
Ta có hệ phương trình:
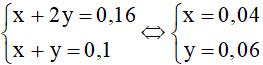
Kết tủa là CaCO3: 0,04 mol
Có
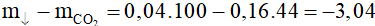
Vậy khối lượng dung dịch Y so với khối lượng dung dịch Ca(OH)2 ban đầu tăng 3,04 gam.
Bài 5: Khi đun nóng dung dịch canxi hydrocarbon?t thì có kết tủa xuất hiện. Tổng các hệ số tỉ lượng (là các số nguyên, tối giản) trong phương trình hóa học của phản ứng là
A. 4.
B. 5.
C. 6.
D. 7.
Lời giải:
Đáp án A
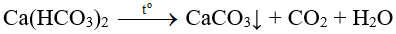
Tổng các hệ số: 1 + 1 + 1 + 1 = 4.
Bài 6: Để tạo độ xốp cho một số loại bánh, có thể dùng muối nào sau đây làm bột nở?
A. (NH4)2SO4.
B. NH4HCO3.
C. CaCO3.
D. NH4NO2.
Lời giải:
Đáp án B
Bài 7: Cặp chất nào sau đây không bị nhiệt phân?
A. CaCO3, BaCO3.
B. Ca(HCO3)2, Ba(HCO3)2.
C. Na2CO3, K2CO3.
D. NaHCO3, KHCO3.
Lời giải:
Đáp án C
Muối carbonate trung hòa của các kim loại Na, K … không bị nhiệt phân hủy.
Bài 8: Nhiệt phân hoàn toàn m gam hỗn hợp gồm CaCO3 và Na2CO3 thu được 11,6 gam chất rắn và 2,24 lít khí (đktc). Phần trăm khối lượng của CaCO3 trong X là
A. 6,25%.
B. 8,62%.
C. 50,2%.
D. 62,5%.
Lời giải:
Đáp án D
Bảo toàn khối lượng: m = 11,6 + 0,1.44 = 16 gam.
Trong hỗn hợp chỉ có CaCO3 bị nhiệt phân hủy.
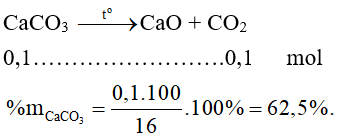
Bài 9: Cho V lít CO ở (đktc) phản ứng với 1 lượng dư hỗn hợp chất rắn gồm Cu và Fe3O4 nung nóng. Sau khi phản ứng hoàn toàn khối lượng chất rắn giảm 0,32 gam. Giá trị của V là
A. 0,112 lít.
B. 0,224 lít.
C. 0,448 lít.
D. 0,56 lít.
Lời giải:
Đáp án C
Vì Cu không phản ứng với CO, nên khối lượng giảm 0,32 gam là do biến đổi từ Fe3O4 thành Fe.
PTHH:
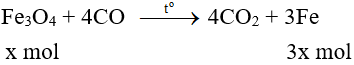
Vậy: 232x – 3x.56 = 0,32
→ x = 0,005 mol
→ nCO = 0,005.4 = 0,02 mol
VCO = 0,02.22,4 = 0,448 lít.
Bài 10: Cho luồng khí CO dư đi qua ống sứ đựng 8,04 gam hỗn hợp FeO và Fe2O3 (nung nóng), thu được m gam chất rắn và hỗn hợp khí X. Cho X vào dung dịch Ca(OH)2 dư, thu được 13,5 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 5,62.
B. 7,48.
C. 6,87.
D. 5,88.
Lời giải:
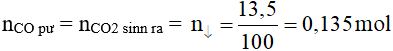
Bảo toàn khối lượng có: m = mCO + 8,04 – mCO2 = 0,135.28 + 8,04 – 0,135.44 = 5,88 gam.
Thi online KHTN 9 KNTTThi online KHTN 9 CDThi online KHTN 9 CTST
Xem thêm các dạng bài tập Hóa học lớp 9 chọn lọc, có lời giải chi tiết hay khác:
- Bài tập Clo và hợp chất của clo (có lời giải)
- Bài tập về Bảng tuần hoàn các nguyên tố hóa học (có lời giải)
- Bài tập Viết công thức cấu tạo của hợp chất hữu cơ (có lời giải)
- Bài tập Lập công thức phân tử của hợp chất hữu cơ (có lời giải)
- Bài tập về methane (có lời giải)
Xem thêm các loạt bài Để học tốt Hóa học 9 hay khác:
- Giải bài tập Hóa học 9
- Giải sách bài tập Hóa 9
- Đề thi Hóa học 9
- Wiki 200 Tính chất hóa học
- Wiki 3000 Phản ứng hóa học quan trọng
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Chuyên đề: Lý thuyết - Bài tập Hóa học lớp 9 có đáp án được biên soạn bám sát nội dung chương trình sgk Hóa học 9.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 9 Global Success
- Giải sgk Tiếng Anh 9 Smart World
- Giải sgk Tiếng Anh 9 Friends plus
- Lớp 9 Kết nối tri thức
- Soạn văn 9 (hay nhất) - KNTT
- Soạn văn 9 (ngắn nhất) - KNTT
- Giải sgk Toán 9 - KNTT
- Giải sgk Khoa học tự nhiên 9 - KNTT
- Giải sgk Lịch Sử 9 - KNTT
- Giải sgk Địa Lí 9 - KNTT
- Giải sgk Giáo dục công dân 9 - KNTT
- Giải sgk Tin học 9 - KNTT
- Giải sgk Công nghệ 9 - KNTT
- Giải sgk Hoạt động trải nghiệm 9 - KNTT
- Giải sgk Âm nhạc 9 - KNTT
- Giải sgk Mĩ thuật 9 - KNTT
- Lớp 9 Chân trời sáng tạo
- Soạn văn 9 (hay nhất) - CTST
- Soạn văn 9 (ngắn nhất) - CTST
- Giải sgk Toán 9 - CTST
- Giải sgk Khoa học tự nhiên 9 - CTST
- Giải sgk Lịch Sử 9 - CTST
- Giải sgk Địa Lí 9 - CTST
- Giải sgk Giáo dục công dân 9 - CTST
- Giải sgk Tin học 9 - CTST
- Giải sgk Công nghệ 9 - CTST
- Giải sgk Hoạt động trải nghiệm 9 - CTST
- Giải sgk Âm nhạc 9 - CTST
- Giải sgk Mĩ thuật 9 - CTST
- Lớp 9 Cánh diều
- Soạn văn 9 Cánh diều (hay nhất)
- Soạn văn 9 Cánh diều (ngắn nhất)
- Giải sgk Toán 9 - Cánh diều
- Giải sgk Khoa học tự nhiên 9 - Cánh diều
- Giải sgk Lịch Sử 9 - Cánh diều
- Giải sgk Địa Lí 9 - Cánh diều
- Giải sgk Giáo dục công dân 9 - Cánh diều
- Giải sgk Tin học 9 - Cánh diều
- Giải sgk Công nghệ 9 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 9 - Cánh diều
- Giải sgk Âm nhạc 9 - Cánh diều
- Giải sgk Mĩ thuật 9 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

