Các dạng bài tập Dẫn xuất của hydrocarbon; polymer (có lời giải)
Tổng hợp Lý thuyết và các dạng bài tập Dẫn xuất của hydrocarbon; polymer lớp 9 với phương pháp giải chi tiết và bài tập đa dạng có lời giải giúp bạn nắm vững kiến thức trọng tâm và biết cách làm bài tập Hóa học 9.
Các dạng bài tập Dẫn xuất của hydrocarbon; polymer (có lời giải)
Thi online KHTN 9 KNTTThi online KHTN 9 CDThi online KHTN 9 CTST
Lý thuyết & bài tập trắc nghiệm Dẫn xuất của hydrocarbon; polymer
- Lý thuyết ethylic alcohol (hay, chi tiết)
- Trắc nghiệm ethylic alcohol
- Bài tập trắc nghiệm ethylic alcohol
- Lý thuyết acetic acid (hay, chi tiết)
- Trắc nghiệm acetic acid
- Bài tập trắc nghiệm acetic acid
- Lý thuyết Mối liên hệ giữa etilen, ethylic alcohol và acetic acid (hay, chi tiết)
- Trắc nghiệm Mối liên hệ giữa etilen, ethylic alcohol và acetic acid
- Bài tập trắc nghiệm Mối liên hệ giữa etilen, ethylic alcohol và acetic acid
- Lý thuyết Chất béo (hay, chi tiết)
- Trắc nghiệm Chất béo
- Bài tập trắc nghiệm Chất béo
- Lý thuyết tổng hợp ethylic alcohol, acetic acid và chất béo (hay, chi tiết)
- Trắc nghiệm tổng hợp ethylic alcohol, acetic acid và chất béo
- Lý thuyết glucose (hay, chi tiết)
- Trắc nghiệm glucose
- Bài tập trắc nghiệm glucose
- Lý thuyết saccharose (hay, chi tiết)
- Trắc nghiệm saccharose
- Bài tập trắc nghiệm saccharose
- Lý thuyết Tinh bột và Cellulose (hay, chi tiết)
- Trắc nghiệm Tinh bột và Cellulose
- Bài tập trắc nghiệm Tinh bột và Cellulose
- Lý thuyết Protein (hay, chi tiết)
- Trắc nghiệm Protein
- Bài tập trắc nghiệm Protein
- Lý thuyết polymer (hay, chi tiết)
- Trắc nghiệm polymer
- Bài tập trắc nghiệm polymer
- Tổng hợp lý thuyết ôn tập cuối năm Hóa học 9 (hay, chi tiết)
- Trắc nghiệm Ôn tập cuối năm
Các dạng bài tập Dẫn xuất của hydrocarbon; polymer
- Bài tập về độ rượu và cách giải
- Phản ứng lên men rượu, lên men giấm và cách giải bài tập
- Bài tập tổng hợp về ethylic alcohol và cách giải
- Bài tập tổng hợp về acetic acid và cách giải
- Bài tập về phản ứng ester hóa và cách giải
- Phản ứng tráng gương của glucose và cách giải bài tập
- Thủy phân chất béo và cách giải bài tập
- Thủy phân tinh bột, Cellulose và cách giải bài tập
- Tính số mắt xích polymer và cách giải bài tập
- Bài tập nhận biết, phân biệt các hợp chất hữu cơ và cách giải
- Bài tập về chuỗi phản ứng hóa học hữu cơ và cách giải
Dạng 3: Mối liên hệ giữa etilen, ethylic alcohol và acetic acid
Phương pháp giải bài tập về độ rượu
Lý thuyết và Phương pháp giải
I. Định nghĩa:
Độ rượu là số ml rượu nguyên chất trong 100 ml hỗn hợp rượu với nước.
II. Công thức cần nhớ
- Công thức tính độ rượu
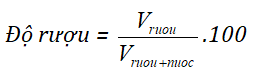
- Công thức khối lượng riêng
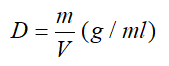
III. Phương pháp giải
- Bước 1: Xử lý dữ kiện đề bài cho.
- Bước 2: Tính Vrươu, Vruou+nuoc.
- Bước 3: Tính độ rượu cần tìm.
Bài tập tự luyện
Bài 1: Hòa tan m gam ethyl alcohol (D=0,8 gam/ml) vào 216 ml nước (D=1 gam/ml) tạo thành dung dịch A. Cho A tác dụng với Na dư thu được 170,24 lit (đktc) khí H2. Dung dịch A có độ rượu bằng bao nhiêu?
Lời giải:
Na + C2H5OH → C2H5ONa + 1/2H2
----------x-------------x-----------x/2
Na + H2O → NaOH + 1/2H2
--------y---------y---------y/2
Theo bài ta có DH2O = 1 gam/ml
⇒ mH2O = 216 gam ⇒ nH2O = 216/18 = 12 mol = y
Mà nH2 = x/2 + y/2 = 170,24/22,4 = 7,6 mol
⇒ nC2H5OH = x = 3,2 mol
⇒ mC2H5OH = 3,2.46 = 147,2 gam
⇒ VC2H5OH = m/D = 147,2/0,8 = 184 ml
⇒ Vdd = 184 + 216 = 400 ml
⇒ D = 184.100/400 = 46 độ
Bài 2: Lên men 1 lit ethyl alcohol 23 độ thu được giấm ăn. Biết hiệu suất lên men là 100% và khối lượng riêng của ethyl alcohol là 0,8 gam/ml. Khối lượng acetic acid trong giấm là bao nhiêu?
Lời giải:
Vruou= Độ rượu.Vdd = 0,23.1000 = 230 ml
⇒ mrượu = Vrượu.D = 230.0,8 = 184 gam
C2H5OH + O2 → CH3COOH + H2O
46 --------------------------------60
184 -------------------------→ m = ?
⇒ mCH3COOH = 184.60/46 = 240 gam
Cách giải bài tập Phản ứng tráng gương của glucose
Lý thuyết và Phương pháp giải
- Phương trình phản ứng:
C6H12O6 + Ag2O → C6H12O7 + 2Ag
Nhớ: 2nC6H12O6 = nAg
- Phương pháp chung:
+ Phân tích xem đề cho gì và hỏi gì
+ Tính n của chất mà đề cho. Tính số mol của chất đề hỏi ⇒ khối lượng của chất đề hỏi
Bài tập tự luyện
Bài 1: Đun nóng 250 gam dung dịch glucose với dung dịch AgNO3 /NH3 thu được 15 gam Ag, nồng độ của dung dịch glucose là bao nhiêu?
Lời giải:
nAg = 15/108 mol
C6H12O6 + Ag2O → C6H12O7 + 2Ag (1)
Theo pt (1) ta có nC6H12O6 = ½.nAg = ½.(15/108) = 0,07 mol
mctC6H12O6 =0,07 .180 = 12,5g
C% C6H12O6 = (12,5/250).100% = 5%
Bài 2: Để tráng bạc một chiếc gương soi, người ta phải đun nóng dung dịch chứa 36g glucose với lượng vừa đủ dung dịch AgNO3 trong amonia. Khối lượng bạc đã sinh ra bám vào mặt kính của gương và khối lượng AgNO3 cần dùng lần lượt là bao nhiêu (biết các phản ứng xảy ra hoàn toàn)
Lời giải:
nglucose = 36/180 = 0,2 mol
C6H12O6 + Ag2O → C6H12O7 + 2Ag
0,2 …………….. →………………0,4 mol
mAg = 0,4.108 = 43,2g
BTNT Ag ta có: nAgNO3 = nAg = 0,4 mol
mAgNO3 = 0,4.(108+14+16.3) = 68g
Cách giải bài tập Phản ứng lên men của glucose
Lý thuyết và Phương pháp giải
- Phương trình phản ứng:
C6H12O6 −to, men rượu→ 2C2H5OH + 2CO2
- Phương pháp chung:
+ Phân tích xem đề cho gì và hỏi gì
+ Tính n của chất mà đề cho. Tính số mol của chất đề hỏi ⇒ khối lượng của chất đề hỏi
Bài tập tự luyện
Bài 1: Lên men dung dịch chứa 300 gam glucose thu được 92 gam ethyl alcohol. Hiệu suất quá trình lên men tạo thành ethyl alcohol là bao nhiêu?
Lời giải:
netylic = 92/46 = 2 mol
C6H12O6 −to, men rượu→ 2C2H5OH + 2CO2
1…………………………….2 mol
Hiệu suất quá trình lên men tạo thành ethyl alcohol là :
H = (1.180/300) .100% =60%
Bài 2: Lên men hoàn toàn m gam glucose thành ethyl alcohol. Toàn bộ khí CO2 sinh ra trong quá trình này được hấp thụ hết vào dung dịch Ca(OH)2 dư tạo ra 40 gam kết tủa. Nếu hiệu suất của quá trình lên men là 75% thì giá trị của m là bao nhiêu?
Lời giải:
C6H12O6 −to, men rượu→ 2C2H5OH + 2CO2 (1)
CO2 + Ca(OH)2 → CaCO3 + H2O (2)
Ta có: nCaCO3 = nCO2 = 40/100 = 0,4 mol
Theo pt (1) ta có: nC6H12O6(ly thuyet) = (1/2).nCO2 = (1/2).0,4 = 0,2 mol
H = 75% ⇒ nC6H12O6(thuc te) = (0,2/75).100 = 0,267 mol
⇒ m = 0,267.180 = 48g
Thi online KHTN 9 KNTTThi online KHTN 9 CDThi online KHTN 9 CTST
Xem thêm cách giải các dạng bài tập Hóa học lớp 9 hay, chi tiết khác:
- Các dạng bài tập Các loại hợp chất vô cơ
- Các dạng bài tập Kim loại
- Các dạng bài tập Phi kim. Sơ lược về bảng tuần hoàn các nguyên tố hóa học
- Các dạng bài tập Hydrocarbon. Nhiên liệu
Xem thêm các loạt bài Để học tốt Hóa học 9 hay khác:
- Giải bài tập Hóa học 9
- Giải sách bài tập Hóa 9
- Đề thi Hóa học 9
- Wiki 200 Tính chất hóa học
- Wiki 3000 Phản ứng hóa học quan trọng
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Chuyên đề: Lý thuyết - Bài tập Hóa học lớp 9 có đáp án được biên soạn bám sát nội dung chương trình sgk Hóa học 9.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 9 Global Success
- Giải sgk Tiếng Anh 9 Smart World
- Giải sgk Tiếng Anh 9 Friends plus
- Lớp 9 Kết nối tri thức
- Soạn văn 9 (hay nhất) - KNTT
- Soạn văn 9 (ngắn nhất) - KNTT
- Giải sgk Toán 9 - KNTT
- Giải sgk Khoa học tự nhiên 9 - KNTT
- Giải sgk Lịch Sử 9 - KNTT
- Giải sgk Địa Lí 9 - KNTT
- Giải sgk Giáo dục công dân 9 - KNTT
- Giải sgk Tin học 9 - KNTT
- Giải sgk Công nghệ 9 - KNTT
- Giải sgk Hoạt động trải nghiệm 9 - KNTT
- Giải sgk Âm nhạc 9 - KNTT
- Giải sgk Mĩ thuật 9 - KNTT
- Lớp 9 Chân trời sáng tạo
- Soạn văn 9 (hay nhất) - CTST
- Soạn văn 9 (ngắn nhất) - CTST
- Giải sgk Toán 9 - CTST
- Giải sgk Khoa học tự nhiên 9 - CTST
- Giải sgk Lịch Sử 9 - CTST
- Giải sgk Địa Lí 9 - CTST
- Giải sgk Giáo dục công dân 9 - CTST
- Giải sgk Tin học 9 - CTST
- Giải sgk Công nghệ 9 - CTST
- Giải sgk Hoạt động trải nghiệm 9 - CTST
- Giải sgk Âm nhạc 9 - CTST
- Giải sgk Mĩ thuật 9 - CTST
- Lớp 9 Cánh diều
- Soạn văn 9 Cánh diều (hay nhất)
- Soạn văn 9 Cánh diều (ngắn nhất)
- Giải sgk Toán 9 - Cánh diều
- Giải sgk Khoa học tự nhiên 9 - Cánh diều
- Giải sgk Lịch Sử 9 - Cánh diều
- Giải sgk Địa Lí 9 - Cánh diều
- Giải sgk Giáo dục công dân 9 - Cánh diều
- Giải sgk Tin học 9 - Cánh diều
- Giải sgk Công nghệ 9 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 9 - Cánh diều
- Giải sgk Âm nhạc 9 - Cánh diều
- Giải sgk Mĩ thuật 9 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

