Đề luyện thi Hóa học tốt nghiệp THPT năm 2026 có đáp án (Đề 5)
Đề luyện thi Hóa học tốt nghiệp THPT năm 2026 có đáp án - Đề 5
Câu 1: Để điều chế Cu người ta tiến hành điện phân dung dịch CuCl2. Phát biểu nào sau đây là đúng
A. Ở anot xảy ra quá trình khử H2O
B. Ở catot xảy ra quá trình oxi hóa H2O
C. Ở catot xảy ra quá trình oxi hóa ion Cu2+
D. Ở anot xảy ra quá trình oxi hóa ion Cl-
Câu 2: Ứng dụng nào sau đây không phải của natri hidroxit
A. Nấu xà phòng
B. Chế phẩm nhuộm
. Luyện nhôm
D. Làm thuốc đau
Câu 3: Kim loại kiềm, kiềm thổ và nhôm có thể được điều chế bằng phương pháp nào sau đây
A. Điện phân nóng chảy
B. Thủy luyện
C. Nhiệt luyện
D. Điện phân dung dịch
Câu 4: Dung dich muối nào sau đây khi cho vào dung dịch HCl, đun nóng sẽ có phản ứng xảy ra
A. FeBr2
B. FeSO4
C. Fe(NO3)2
D. Fe(NO3)3
Câu 5: Phản ứng nào sau đây không đúng
A. 2Cr + 3Cl2 → 2CrCl3
B. Cr2O3 + 2NaOH → 2NaCrO2 + H2O
C. 2Cr + 6 HCl → 2CrCl3 + 3H2
D. 2NaCrO2 + 8NaOH + 3Cl2 → 2Na2CrO4 + 6 NaCl + 4H2O
Câu 6: Kim loại nào sau đây có tính nhiễm từ
A. Cu B. Fe C. Al D. Ag
Câu 7: Có 4 ống nghiệm đựng các dung dịch riêng biệt: Nh4Cl, NaNO3, (NH4)2CO3, Na2SO4. Chỉ dùng dung dịch Ba(OH)2 làm thuốc thử thì số dung dịch nhận biết được là
A. 1 B. 2 C. 3 D. 4
Câu 8: Trong các nguyên nhân sau đây
(1) Do hoạt động của núi lửa
(2) Do khí thải công nghiệp, khí thải sinh hoạt
(3) Do khí thải từ các phương tiện giao thông
(4) Do khí sinh ra từ quá trình quang hợp của cây xanh
(5) Do nồng độ cao của các ion kim loại: Pb2+; Hg2+; Mn2+; Cu2+ trong các nguồn nước
Những nguyên nhân gây ô nhiễm môi trường không khí là
A. 2, 3, 4
B. 1, 2, 3
C. 2, 3, 5
D. 1, 2, 4
Câu 9: Đặc điểm giống nhau giữa saccarozơ và glucozơ là
A. Có nhóm chức CHO trong phân tử
B. Tác dụng được với dung dịch AgNO3 trong NH3 dư
C. Bị thủy phân
D. Tác dụng được với Cu(OH)2 ở nhiệt độ thường
Câu 10: Đốt cháy hoàn toàn một amin đơn chức thì sản phẩm thu được có tỉ lệ mol nCO2 : nH2O = 8:9. Công thức phân tử của amin là
A. C4H11N B. C4H9N C. C3H9N D. C3H7N
Câu 11: Nhúng quỳ tím vào các dung dịch sau
(1) H2NCH2CH(NH2)COOH
(2) H2NCH2COONa
(3) ClH3NCH2COO
(4) HOOCCH2CH2CH(NH2)COOH
(5) NaOOCCH2CH2CH(NH2)COONa
Những dung dịch làm quỳ tím chuyển sang màu xanh là
A. 1, 2, 5
B. 1, 3, 5
C. 2, 3, 5
D. 1, 4, 5
Câu 12: Cho phát biểu sau
(a) Dùng phản ứng tráng bạc để phân biệt fructozơ và glucozơ
(b) Trong môi trường bazơ, fructozơ chuyển hóa thành glucozơ
(c) Trong dung dịch nước, glucozơ tồn tại chủ yếu ở dạng mạch hở
(d) Xenlulozơ và tinh bột là đồng phân của nhau
(e) Saccarozơ có tính chất của ancol đa chức và anđehit đơn chức
Trong các phát biểu trên, số phát biểu đúng là
A. 2 B. 1 C. 4 D. 3
Câu 13: Dẫn luồng khí CO dư đi 2,4g hỗn hợp CuO và Fe2O3 nung nóng đến khi phản ứng xảy ra hoàn toàn, thu được 1,76g chất rắn. Phần trăm khối lượng CuO có trong hỗn hợp ban đầu là
A. 55,28% B. 45,72% C. 66,67% D. 33,33%
Câu 14: Bốn kim loại Na, Al, Fe và Cu được ấn định không theo thứ tự X,Y , Z, T. Biết rằng
X;Y được điều chế bằng phương pháp điện phân nóng chảy
X đẩy được kim loại T ra khỏi dung dịch muối
Z tác dụng được với dung dịch H2SO4 đặc, nóng nhưng không tác dụng được với dung dịch H2SO4 đặc, nguội
X,Y, Z, T theo thứ tự là
A. Al, Na, Cu, Fe
B. Na, Al, Fe, Cu
C. Na, Fe, Al, Cu
D. Al, Na, Fe, Cu
Câu 15: Cho một mẫu nước cứng có chứa a mol Ca2+, b mol Mg2+ còn lại là ion HCO3-. Số mol Ca(OH)2 cần dùng để làm mất hoàn toàn tính cứng của mẫu nước trên là
A. a mol B. b mol C. (a+b) mol D. (a+2b) mol
Câu 16: Trộn 100ml dung dịch FeCl2 2M với 100ml dung dịch NaOH 2M. Lọc tách kết tủa đem nung trong không khí đến khối lượng không đổi thu được chất rắn có khối lượng là
A. 8g B. 7,2g C. 16g D. 14,4g
Câu 17: Ở nhiệt độ thích hợp Fe, Cu đều phản ứng với
A. Cl2; O2; dung dịch HNO3
B. O2; dung dịch HCl; dung dịch HNO3
C. S; Cl2; dung dịch H2SO4 loãng
D. O2; dung dich HCl; dung dịch H2SO4 loãng
Câu 18: Cho hỗn hợp X gồm CuO, Fe3O4 có số mol bằng nhau tác dụng hết với dung dịch HNO3, thu được hỗn hợp khí Y gồm 0,03 mol NO2 và 0,02 mol NO. Số mol của mỗi chất trong X là
A. 0,03 B. 0,06 C. 0,05 D. 0,09
Câu 19: Công thức nào sau đây không thể là công thức đơn giản của 1 este no, mạch hở
A. C5H8O2 B. C5H10O C. C5H9O2 D. C4H5O4
Câu 20: Sản phẩm của phản ứng thủy phân hoàn toàn chất béo (C17H33COO)3C3H5 trong dung dịch H2SO4 loãng là
A. C17H33(COOH)3 và C3H5OH
B. C17H33COOH và C3H5(OH)3
C. C17H35COOH và C3H5(OH)3
D. C17H33COOH và C3H5OH
Câu 21: Một peptit X mạch hở khi thủy phân hoàn toàn chỉ thu được glyxin và alanin với số mol bằng nhau. Khi đốt cháy 0,1 mol X thu được 16,2 g nước. Số nguyên tử oxi có trong 1 phân tử X là
A. 5 B. 4 C. 2 D. 3
Câu 22: Cho các polime sau: cao su lưu hóa, poli (vinyl clorua), thủy tinh hữu cơ, glicogen, polietilen, amilozơ, nhựa rezol. Số polime có cấu trúc mạch thẳng là
A. 6 B. 3 C. 4 D. 5
Câu 23: Phát biểu nào sau đây là đúng
A. Ancol etylic phản ứng được với dung dịch NaOH
B. Cả ba chất etilen, benzen và stiren đều tham gia phản ứng trùng hợp
C. Anilin là một bazơ mạnh
D. Để polime hóa cao su thiên nhiên được isopren
Câu 24: Dãy gồm các chất được sắp xếp theo thứ tự giảm dần lực bazơ từ trái sang phải là
A. Phenylamin, amoniac, metylamin
B. Metylamin, amoniac, phenylamin
C. Metylamin, phenylamin, amoniac
D. Phenylamin, metylamin, amoniac
Câu 25: Cho dung dịch X chứa x mol FeCl2 và x mol NaCl vào dung dịch chứa 4,8x mol AgNO3, thu được 64,62g kết tủa và dung dịch Y. Khối lượng chất tan có trong dung dịch Y là
A. 38,604g B. 40,439g C. 55,56g D. 56,412g
Câu 26: Nhỏ từ từ 3V ml dung dịch Ba(OH)2(dung dịch X) vào V ml dung dịch Al2(SO4)3 (dung dịch Y) thì phản ứng vừa đủ thu được kết tủa lớn nhất có khối lượng m1 g. Nếu trộn V ml dung dịch X vào V ml dung dịch Y, thu được m2g kết tủa. tỉ lệ m1/m2 là
A. 1,37 B. 2,2 C. 3 D. 1,65
Câu 27: Tiến hành phản ứng nhiệt nhôm hỗn hợp gồm Al và Cr2O3 trong khí quyển trơ. Sau một thời gian thu được 21,95g hỗn hợp X. Chia X thành hai phần bằng nhau. Phần (1) cho phản ứng với dung dịch HCl loãng, nóng (dư) thu được 3,36l H2(dktc). Phần (2) cho phản ứng với dung dịch NaOH đặc, nóng (dư) thu được 1,68 lít H2(đktc). Hiệu suất phản ứng nhiệt nhôm là
A. 75% B. 60% C. 25% D. 40%
Câu 28: Cho hỗn hợp kim loại Mg, Al, Fe vào dung dịch AgNO3,Cu(NO3)2 và HNO3. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch X gồm 3 muối và chất rắn Y gồm ba kim loại. Ba muối trong X là
A. Mg(NO3)2, Al(NO3)3, Fe(NO3)2
B. Mg(NO3)2, Al(NO3)3, Cu(NO3)2
C. Mg(NO3)2, Fe(NO3)3, AgNO3
D. Mg(NO3)2, Al(NO3)3, Fe(NO3)3
Câu 29: Điện phân một dung dịch gồm NaCl và CuSO4 có cùng số mol đến khi ở catot xuất hiện bọt khí thì dừng điện phân. Trong cả quá trình điện phân trên, sản phẩm thu được ở anot là
A. Khí Cl2 và H2
B. Khí Cl2 và O2
C. Chỉ có khí Cl2
D. Khí H2 và O2
Câu 30: Đốt cháy hoàn toàn a mol chất X là este của glixerol với 3 axit cacboxylic đơn chức thu được b mol CO2 và c mol H2O. biết b – c =4a. Hidro hóa hoàn toàn m gam X cần 5,6 lít khí H2 thu được 32g Y. Nếu đun m gam X với dung dịch NaOH vừa đủ thì khối lượng muối khan thu được là
A. 35,5g B. 39,6g C. 40,6g D. 35g
Câu 31: Peptit X được cấu tạo bởi 1 amino axit trong phân tử chỉ chứa 1 nhóm –COOH và 1 nhóm –CH2. Thủy phân hòan toàn 0,1 mol X trong dung dịch NaOH (lấy dư 20% so với lượng phản ứng), cô cạn dung dịch sau phản ứng thu được 168g chất rắn khan. Số liên kết peptit trong phân tử X là
A. 17 B. 14 C. 15 D. 16
Câu 32: Este X có công thức phân tử C4H8O2. Cho X tác dụng với NaOH đun nóng thu được muối Y và ancol Z. Oxi hóa Z bằng CuO thu được chất hữu cơ Z1 . Khi cho 1 mol Z1 tác dụng với AgNO3 trong dung dịch NH3 thì thu được tối đa 4 mol Ag. Tên gọi đúng của X là
A. Etyl axetat
B. N-propyl fomat
C. Isopropyl fomat
D. Metyl propionat
Câu 33: Ứng với công thức phân tử C3H9O2N có bao nhiêu chất vừa phản ứung được với dung dịch NaOH, vừa phản ứng được với dung dịch HCl
A. 2 B. 4 C. 1 D. 3
Câu 34: Cho các polime: (1) poli (vinyl clorua), (2) poli (metyl metacrylat), (3) poliisopren (4) policaproamit, (5) poli (vinyl axetat) và (6) tơ nilon 6-6. Trong các polime lên, số polime có thể bị thủy phân trong dung dịch axit và dung dịch kiềm là
A. 2 B. 4 C. 5 D. 3
Câu 35: Hỗn hợp X gồm :HCHO, CH3COOH, HCOOCH3, CH3Ch(OH)COOH. Đốt cháy hoàn toàn hỗn hợp X cần V lít O2(dktc) sau phản ứng thu được CO2 và H2O. Hấp thụ hết sản phẩm chảy vào nước vôi trong dư thu được 50g kết tủa. Giá trị của V là
A. 16,8 B. 8,4 C. 11,2 D. 7,84
Câu 36: Cho hỗn hợp X gồm clo và oxi tác dụng vừa hết với 1,92g Mg và 4,48 Fe tạo ra hỗn hợp Y gồm muối clorua và oxit. Hòa tan hoàn toàn Y cần 120ml dung dịch HCl 2M, thu được dung dịch Z. Cho AgNO3 dư vào Z thu được 56,69g kết tủa. Phần trăm theo thể tích khí Cl2 trong X là
A. 51,72% B. 53,85% C. 76,7% D. 56,36%
Câu 37: Hỗn hợp X gồm FeO, Fe2O3, S,FeS2 và CuS (oxi chiếm 16% khối lượng). Cho 10 g X tác dụng vừa đủ với dung dịch chứa 0,325 mol H2SO4 thu được dung dịch Y gồm Fe3+, Cu2+và SO42- và khí SO2 thoát ra. Nhúng thanh Mg vào Y, sau khi các phản ứng xảy ra hoàn toàn lấy thanh Mg ra làm khô và cân thấy khối lượng tăng 3g . Mặt khác đốt cháy hoàn toàn 10g X cần V lít khí O2. Giá trị của V là
A. 1,68 B. 1,484 C. 0,924 D. 1,316
Câu 38: Cho 9,36g hỗn hợp X gồm 3 amino axit vào dung dịch chứa 0,1 mol axit malonic, thu được dung dịch X. Thêm tiếp 400ml dung dịch KOH 1M vào dung dịch X, sau khi các phản ứung xảy ra hoàn toàn, cô cạn dung dịch sau phản ứng thu được 36,76g chất rắn khan Y. Hòa tan Y trong dung dịch HCl (dư) thu được chứa m gam muối. Giá trị của m là
A. 13,01 B. 42,81 C. 39,16 D. 46,46
Câu 39: X và Y là 2 hợp chất hữu cơ, mạch hở hơn nhau một nguyên tử cacbon MX > MY. Đốt cháy hoàn toàn 0,34 mol hỗn hợp E gồm X và Y bằng O2 rồi cho toàn bộ sản phẩm thu được (chỉ gồm CO2 và H2O) hấp thụ hết vào một dung dịch cứa 0,3 mol Ba(OH)2 và 0,1 mol NaOH sau phản ứng thu được 39,4 g kết tủa. Để tác dụng hết với 0,34g hỗn hợp E cần vừa đủ 0,5 mol KOH. Phần trăm khối lượng của Y trong hỗn hợp E là
A. 31,34% B. 38,16% C. 34,38% D. 36,51%
Câu 40: Khử hoàn toàn 32g CuO bằng khí CO dư thu được m gam kim loại. Giá trị m là
A. 25,6 B. 19,2 C. 6,4 D. 12,8
Đáp án:
| Câu | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| Đáp án | D | D | A | C | C | B | D | B | D | B |
| Câu | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| Đáp án | A | B | D | D | D | A | A | D | A | B |
| Câu | 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 | 30 |
| Đáp án | A | D | D | B | C | C | A | A | A | B |
| Câu | 31 | 32 | 33 | 34 | 35 | 36 | 37 | 38 | 39 | 40 |
| Đáp án | D | C | D | B | B | C | B | A | B | A |
Hướng dẫn giải
Câu 32:

Câu 36:
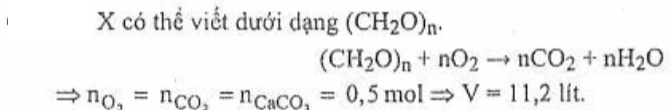
Câu 38:

Câu 39:

Câu 40:

Tham khảo thêm các Đề thi trắc nghiệm môn Hóa học khác:
- Đề luyện thi Hóa học tốt nghiệp THPT năm 2026 có đáp án - Đề 3
- Đề luyện thi Hóa học tốt nghiệp THPT năm 2026 có đáp án - Đề 4
- Đề luyện thi Hóa học tốt nghiệp THPT năm 2026 có đáp án - Đề 5
- Đề luyện thi Hóa học tốt nghiệp THPT năm 2026 có đáp án - Đề 6
- Đề luyện thi Hóa học tốt nghiệp THPT năm 2026 có đáp án - Đề 7
Sách VietJack thi THPT quốc gia 2025 cho học sinh 2k7:
- Giải Tiếng Anh 12 Global Success
- Giải sgk Tiếng Anh 12 Smart World
- Giải sgk Tiếng Anh 12 Friends Global
- Lớp 12 Kết nối tri thức
- Soạn văn 12 (hay nhất) - KNTT
- Soạn văn 12 (ngắn nhất) - KNTT
- Giải sgk Toán 12 - KNTT
- Giải sgk Vật Lí 12 - KNTT
- Giải sgk Hóa học 12 - KNTT
- Giải sgk Sinh học 12 - KNTT
- Giải sgk Lịch Sử 12 - KNTT
- Giải sgk Địa Lí 12 - KNTT
- Giải sgk Giáo dục KTPL 12 - KNTT
- Giải sgk Tin học 12 - KNTT
- Giải sgk Công nghệ 12 - KNTT
- Giải sgk Hoạt động trải nghiệm 12 - KNTT
- Giải sgk Giáo dục quốc phòng 12 - KNTT
- Giải sgk Âm nhạc 12 - KNTT
- Giải sgk Mĩ thuật 12 - KNTT
- Lớp 12 Chân trời sáng tạo
- Soạn văn 12 (hay nhất) - CTST
- Soạn văn 12 (ngắn nhất) - CTST
- Giải sgk Toán 12 - CTST
- Giải sgk Vật Lí 12 - CTST
- Giải sgk Hóa học 12 - CTST
- Giải sgk Sinh học 12 - CTST
- Giải sgk Lịch Sử 12 - CTST
- Giải sgk Địa Lí 12 - CTST
- Giải sgk Giáo dục KTPL 12 - CTST
- Giải sgk Tin học 12 - CTST
- Giải sgk Hoạt động trải nghiệm 12 - CTST
- Giải sgk Âm nhạc 12 - CTST
- Lớp 12 Cánh diều
- Soạn văn 12 Cánh diều (hay nhất)
- Soạn văn 12 Cánh diều (ngắn nhất)
- Giải sgk Toán 12 Cánh diều
- Giải sgk Vật Lí 12 - Cánh diều
- Giải sgk Hóa học 12 - Cánh diều
- Giải sgk Sinh học 12 - Cánh diều
- Giải sgk Lịch Sử 12 - Cánh diều
- Giải sgk Địa Lí 12 - Cánh diều
- Giải sgk Giáo dục KTPL 12 - Cánh diều
- Giải sgk Tin học 12 - Cánh diều
- Giải sgk Công nghệ 12 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 12 - Cánh diều
- Giải sgk Giáo dục quốc phòng 12 - Cánh diều
- Giải sgk Âm nhạc 12 - Cánh diều








 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp



