Giải SBT Hóa học 10 trang 42 Chân trời sáng tạo
Với Giải SBT Hóa học 10 trang 42 trong Ôn tập chương 3 Sách bài tập Hóa 10 Chân trời sáng tạo hay nhất, chi tiết sẽ giúp học sinh dễ dàng làm bài tập trong SBT Hóa 10 trang 42.
Giải SBT Hóa học 10 trang 42 Chân trời sáng tạo
Bài OT 3.1 trang 42 SBT Hóa học 10: Ion nào sau đây có cấu hình electron của khí hiếm helium?
A. Mg2+
B. O2-
C. Na+
D. Li+
Lời giải:
Đáp án đúng là: D
Ion Li3+ có cấu hình electron của khí hiếm helium.
Bài OT 3.2 trang 42 SBT Hóa học 10: Trong sự hình thành phân tử lithium fluoride (LiF), ion lithium và ion fluoride đã lần lượt đạt được cấu hình electron bền của các khí hiếm nào?
A. Helium và neon
B. Helium và argon
C. Neon và argon
D. Cùng là neon
Lời giải:
Đáp án đúng là: A
Li (Z = 3) có 1 electron ở lớp ngoài cùng, có xu hướng nhường 1 electron để đạt cấu hình electron bền vững của khí hiếm helium.
F (Z = 9) có 7 electron ở lớp ngoài cùng, có xu hướng nhận 1 electron để đạt cấu hình electron bền vững của khí hiếm neon.
Bài OT 3.3 trang 42 SBT Hóa học 10: Không cần sử dụng hiệu độ âm điện, có bao nhiêu phân tử trong số các phân tử sau có liên kết ion BaCl2, CS2, Na2O và HI?
A. 3
B. 2
C. 4
D. 1
Lời giải:
Đáp án đúng là: B
Phân tử BaCl2 và Na2O có sự liên kết giữa kim loại điển hình và phi kim điển hình nên chúng có liên kết ion.
Bài OT 3.4 trang 42 SBT Hóa học 10: Tổng số các phân tử có cực trong số các phân tử sau: Cl2, O2, CCl4, CO2 và SO2 là bao nhiêu?
A. 1
B. 2
C. 4
D. 3
Lời giải:
Đáp án đúng là: A
Trong số các phân tử Cl2, O2, CCl4, CO2 và SO2, các phân tử Cl2 và O2 không hình thành moment lưỡng cực, còn phân tử CCl4 có dạng tứ diện đều và phân tử CO2 có dạng đường thẳng nên phân tử CCl4 và CO2 có tổng các moment lưỡng cực bằng 0.
Vậy các phân tử Cl2, O2, CCl4, CO2 đều là các phân tử không cực.
Phân tử SO2 có dạng góc nên là phân tử có cực.
Bài OT 3.5 trang 42 SBT Hóa học 10: Phân tử sodium fluoride (NaF) và magnesium oxide (MgO) có cùng 20 electron và khoảng cách giữa các hạt nhân là tương tự nhau (235 pm và 215 pm). Giải thích tại sao nhiệt độ nóng chảy của NaF và MgO lại chênh lệch nhiều (992oC so với 2642oC).
Lời giải:
Phân tử NaF và MgO có cùng 20 electron và khoảng cách giữa các hạt nhân là tương tự nhau (235pm và 215pm), tuy nhiên nhiệt độ nóng chảy của MgO cao hơn nhiều so với NaF, đó là do các ion magnesium và oxide mang điện tích lần lượt là +2 và -2 nên có lực hút tĩnh điện mạnh hơn nhiều so với các ion sodium và fluoride chỉ mang điện tích lần lượt là +1 và -1.
Bài OT 3.6 trang 42 SBT Hóa học 10: Lithium fluoride (LiF) và sodium chloride (NaCl) đều là các hợp chất ion. Dự đoán nhiệt độ sôi và nhiệt độ nóng chảy của chất nào cao hơn. Giải thích.
Lời giải:
Lực hút tĩnh điện mạnh giữa các ion âm và ion dương làm cho LiF và NaCl đều có nhiệt độ nóng chảy và nhiệt độ sôi cao. Do các ion lithium và sodium đều mang điện tích +1, các ion fluoride và chloride đều mang điện tích -1 nên lực hút tĩnh điện ở đây phụ thuộc vào khoảng cách ion giữa các phân tử. Nếu các ion càng nhỏ, chúng càng gần nhau hơn dẫn đến lực hút tĩnh điện lớn hơn.
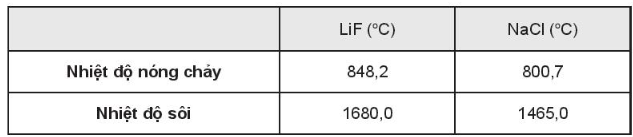
Do kích thước của ion Na+ lớn hơn ion Li+, kích thước ion Cl- lớn hơn ion F- nên lực hút tĩnh điện giữa các ion trong phân tử LiF lớn hơn trong phân tử NaCl làm nhiệt độ sôi và nhiệt độ nóng chảy của LiF cao hơn NaCl.
Bảng số liệu tham khảo:
Bài OT 3.7 trang 42 SBT Hóa học 10: Sodium peroxide (Na2O2) là một chất rắn màu vàng, thu được khi đốt sodium trong khí oxygen dư. Sodium peroxide được dùng để tẩy trắng gỗ, bột giấy, … Nêu rõ bản chất hóa học giữa các nguyên tử (hoặc nhóm nguyên tử) trong phân tử Na2O2.
Lời giải:
Công thức của Na2O2:
Trong phân tử Na2O2, liên kết giữa hai nguyên tử oxygen là liên kết cộng hóa trị không phân cực. Ngoài ra, mỗi nguyên tử sodium nhường 1 electron cho mỗi nguyên tử oxygen, hình thành nên các ion và Na+, những ion này hút nhau bằng lực hút tĩnh điện tạo nên phân tử Na2O2.
+ 2Na+ → 2Na2O2.
Bài OT 3.8 trang 42 SBT Hóa học 10: Liên kết hydrogen có phải là sự xen phủ giữa các orbital? Giải thích và cho ví dụ minh họa.
Lời giải:
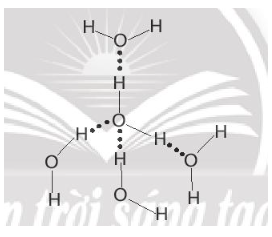
Liên kết hydrogen không phải là sự xen phủ giữa các AO, mà chỉ là lực hút tĩnh điện giữa nguyên tử hydrogen mang một phần điện tích dương đã liên kết với một nguyên tử có độ âm điện lớn (thường là N, O, F) với một nguyên tử có độ âm điện lớn khác (thường là N, O, F).
Ví dụ liên kết hydrogen giữa các phân tử nước:
Lời giải SBT Hóa 10 Ôn tập chương 3 hay khác:
Xem thêm lời giải sách bài tập Hóa học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Xem thêm các tài liệu học tốt lớp 10 hay khác:
- Giải sgk Hóa học 10 Chân trời sáng tạo
- Giải Chuyên đề Hóa học 10 Chân trời sáng tạo
- Giải SBT Hóa học 10 Chân trời sáng tạo
- Giải lớp 10 Chân trời sáng tạo (các môn học)
- Giải lớp 10 Kết nối tri thức (các môn học)
- Giải lớp 10 Cánh diều (các môn học)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Soạn văn 10 (hay nhất) - CTST
- Soạn văn 10 (ngắn nhất) - CTST
- Soạn văn 10 (siêu ngắn) - CTST
- Giải Toán 10 - CTST
- Giải Tiếng Anh 10 Global Success
- Giải Tiếng Anh 10 Friends Global
- Giải sgk Tiếng Anh 10 iLearn Smart World
- Giải sgk Tiếng Anh 10 Explore New Worlds
- Giải sgk Vật lí 10 - CTST
- Giải sgk Hóa học 10 - CTST
- Giải sgk Sinh học 10 - CTST
- Giải sgk Địa lí 10 - CTST
- Giải sgk Lịch sử 10 - CTST
- Giải sgk Kinh tế và Pháp luật 10 - CTST
- Giải sgk Hoạt động trải nghiệm 10 - CTST







 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

