50 câu trắc nghiệm Phản ứng oxi hóa, khử có lời giải (cơ bản - phần 2)
Với 50 câu trắc nghiệm Phản ứng oxi hóa, khử (cơ bản - phần 2) có lời giải chi tiết sẽ giúp học sinh ôn tập, biết cách làm câu trắc nghiệm Phản ứng oxi hóa, khử (cơ bản - phần 2).
50 câu trắc nghiệm Phản ứng oxi hóa, khử có lời giải (cơ bản - phần 2)
Thi online Hóa 10 KNTTThi online Hóa 10 CDThi online Hóa 10 CTST
Bài 1: Cho sơ đồ phản ứng: Fe(OH)2 + HNO3 → Fe(NO3)3 + NO + H2O. Sau khi cân bằng, hệ số của các chất tương ứng là
A. 3, 10, 3, 1, 8. B. 3, 28, 9, 1, 14.
C. 3, 26, 9, 2, 13. D. 2, 28, 6, 1, 14.
Lời giải:
Đáp án A
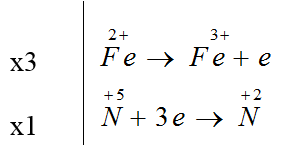
3Fe(OH)2 + 10HNO3 → 3Fe(NO3)3 + NO + 8H2O
Bài 2: Hòa tan hoàn toàn 2,4 gam kim loại Mg vào dung dịch HNO3 loãng, giả sử chỉ thu được V lít khí N2 là sản phẩm khử duy nhất (đktc). Giá trị của V là :
A. 0,672 lít. B. 6,72 lít. C. 0,448 lít. D. 4,48 lít.
Lời giải:
Đáp án C.
nMg = 0,1 (mol)
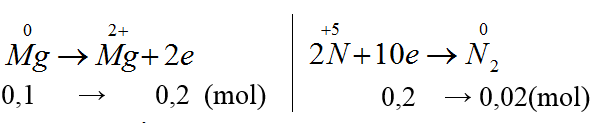
VN2 = 0,02.22,4 = 4,48 l
Bài 3: Phản ứng nào sau đây là phản ứng thế?
A. 4S + 8NaOH → Na2SO4 + 3Na2S + 4H2O
B. Fe + CuSO4 → FeSO4 + Cu.
C. 3Zn + 8HNO3 → 3Zn(NO3)2 + 2NO + 4H2O
D. Fe(NO3)2 + AgNO3 → Fe(NO3)3 + Ag
Lời giải:
Đáp án B.
Phản ứng thế là phản ứng hóa học trong đó nguyên tử của đơn chất thay thế nguyên tử của một nguyên tố khác trong hợp chất.
Bài 4: Phản ứng nào sau đây là phản ứng trao đổi?
A. SO3 + H2O → H2SO4 B. 2Cu(NO3)2 → 2CuO + 4NO2 + O2
C. CO2 + C → 2CO D. H2S + CuCl2 → CuS + 2HCl
Lời giải:
Đáp án D.
Bài 5: Cho phản ứng:
aFe + bHNO3 → cFe(NO3)3 + dNO + eH2O
Các hệ số a,b, c, d, e là những số nguyên, đơn giản nhất. Tổng (a + b) bằng:
A. 4. B. 3. C. 6. D. 5.
Lời giải:
Đáp án D
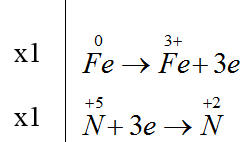
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
Tổng (a + b) bằng = 1+4 = 5
Bài 6: Nitơ trong chất nào sau đây vừa có tính oxi hoá, vừa có tính khử?
A. NH4Cl. B. NH3. C. N2. D. HNO3.
Lời giải:
Đáp án C.
Bài 7: Cho phản ứng: Mg + H2SO4 → MgSO4 + H2S + H2O
Khi hệ số cân bằng phản ứng là nguyên và tối giản thì số phân tử H2O tạo thành là:
A. 3. B. 10. C. 5. D. 4.
Lời giải:
Đáp án D.
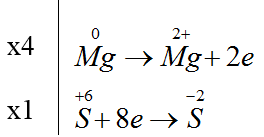
4Mg + 5H2SO4 → 4MgSO4 + H2S + 4H2O
Bài 8: Phản ứng nào sau đây là phản ứng oxi hóa – khử?
A. NH3 + HCl → NH4Cl B. H2S + 2NaOH → Na2S + 2H2O
C. 4NH3 + 3O2 → 2N2 + 6H2O D. H2SO4 + BaCl2 → BaSO4 ↓ + 2HCl
Lời giải:
Đáp án C.
Sự thay đổi số oxi hóa của các chất:
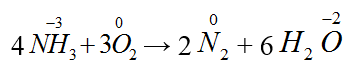
Bài 9: Trong phản ứng: CaCO3 → CaO + CO2, nguyên tố cacbon
A. chỉ bị oxi hóa. B. chỉ bị khử.
C. vừa bị oxi hóa, vừa bị khử. D. không bị oxi hóa, cũng không bị khử
Lời giải:
Đáp án D.
Số oxi hóa của C trước và sau phản ứng không thay đổi.
Bài 10: Cho phản ứng hoá học sau: Al + HNO3 → Al(NO3)3 + NH4NO3 + H2O
Hệ số cân bằng của các chất trong sản phẩm lần lượt là:
A. 8, 3, 15. B. 8, 3, 9. C. 2, 2, 5. D. 2, 1, 4.
Lời giải:
Đáp án B
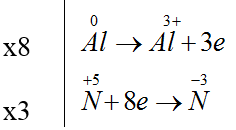
8Al + 30HNO3 → 8Al(NO3)3 + 3NH4NO3 + 9H2O
Bài 11: Mg có thể khử được axit HNO3 thành khí N2 theo phản ứng hoá học:
aMg + bHNO3 → cMg(NO3)2 + dN2 + eH2O
Tỉ lệ a:b là
A. 1:3. B. 5:12. C. 3:8. D. 4:15.
Lời giải:
Đáp án B.
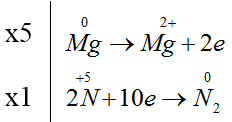
5Mg + 12HNO3 → 5Mg(NO3)2 + N2 + 6H2O
Bài 12: Chất nào sau đây trong các phản ứng chỉ đóng vai trò là chất oxi hóa?
A. S B. F2 C. Cl2 D. N2
Lời giải:
Đáp án B.
F2 là nguyên tố có độ âm điện lớn nhất trong bảng tuần hoàn, là phi kim mạnh nhất.
Bài 13: Số oxi hóa của oxi trong các hợp chất HNO3, H2O2, F2O, KO2 theo thứ tự là
A. -2, -1, -2, -0,5. B. -2, -1, +2, -0, 5.
C. -2, +1, +2, +0,5. D. -2, +1, -2, +0,5.
Lời giải:
Đáp án B.
Bài 14: Trong phản ứng oxi hóa – khử, chất bị oxi hóa là
A. chất nhận electron. B. chất nhường electron.
C. chất làm giảm số oxi hóa. D. chất không thay đổi số oxi hóa.
Lời giải:
Đáp án B
Chất bị oxi hóa (chất khử) là chất nhường electron và có sự tăng số oxi hóa.
Bài 15: Cho phản ứng: Ca +Cl2 → CaCl2. Kết luận nào sau đây đúng
A. Mỗi nguyên tử Ca nhận 2e. B. Mỗi nguyên tử Cl nhận 2e.
C. Mỗi phân tử Cl2 nhường 2e. D. Mỗi nguyên tử Ca nhường 2e.
Lời giải:
Đáp án D.
Bài 16: Oxit nào sau đây bị oxi hoá khi phản ứng với dung dịch HNO3 loãng?
A. MgO. B. Fe2O3. C. FeO. D. Al2O3.
Lời giải:
Đáp án C.
Trong đáp án A,B,D các kim loại đều đã có số oxi hóa cao nhất. Không bị oxi hóa bởi HNO3.
Bài 17: Phản ứng nào dưới đây không phải phản ứng oxi hoá - khử?
A. 2NaOH + 2NO2 to→ NaNO2 + NaNO3 + H2O
B. 2KMnO4 to→ K2MnO4 + MnO2 + O2
C. 2Fe(OH)3 to→ Fe2O3 + 3H2O
D. 4Fe(OH)2 + O2 to→ 2Fe2O3 + 4H2O
Lời giải:
Đáp án C.
Trong phản ứng, không xảy ra sự thay đổi số oxi hóa của các nguyên tố.
Bài 18: Phản ứng nào sau đây lưu huỳnh đóng vai trò là chất oxi hoá?
A. S+ O2 to→ SO2
B. S+ Na to→ Na2S
C. S+ H2SO4 → 3SO2 + 2H2O
D. S+ 6HNO3 to→ H2SO4 + 6NO2 + 2H2O
Lời giải:
Đáp án B.
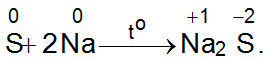
Bài 19: Chất hoặc ion nào sau đây có cả tính khử và tính oxi hoá?
A. SO2. B. F2. C. Al3+. D. Na.
Lời giải:
Đáp án A.
Bài 20: Lưu huỳnh trong chất nào sau đây vừa có tính oxi hoá vừa có tính khử?
A. Na2SO4. B. SO2. C. H2S. D. H2SO4.
Lời giải:
Đáp án B.
Trong SO2, số oxi hóa của S là +4, có khả năng tăng lên +6, thể hiện tính khử, hay giảm xuống -2 thể hiện tính oxi hóa.
Bài 21: Trong phản ứng: NO2 + H2O → HNO3 + NO, nguyên tố nitơ
A. chỉ bị oxi hóa. B. chỉ bị khử.
C. vừa bị oxi hóa, vừa bị khử. D. không bị oxi hóa, cũng không bị khử.
Lời giải:
Đáp án C.
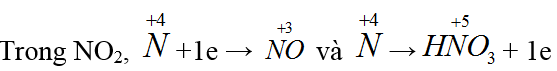
Bài 22: Trong phản ứng: Cu + 2H2SO4 (đặc, nóng) → CuSO4 + SO2 + 2H2O, axit sunfuric
A. là chất oxi hóa. B. vừa là chất oxi hóa, vừa là chất tạo môi trường.
C. là chất khử. D. vừa là chất khử, vừa là chất tạo môi trường.
Lời giải:
Đáp án B.
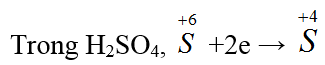
Bài 23: Trong phản ứng oxi hóa – khử, chất oxi hóa là
A. chất nhận electron. B. chất nhường electron.
C. chất làm tăng số oxi hóa. D. chất không thay đổi số oxi hóa.
Lời giải:
Đáp án A.
Chất oxi hóa là chất nhận electron và có sự giảm số oxi hóa.
Bài 24: Cho phương trình hoá học của phản ứng: 2Cr + 3Sn2+ → 2Cr3+ + 3Sn
Nhận xét nào sau đây về phản ứng trên là đúng?
A. Cr là chất oxi hoá, Sn2+ là chất khử.
B. Sn2+ là chất khử, Cr3+ là chất oxi hoá.
C. Cr là chất khử, Sn2+ là chất oxi hoá.
D. Cr3+ là chất khử, Sn2+ là chất oxi hoá.
Lời giải:
Đáp án C.
Cr có sự tăng số oxi hóa : chất khử, Sn2+ có sự giảm số oxi hóa : chất oxi hóa.
Bài 25: Cho phản ứng hoá học: Br2 + 5Cl2 + 6H2O ⇔ 2HBrO3 + 10HCl
Câu nào sau đây diễn tả đúng tính chất của các chất phản ứng?
A. Br2 là chất oxi hoá, Cl2 là chất khử.
B. Br2 là chất oxi hoá, H2O là chất khử.
C. Br2 là chất khử, Cl2 là chất oxi hoá.
D. Cl2 là chất oxi hoá, H2O là chất khử.
Lời giải:
Đáp án C.
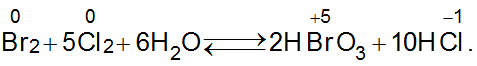
Br2 tăng số oxi hóa: chất khử, Cl2 giảm số oxi hóa: chất oxi hóa.
Thi online Hóa 10 KNTTThi online Hóa 10 CDThi online Hóa 10 CTST
Xem thêm các dạng bài tập Hóa học lớp 10 có trong đề thi Tốt nghiệp THPT khác:
- 50 câu trắc nghiệm Phản ứng oxi hóa, khử có lời giải (cơ bản - phần 1)
- 50 câu trắc nghiệm Phản ứng oxi hóa, khử có lời giải (nâng cao - phần 1)
- 50 câu trắc nghiệm Phản ứng oxi hóa, khử có lời giải (nâng cao - phần 2)
Để học tốt lớp 10 các môn học sách mới:
- Giải bài tập Lớp 10 Kết nối tri thức
- Giải bài tập Lớp 10 Chân trời sáng tạo
- Giải bài tập Lớp 10 Cánh diều
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 10 Global Success
- Giải Tiếng Anh 10 Friends Global
- Giải sgk Tiếng Anh 10 iLearn Smart World
- Giải sgk Tiếng Anh 10 Explore New Worlds
- Lớp 10 - Kết nối tri thức
- Soạn văn 10 (hay nhất) - KNTT
- Soạn văn 10 (ngắn nhất) - KNTT
- Soạn văn 10 (siêu ngắn) - KNTT
- Giải sgk Toán 10 - KNTT
- Giải sgk Vật lí 10 - KNTT
- Giải sgk Hóa học 10 - KNTT
- Giải sgk Sinh học 10 - KNTT
- Giải sgk Địa lí 10 - KNTT
- Giải sgk Lịch sử 10 - KNTT
- Giải sgk Kinh tế và Pháp luật 10 - KNTT
- Giải sgk Tin học 10 - KNTT
- Giải sgk Công nghệ 10 - KNTT
- Giải sgk Hoạt động trải nghiệm 10 - KNTT
- Giải sgk Giáo dục quốc phòng 10 - KNTT
- Lớp 10 - Chân trời sáng tạo
- Soạn văn 10 (hay nhất) - CTST
- Soạn văn 10 (ngắn nhất) - CTST
- Soạn văn 10 (siêu ngắn) - CTST
- Giải Toán 10 - CTST
- Giải sgk Vật lí 10 - CTST
- Giải sgk Hóa học 10 - CTST
- Giải sgk Sinh học 10 - CTST
- Giải sgk Địa lí 10 - CTST
- Giải sgk Lịch sử 10 - CTST
- Giải sgk Kinh tế và Pháp luật 10 - CTST
- Giải sgk Hoạt động trải nghiệm 10 - CTST
- Lớp 10 - Cánh diều
- Soạn văn 10 (hay nhất) - Cánh diều
- Soạn văn 10 (ngắn nhất) - Cánh diều
- Soạn văn 10 (siêu ngắn) - Cánh diều
- Giải sgk Toán 10 - Cánh diều
- Giải sgk Vật lí 10 - Cánh diều
- Giải sgk Hóa học 10 - Cánh diều
- Giải sgk Sinh học 10 - Cánh diều
- Giải sgk Địa lí 10 - Cánh diều
- Giải sgk Lịch sử 10 - Cánh diều
- Giải sgk Kinh tế và Pháp luật 10 - Cánh diều
- Giải sgk Tin học 10 - Cánh diều
- Giải sgk Công nghệ 10 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 10 - Cánh diều
- Giải sgk Giáo dục quốc phòng 10 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

