30 Bài tập về Clo cực hay, có lời giải
Với 30 Bài tập về Clo cực có lời giải chi tiết sẽ giúp học sinh ôn tập, biết cách làm Bài tập về Clo cực.
30 Bài tập về Clo cực hay, có lời giải
Thi online Hóa 10 KNTTThi online Hóa 10 CDThi online Hóa 10 CTST
Câu 1: Vị trí của Cl (z = 17) trong bảng tuần hoàn là
A. ô 17, chu kỳ 3, nhóm VIIA.
B. ô 17, chu kỳ 3, nhóm VA.
C. ô 17, chu kỳ 4, nhóm VIIA.
D. ô 17, chu kỳ 4, nhóm VA.
Lời giải:
Đáp án A
Cấu hình electron của Cl: 1s22s22p63s23p5.
Cl thuộc ô 17 (do z = 17), chu kỳ 3 (do có 3 lớp e), nhóm VIIA (do 7e lớp ngoài cùng, nguyên tố p).
Câu 2: Cho một luồng khí clo dư tác dụng với 9,2 gam kim loại sinh ra 23,4 gam muối kim loại M hoá trị I. Muối kim loại hoá trị I là muối nào sau đây?
A. NaCl. B. KCl.
C. LiCl. D. Kết quả khác
Lời giải:
Đáp án A
2M + Cl2 → 2MCl
Ta có:
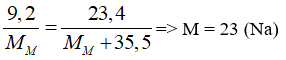
Vậy muối là NaCl.
Câu 3: Hòa tan khí Cl2 vào dung dịch KOH đặc, nóng, dư thu được dung dịch chứa các chất thuộc dãy nào sau đây?
A. KCl, KClO3, Cl2 B. KCl, KClO, KOH
C. KCl, KClO3, KOH D. KCl, KClO3
Lời giải:
Đáp án C
3Cl2 + 6KOH -to→ 5KCl + KClO3 + 3H2O
Câu 4: Để điều chế clo, người ta có thể làm như sau:
A. Điện phân muối NaCl nóng chảy hoặc dung dịch NaCl bão hòa có màng ngăn.
B. Cho KMnO4 hoặc MnO2 tác dụng với dung dịch HCl đặc.
C. Cho KClO3 tác dụng với dung dịch HCl đặc.
D. A hoặc B hoặc C.
Lời giải:
Đáp án D.
2NaCl + 2H2O
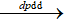
2NaCl
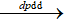
MnO2 + 4HCl → MnCl2 + 2H2O + Cl2
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 8H2O + 5Cl2
KClO3 + 6HCl → KCl + 3H2O + 3Cl2
Câu 5: Cho 17,4 gam MnO2 tác dụng với dd HCl đặc, dư và đun nóng. Thể tích khí thoát ra (đktc) là (cho Mn = 55)
A. 4,48 lít. B. 2,24 lít.
C. 3,36 lít. D. 6,72 lít.
Lời giải:
Đáp án A.
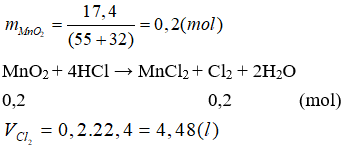
Câu 6: Hòa tan khí Cl2 vào dung dịch NaOH loãng, dư ở nhiệt độ phòng thu được dung dịch chứa các chất
A. NaCl, NaClO3, Cl2
B. NaCl, NaClO, NaOH
C. NaCl, NaClO3, NaOH
D. NaCl, NaClO3
Lời giải:
Đáp án B
Cl2 + 2NaOH → NaCl + NaClO + H2O
Dung dịch còn chứa NaOH dư.
Câu 7: Khí Cl2 không tác dụng với
A. khí O2.
B. dung dịch NaOH.
C. H2O.
D. dung dịch Ca(OH)2.
Lời giải:
Đáp án A
Cl2 + 2NaOH → NaCl + NaClO + H2O
Cl2 + H2O ⇆ HCl + HClO
Cl2 + Ca(OH)2 → CaOCl2 + H2O
Câu 8: Khí X được dùng để khử trùng cho nước sinh hoạt. Khí X là
A. CO2. B. O2.
C. Cl2. D. N2.
Lời giải:
Đáp án C
Câu 9: Trong phản ứng : Cl2 + H2O ⇆ HCl + HClO, Clo đóng vai trò
A. Chất tan.
B. Chất khử.
C. Vừa là chất oxi hóa, vừa là chất khử.
D. Chất oxi hóa.
Lời giải:
Đáp án C
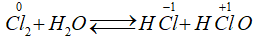
Câu 10: Có phản ứng hoá học xảy ra như sau:
H2S + 4Cl2 + 4H2O → H2SO4 + 8HCl
Câu nào diễn tả đúng tính chất các chất phản ứng?
A. H2S là chất khử, H2O là chất oxi hoá.
B. Cl2 là chất oxi hoá. H2O là chất khử.
C. H2S là chất oxi hoá, Cl2 là chất khử.
D. Cl2 là chất oxi hoá, H2S là chất khử.
Lời giải:
Đáp án D
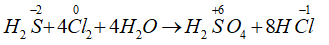
Số oxi hóa của S tăng từ -2 lên +6 do đó H2S là chất khử.
Số oxi hóa của Cl giảm từ 0 xuống – 1 do đó Cl2 là chất oxi hóa.
Câu 11: Số electron lớp ngoài cùng của nguyên tử Cl (z = 17) là
A. 7 B. 6
C. 5 D. 4
Lời giải:
Đáp án A
Cấu hình electron của Cl: 1s22s22p63s23p5.
→ Clo có 7e lớp ngoài cùng.
Câu 12: Phương trình hóa học nào sau đây biểu diễn đúng phản ứng xảy ra khi đưa dây sắt nóng đỏ vào bình chứa khí clo?
A. Fe + Cl2 → FeCl2
C. Fe + Cl2 → FeCl2 + FeCl3
B. 2Fe + 3Cl2 → 2FeCl3
D. Tất cả đều sai.
Lời giải:
Đáp án B
Câu 13: Sục clo từ từ đến dư vào dung dịch KBr thì hiện tượng quan sát được là
A. dung dịch từ không màu chuyển sang màu vàng, sau đó lại mất màu.
B. dung dịch có màu vàng nâu.
C. không có hiện tượng gì.
D. dung dịch có màu xanh nhạt.
Lời giải:
Đáp án B
Cl2 + 2KBr → 2KCl + Br2
Brom trong dung dịch có màu vàng nâu.
Câu 14: Trong phản ứng: 3Cl2 + 6KOH → 5KCl + KClO3 + 3H2O, clo đóng vai trò
A. vừa là chất khử, vừa là chất oxi hóa.
C. chất khử.
B. chất oxi hóa.
D. môi trường.
Lời giải:
Đáp án A
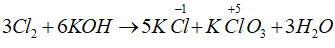
Câu 15: Phản ứng nào sau đây được dùng để điều chế clo trong phòng thí nghiệm?
A. 2NaCl -dpnc→ 2Na + Cl2
B. 2NaCl + 2H2O -dpnc→ H2 + 2NaOH + Cl2
C. MnO2 + 4HClđặc -t0→ MnCl2 + Cl2 + 2H2O
D. F2 + 2NaCl → 2NaF + Cl2
Lời giải:
Đáp án C
Trong PTN, Clo được điều chế bằng cách dùng các chất oxi hóa mạnh như KMnO4, MnO2 … oxi hóa Cl- thành Cl0.
Câu 16: Đốt 16,8g Fe trong bình đựng khí clo. Thể tích khí clo (đktc) tham gia phản ứng là
A. 4,48 lít. B. 10,08 lít.
C. 2,24 lít. D. 8,96 lít.
Lời giải:
Đáp án B
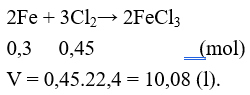
Câu 17: Trong phản ứng: Cl2 + 2NaBr → 2NaCl + Br2, clo đóng vai trò
A. vừa là chất khử, vừa là chất oxi hóa.
C. là chất khử.
B. là chất oxi hóa.
D. là môi trường.
Lời giải:
Đáp án B
Số oxi hóa của Cl giảm từ 0 xuống -1, do đó Cl2 là chất oxi hóa.
Câu 18: Nguyên tố X có cấu hình electron là 1s22s22p63s23p5. Nguyên tố X có đặc điểm
A. Thuộc chu kì 3, nhóm VIIA.
B. Là phi kim có 7 electron lớp ngoài cùng.
C. Có 17 proton trong nguyên tử.
D. Tất cả các câu trên đều đúng.
Lời giải:
Đáp án D
Câu 19: Thêm dần Clo vào dung dịch KI có chứa sẵn một ít hồ tinh bột. Hiện tượng xảy ra là
A. Không hiện tượng.
C. Dung dịch chuyển sang màu xanh.
B. Dung dịch hóa đỏ.
D. Dung dịch xuất hiện kết tủa.
Lời giải:
Đáp án C
Phản ứng sinh ra iot làm xanh hồ tinh bột
Cl2 + 2KI → I2 + 2KCl.
Câu 20: Số oxi hóa của Clo trong các hợp chất: Cl2, KCl, KClO3, KClO4 lần lượt là
A. +1, -1, +5, +7 C. 0,-1, +5, +7
B. -1, +1, +5, +7 D. 0, +2, +5, +7
Lời giải:
Đáp án C.
Câu 21: Từ bột Fe và một hoá chất X có thể điều chế trực tiếp được FeCl3. Vậy X là
A. Dung dịch HCl.
B. Dung dịch CuCl2.
C. Khí clo.
D. Cả A, B, C đều được.
Lời giải:
Đáp án C
2Fe + 3Cl2 → 2FeCl3
Câu 22: Điện phân dung dịch chứa 5,85 gam NaCl trong điều kiện có màng ngăn, sau phản ứng thu được V lít khí Cl2 ở đktc. Giá trị của V là?
A. 2,24 lít. B. 4,48 lít.
C. 1,12 lít. D. 5,6 lít.
Lời giải:
Đáp án C
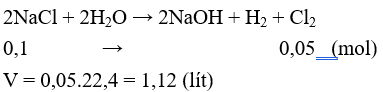
Câu 23: Đốt cháy hết 13,6g hỗn hợp Mg, Fe trong bình khí clo dư, sau phản ứng thấy khối lượng khí clo giảm 28,4 gam. Khối lượng muối clorua khan thu được là
A. 65,0 g. B. 38,0 g.
C. 50,8 g. D. 42,0 g.
Lời giải:
Đáp án D
Khối lượng khí clo giảm chính bằng khối lượng khí clo đã phản ứng.
mmuối = mKL + mClo = 13,6 + 28,4 = 42 (g).
Câu 24: Trong PTN, Cl2 thường được điều chế theo phản ứng :
HClđặc + KMnO4 → KCl + MnCl2 + Cl2 + H2O. Hệ số cân bằng tối giản của HCl trong phản ứng là
A. 4. B. 8.
C. 10. D. 16.
Lời giải:
Đáp án D
16HClđặc + 2KMnO4 → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
Câu 25: Lấy 2 lít khí H2 cho tác dụng với 3 lít khí Cl2. Hiệu suất phản ứng là 90%. Thể tích hỗn hợp sau phản ứng là (giả sử các thể tích đo trong cùng điều kiện nhiệt độ và áp suất)
A. 4,5 lít. B. 4 lít.
C. 5 lít. D. Kết quả khác.
Lời giải:
Đáp án C
Trong cùng điều kiện nhiệt độ và áp suất, tỉ lệ về thể tích cũng chính là tỉ lệ về số mol

⇒ Vsau phản ứng = 0,2 + 1,2 + 3,6 = 5.
Câu 26: Khối lượng HCl bị oxi hóa bởi MnO2 là bao nhiêu, biết rằng khí Cl2 sinh ra trong phản ứng đó có thể đẩy được 12,7g I2 từ dung dịch NaI.
A. 3,65g. B. 7,3g.
C. 14,6g. D. 36,5g.
Lời giải:
Đáp án B
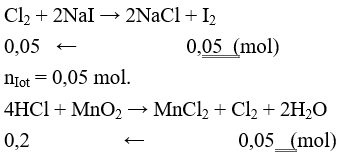
Khối lượng HCl cần dùng là: mHCl = 0,2 x 36,5 = 7,3g.
Câu 27: Đốt cháy hoàn toàn 7,2 gam kim loại M (có hoá trị II không đổi trong hợp chất) trong hỗn hợp khí X gồm Cl2 và O2. Sau phản ứng thu được 23,0 gam chất rắn và thể tích hỗn hợp khí đã phản ứng là 5,6 lít (đktc). Kim loại M là
A. Mg. B. Ca.
C. Be. D. Cu.
Lời giải:
Đáp án A
mrắn sau − mM = mX ⇒ 71nCl2 + 32nO2 = 23 − 7,2 = 15,8 g (1)
Lại có: nkhí = nCl2 + nO2 = 0,25 mol (2)
Giải hệ (1) và (2) ⇒ nCl2 = 0,2; nO2 = 0,05 mol
Gọi hóa trị của M là n
Bảo toàn e
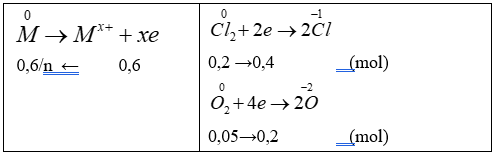
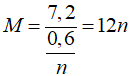
→ n = 2 ⇒ M = 24 (Mg) thỏa mãn.
Câu 28: Cho 10,8 gam kim loại M tác dụng hoàn toàn với khí Cl2 dư thu được 53,4 gam muối clorua. Kim loại M là
A. Mg. B. Al.
C. Fe. D. Zn.
Lời giải:
Đáp án B
Gọi n là hóa trị của M.
2M + nCl2 → 2MCln
Theo pt, nM = nmuối
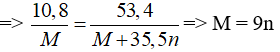
→ n = 3 ⇒ M = 27 (Al) thỏa mãn.
Câu 29: Để chứng minh Cl2 vừa có tính khử vừa có tính oxi hóa, người ta cho Cl2 tác dụng với
A. Dung dịch FeCl2.
B. Dây sắt nóng đỏ.
C. Dung dịch NaOH loãng.
D. Dung dịch KI.
Lời giải:
Đáp án C
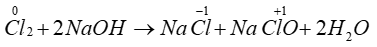
Câu 30: Cho m gam một đơn chất halogen (X2) tác dụng hết với magie thì thu được 9,5 gam muối. Mặt khác cho m gam X2 tác dụng hết với nhôm thì thu được 8,9 gam muối. Đơn chất halogen X2 là
A. F2 B. Cl2
C. Br2 D. I2.
Lời giải:
Đáp án B
Mg + X2 → MgX2
2Al + 3X2 → 2AlX3
Bảo toàn nguyên tố X:
2nMgX2 = 3nAlX3
⇒ 2.9,5/(24 + 2X) = 3.8,9/(27 + 3X) ⇒ X = 35,5 (Cl).
Thi online Hóa 10 KNTTThi online Hóa 10 CDThi online Hóa 10 CTST
Xem thêm các dạng bài tập Hóa học lớp 10 có trong đề thi Tốt nghiệp THPT khác:
- Bài tập về Flo, Brom, Iot cực hay, có lời giải
- Bài tập về hydrochloric acid HCl cực hay, có lời giải
- Bài tập về Hợp chất có oxi của clo cực hay, có lời giải
- Bài tập về Oxi cực hay, có lời giải
Để học tốt lớp 10 các môn học sách mới:
- Giải bài tập Lớp 10 Kết nối tri thức
- Giải bài tập Lớp 10 Chân trời sáng tạo
- Giải bài tập Lớp 10 Cánh diều
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 10 Global Success
- Giải Tiếng Anh 10 Friends Global
- Giải sgk Tiếng Anh 10 iLearn Smart World
- Giải sgk Tiếng Anh 10 Explore New Worlds
- Lớp 10 - Kết nối tri thức
- Soạn văn 10 (hay nhất) - KNTT
- Soạn văn 10 (ngắn nhất) - KNTT
- Soạn văn 10 (siêu ngắn) - KNTT
- Giải sgk Toán 10 - KNTT
- Giải sgk Vật lí 10 - KNTT
- Giải sgk Hóa học 10 - KNTT
- Giải sgk Sinh học 10 - KNTT
- Giải sgk Địa lí 10 - KNTT
- Giải sgk Lịch sử 10 - KNTT
- Giải sgk Kinh tế và Pháp luật 10 - KNTT
- Giải sgk Tin học 10 - KNTT
- Giải sgk Công nghệ 10 - KNTT
- Giải sgk Hoạt động trải nghiệm 10 - KNTT
- Giải sgk Giáo dục quốc phòng 10 - KNTT
- Lớp 10 - Chân trời sáng tạo
- Soạn văn 10 (hay nhất) - CTST
- Soạn văn 10 (ngắn nhất) - CTST
- Soạn văn 10 (siêu ngắn) - CTST
- Giải Toán 10 - CTST
- Giải sgk Vật lí 10 - CTST
- Giải sgk Hóa học 10 - CTST
- Giải sgk Sinh học 10 - CTST
- Giải sgk Địa lí 10 - CTST
- Giải sgk Lịch sử 10 - CTST
- Giải sgk Kinh tế và Pháp luật 10 - CTST
- Giải sgk Hoạt động trải nghiệm 10 - CTST
- Lớp 10 - Cánh diều
- Soạn văn 10 (hay nhất) - Cánh diều
- Soạn văn 10 (ngắn nhất) - Cánh diều
- Soạn văn 10 (siêu ngắn) - Cánh diều
- Giải sgk Toán 10 - Cánh diều
- Giải sgk Vật lí 10 - Cánh diều
- Giải sgk Hóa học 10 - Cánh diều
- Giải sgk Sinh học 10 - Cánh diều
- Giải sgk Địa lí 10 - Cánh diều
- Giải sgk Lịch sử 10 - Cánh diều
- Giải sgk Kinh tế và Pháp luật 10 - Cánh diều
- Giải sgk Tin học 10 - Cánh diều
- Giải sgk Công nghệ 10 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 10 - Cánh diều
- Giải sgk Giáo dục quốc phòng 10 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

