Chuyên đề bồi dưỡng HSG Hóa học 10 Bảng tuần hoàn (có lời giải)
Bài viết Chuyên đề bồi dưỡng HSG Hóa học 10 Bảng tuần hoàn gồm các dạng bài tập từ cơ bản đến nâng cao với phương pháp giải chi tiết và bài tập tự luyện đa dạng giúp Giáo viên có thêm tài liệu ôn thi Học sinh giỏi Hóa 10.
Chuyên đề bồi dưỡng HSG Hóa học 10 Bảng tuần hoàn (có lời giải)
Xem thử Chuyên đề bồi dưỡng HSG Hóa 10 Xem thử Đề thi HSG Hóa 10
Chỉ từ 300k mua trọn Chuyên đề bồi dưỡng HSG Hóa học 10 bản word có lời giải chi tiết:
- B1: gửi phí vào tk:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official - nhấn vào đây để thông báo và nhận giáo án
Phần I: HỆ THỐNG LÝ THUYẾT CƠ BẢN VÀ NÂNG CAO
I. CẤU TẠO BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
* Nguyên tắc sắp xếp
- Các nguyên tố được sắp xếp theo chiều tăng dần của điện tích hạt nhân nguyên tử.
- Các nguyên tố có cùng số lớp electron trong nguyên tử được xếp thành 1 hàng.
- Các nguyên tố có cùng số electron hóa trị trong nguyên tử được xếp thành 1 cột (trừ nhóm VIIIB).
* Cấu tạo bảng tuần hoàn
- Ô nguyên tố: mỗi nguyên tố hóa học được xếp vào 1 ô trong bảng tuần hoàn.
Số thứ tự ô nguyên tố = số hiệu nguyên tử Z
- Chu kì: là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron, được sắp xếp theo chiều tăng dần điện tích hạt nhân tăng dần.
Số thứ tự chu kì = số lớp electron
- Nhóm nguyên tố: là tập hợp các nguyên tố mà nguyên tử có cấu hình electron tương tự nhau, do đó tính chất hóa học gần giống nhau và được xếp thành 1 cột.
Số thứ tự nhóm nguyên tố = số electron hóa trị
Electron hóa trị = electron lớp ngoài cùng + phân lớp sát ngoài cùng chưa bão hòa.
* Phân loại nguyên tố
- Nguyên tố s: là nguyên tố mà electron cuối cùng được phân bố vào phân lớp s. Gồm nhóm IA, IIA và He.
- Nguyên tố p: là nguyên tố mà electron cuối cùng được phân bố vào phân lớp p. Gồm nhóm IIIA - VIIIA (trừ He).
- Nguyên tố d: là nguyên tố mà electron cuối cùng được phân bố vào phân lớp d. Gồm nhóm IB – VIIIB.( trừ họ La, Họ Ac )
- Nguyên tố f: là nguyên tố mà electron cuối cùng được phân bố vào phân lớp f. .( họ La, Họ Ac )
II.XU HƯỚNG BIẾN ĐỔI MỘT SỐ TÍNH CHẤT TRONG MỘT CHU KÌ, NHÓM A
* Xu hướng biến đổi một số tính chất nguyên tử các nguyên tố trong 1 chu kì và trong 1 nhóm A
- Trong một chu kì từ trái sang phải theo chiều tăng của điện tích hạt nhân nguyên tử thì:
+ Bán kính nguyên tử giảm dần.
+ Độ âm điện tăng dần.
+ Tính kim loại giảm dần và tính phi kim tăng dần.
+ Số electron hóa trị của các nguyên tố nhóm A (trừ chu kì 1) tăng từ 1 – 8.
- Trong một nhóm A từ trên xuống theo chiều tăng dần của điện tích hạt nhân nguyên tử thì:
+ Bán kính nguyên tử tăng dần.
+ Độ âm điện giảm dần.
+ Tính kim loại tăng dần và tính phi kim giảm dần.
* Xu hướng biến đổi thành phần và một số tính chất của hợp chất trong 1 chu kì
- Trong một chu kì từ trái sang phải theo chiều tăng của điện tích hạt nhân nguyên tử thì:
+ Hóa trị cao nhất của các nguyên tố nhóm A trong hợp chất với oxygen tăng từ I – VII (trừ chu kì 1 và nguyên tố fluorine).
+ Tính base của oxide và hydroxide tương ứng giảm dần, đồng thời tính acid của chúng tăng dần.
III. Ý NGHĨA BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC –ĐỊNH LUẬT TUẦN HOÀN
* Định luật tuần hoàn:
Tính chất của các nguyên tố và đơn chất, cũng như thành phần và tính chất của các hợp chất tạo nên từ các nguyên tố đó biến đổi tuần hoàn theo chiều tăng của điện tích hạt nhân nguyên tử.
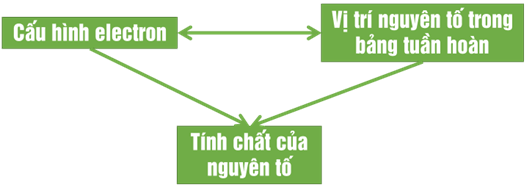
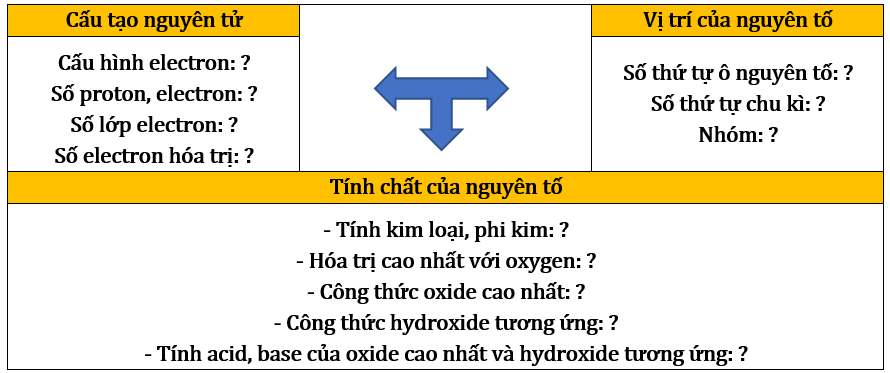
* Ý nghĩa bảng tuần hoàn
Cụ thể
Phần II: HỆ THỐNG BÀI TẬP THEO KIẾN THỨC LÝ THUYẾT CÓ PHÂN DẠNG
DẠNG 1. XÁC ĐỊNH TÊN NGUYÊN TỐ KHI BIẾT THÀNH PHẦN NGUYÊN TỐ TRONG HỢP CHẤT
A. TÓM TẮT LÝ THUYẾT VÀ PHƯƠNG PHÁP GIẢI
Cần nhớ một số điểm sau
- Hóa trị cao nhất với oxygen của nguyên tố = STT nhóm A.(trừ chu kì 1 và nguyên tố fluorine).
- Hóa trị với H( nếu có) = 8 - hóa trị cao nhất với oxygen. ( chỉ xét với các phi kim )
- % khối lượng của A trong hợp chất AxBy là: %A= MA*100/M.
- Muốn xác định nguyên tố đó là nguyên tố nào cần tìm được M =?.
Ví dụ minh họa
Ví dụ 1. Nguyên tố R có hóa trị cao nhất trong oxide gấp 3 lần hóa trị trong hợp chất với hydrogen. Hãy cho biết hóa trị cao nhất của R trong oxide.
Hướng dẫn giải:
Gọi hóa trị cao nhất của R trong oxide là m, hóa trị trong hợp chất với hydrogen là n. Ta có: m + n = 8.
Theo bài: m = 3n. Từ đây tìm được m = 6; n = 2.
................................
................................
................................
Xem thử Chuyên đề bồi dưỡng HSG Hóa 10 Xem thử Đề thi HSG Hóa 10
Xem thêm các Chuyên đề bài tập bồi dưỡng Học sinh giỏi Hóa học lớp 10 có đáp án hay khác:
Để học tốt lớp 10 các môn học sách mới:
- Giải bài tập Lớp 10 Kết nối tri thức
- Giải bài tập Lớp 10 Chân trời sáng tạo
- Giải bài tập Lớp 10 Cánh diều
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 10 Global Success
- Giải Tiếng Anh 10 Friends Global
- Giải sgk Tiếng Anh 10 iLearn Smart World
- Giải sgk Tiếng Anh 10 Explore New Worlds
- Lớp 10 - Kết nối tri thức
- Soạn văn 10 (hay nhất) - KNTT
- Soạn văn 10 (ngắn nhất) - KNTT
- Soạn văn 10 (siêu ngắn) - KNTT
- Giải sgk Toán 10 - KNTT
- Giải sgk Vật lí 10 - KNTT
- Giải sgk Hóa học 10 - KNTT
- Giải sgk Sinh học 10 - KNTT
- Giải sgk Địa lí 10 - KNTT
- Giải sgk Lịch sử 10 - KNTT
- Giải sgk Kinh tế và Pháp luật 10 - KNTT
- Giải sgk Tin học 10 - KNTT
- Giải sgk Công nghệ 10 - KNTT
- Giải sgk Hoạt động trải nghiệm 10 - KNTT
- Giải sgk Giáo dục quốc phòng 10 - KNTT
- Lớp 10 - Chân trời sáng tạo
- Soạn văn 10 (hay nhất) - CTST
- Soạn văn 10 (ngắn nhất) - CTST
- Soạn văn 10 (siêu ngắn) - CTST
- Giải Toán 10 - CTST
- Giải sgk Vật lí 10 - CTST
- Giải sgk Hóa học 10 - CTST
- Giải sgk Sinh học 10 - CTST
- Giải sgk Địa lí 10 - CTST
- Giải sgk Lịch sử 10 - CTST
- Giải sgk Kinh tế và Pháp luật 10 - CTST
- Giải sgk Hoạt động trải nghiệm 10 - CTST
- Lớp 10 - Cánh diều
- Soạn văn 10 (hay nhất) - Cánh diều
- Soạn văn 10 (ngắn nhất) - Cánh diều
- Soạn văn 10 (siêu ngắn) - Cánh diều
- Giải sgk Toán 10 - Cánh diều
- Giải sgk Vật lí 10 - Cánh diều
- Giải sgk Hóa học 10 - Cánh diều
- Giải sgk Sinh học 10 - Cánh diều
- Giải sgk Địa lí 10 - Cánh diều
- Giải sgk Lịch sử 10 - Cánh diều
- Giải sgk Kinh tế và Pháp luật 10 - Cánh diều
- Giải sgk Tin học 10 - Cánh diều
- Giải sgk Công nghệ 10 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 10 - Cánh diều
- Giải sgk Giáo dục quốc phòng 10 - Cánh diều











 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

