Chuyên đề bồi dưỡng HSG Hóa học 10 Liên kết hóa học - Cấu tạo phân tử - Lai hóa Orbital, thuyết Vsepr (có lời giải)
Bài viết Chuyên đề bồi dưỡng HSG Hóa học 10 Liên kết hóa học - Cấu tạo phân tử - Lai hóa Orbital, thuyết Vsepr gồm các dạng bài tập từ cơ bản đến nâng cao với phương pháp giải chi tiết và bài tập tự luyện đa dạng giúp Giáo viên có thêm tài liệu ôn thi Học sinh giỏi Hóa 10.
Chuyên đề bồi dưỡng HSG Hóa học 10 Liên kết hóa học - Cấu tạo phân tử - Lai hóa Orbital, thuyết Vsepr (có lời giải)
Xem thử Chuyên đề bồi dưỡng HSG Hóa 10 Xem thử Đề thi HSG Hóa 10
Chỉ từ 300k mua trọn Chuyên đề bồi dưỡng HSG Hóa học 10 bản word có lời giải chi tiết:
- B1: gửi phí vào tk:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official - nhấn vào đây để thông báo và nhận giáo án
PHẦN I: HỆ THỐNG LÝ THUYẾT CƠ BẢN VÀ NÂNG CAO
I. ĐẠI CƯƠNG VỀ LIÊN KẾT HÓA HỌC
Liên kết hóa học là sự kết hợp giữa các nguyên tử tạo thành phân tử hay tinh thể bền vững hơn. Nói cách khác là các nguyên tử chuyển thành phân tử hoặc tinh thể để đạt đến cấu hình electron bền vững của khí hiểm (qui tắc bát tử). Cần lưu ý là có một số trường hợp qui tắc bát tử (octet) không thỏa mãn nhưng phân tử đó vẫn tồn tại.
Ví dụ: PCl5 ; SF6 ; NO ; BeH2 ; …
1. Liên kết ion
a. Sự tạo thành ion, cation, anion
- Ion là những phần tử mang điện tích (nguyên tử vốn trung hòa điện do số electron bằng số proton, khi nguyên tử mất bớt hoặc thu thêm electron nó trở thành phần tử mang điện tích gọi là ion).
- Nguyên tử của nguyên tố kim loại nhường electron (thường là toàn bộ electron lớp ngoài cùng) để tạo ion dương (cation)
M → Mn+ + ne (n = 1, 2, 3)
Ví dụ: 12Mg : 1s22s22p63s2 =>Mg → Mg2++ 2e
- Nguyên tử của nguyên tố phi kim có xu hướng thu thêm để tạo ion âm (anion)
X + ne → Xn-(n = 1, 2, 3)
Ví dụ: 8O : 1s22s22p4=>O + 2e → O2-
b. Ion đơn nguyên tử, ion đa nguyên tử
- Ion đơn nguyên tử chỉ do một nguyên tử tạo nên còn ion đa nguyên tử là nhóm nguyên tử mang điện tích.
Ion đơn nguyên tử |
Ion đa nguyên tử |
|
Mg2+: Cation magnesium O2-: Anion oxide Cl- : Anion chloride S- Anion sulfide |
NO3-: Anion nitrate SO32- Anion sulfite SO42-: Anion sulfate H2SO4-: Anion dihydrogen phosphate ClO4-: Anion perchlorate |
c. Sự tạo thành liên kết ion
- Là liên kết được hình thành bởi lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
- Liên kết ion được hình thành giữa nguyên tử kim loại điển hình và nguyên tử phi kim điển hình.
- Đặc điểm của liên kết ion là không có tính định hướng và không có tính bão hòa.
- Do liên kết ion rất bền vững nên hợp chất ion đa phần là chất rắn, khó bay hơi, khó nóng chảy, một số hợp chất ion tan được trong nước tạo dung dịch dẫn điện. Độ bền vững của liên kết ion phụ thuộc vào bán kính ion, điện tích ion, năng lượng mạng lưới tinh thể, …
Ví dụ: Liên kết ion trong phân tử NaCl được hình thành theo sơ đồ sau
2. Liên kết cộng hóa trị
- Là liên kết được hình thành giữa hai nguyên tử bằng một hoặc nhiều cặp electron chung. Mỗi cặp electron chung tạo nên một liên kết cộng hóa trị.
- Liên kết cộng hóa trị trong đó cặp electron chung nằm chính giữa hai nguyên tử gọi là liên kết cộng hóa trị không phân cực (thường là liên cộng hóa trị trong đơn chất).
- Liên kết cộng hóa trị trong đó cặp electron chung bị lệch về phía nguyên tử có độ âm điện lớn hơn gọi là liên kết cộng hóa trị phân cực (thường là liên cộng hóa trị trong hợp chất).
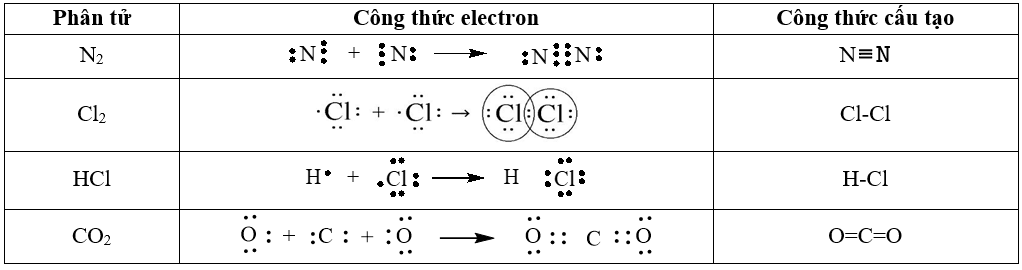
Ví dụ: Xét sự hình thành liên kết cộng hóa trị trong các phân tử N2; Cl2; HCl; CO2
Công thức Lewis: Cho biết sơ đồ liên kết trong các phân tử.Các bước để viết công thức Lewis:
● Nguyên tử trung tâm trong phân tử thường là nguyên tử có độ âm điện nhỏ nhất, các nguyên tử H và F thường ở đầu hoặc cuối (vì chỉ có hóa trị I).
● Sử dụng các cặp electron hóa trị để tạo liên kết giữa các nguyên tử sao cho mỗi nguyên tử có một cộng hóa trị hợp lí và thỏa mãn quy tắc bát tử.
3. Liên kết cho-nhận (liên kết phối trí)
- Liên kết cho-nhận là trường hợp riêng của liên kết cộng hóa trị, cặp electron chung chỉ do một nguyên tử đóng góp. Liên kết cho-nhận được biểu diễn bằng dấu mũi tên hướng từ nguyên tử cho sang nguyên tử nhận.
● Điều kiện hình thành liên cho nhận X→Y:
- Nguyên tử cho (X) có orbital chứa cặp electron tự do.
- Nguyên tử nhận (Y) có orbital hóa trị còn trống.
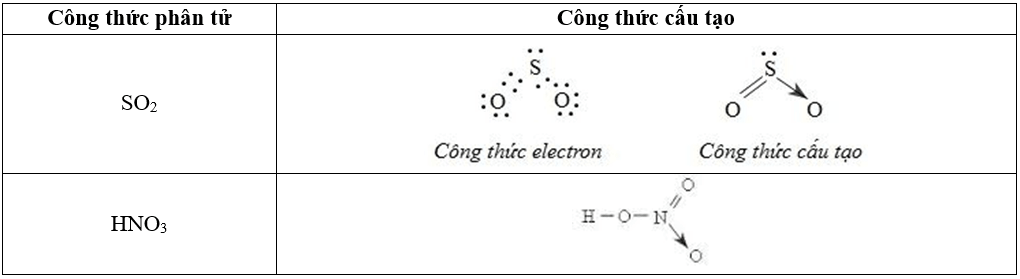
Ví dụ: Xét sự hình thành liên kết cho-nhận trong phân tử CO; SO2; HNO3.
................................
................................
................................
Xem thử Chuyên đề bồi dưỡng HSG Hóa 10 Xem thử Đề thi HSG Hóa 10
Xem thêm các Chuyên đề bài tập bồi dưỡng Học sinh giỏi Hóa học lớp 10 có đáp án hay khác:
Để học tốt lớp 10 các môn học sách mới:
- Giải bài tập Lớp 10 Kết nối tri thức
- Giải bài tập Lớp 10 Chân trời sáng tạo
- Giải bài tập Lớp 10 Cánh diều
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 10 Global Success
- Giải Tiếng Anh 10 Friends Global
- Giải sgk Tiếng Anh 10 iLearn Smart World
- Giải sgk Tiếng Anh 10 Explore New Worlds
- Lớp 10 - Kết nối tri thức
- Soạn văn 10 (hay nhất) - KNTT
- Soạn văn 10 (ngắn nhất) - KNTT
- Soạn văn 10 (siêu ngắn) - KNTT
- Giải sgk Toán 10 - KNTT
- Giải sgk Vật lí 10 - KNTT
- Giải sgk Hóa học 10 - KNTT
- Giải sgk Sinh học 10 - KNTT
- Giải sgk Địa lí 10 - KNTT
- Giải sgk Lịch sử 10 - KNTT
- Giải sgk Kinh tế và Pháp luật 10 - KNTT
- Giải sgk Tin học 10 - KNTT
- Giải sgk Công nghệ 10 - KNTT
- Giải sgk Hoạt động trải nghiệm 10 - KNTT
- Giải sgk Giáo dục quốc phòng 10 - KNTT
- Lớp 10 - Chân trời sáng tạo
- Soạn văn 10 (hay nhất) - CTST
- Soạn văn 10 (ngắn nhất) - CTST
- Soạn văn 10 (siêu ngắn) - CTST
- Giải Toán 10 - CTST
- Giải sgk Vật lí 10 - CTST
- Giải sgk Hóa học 10 - CTST
- Giải sgk Sinh học 10 - CTST
- Giải sgk Địa lí 10 - CTST
- Giải sgk Lịch sử 10 - CTST
- Giải sgk Kinh tế và Pháp luật 10 - CTST
- Giải sgk Hoạt động trải nghiệm 10 - CTST
- Lớp 10 - Cánh diều
- Soạn văn 10 (hay nhất) - Cánh diều
- Soạn văn 10 (ngắn nhất) - Cánh diều
- Soạn văn 10 (siêu ngắn) - Cánh diều
- Giải sgk Toán 10 - Cánh diều
- Giải sgk Vật lí 10 - Cánh diều
- Giải sgk Hóa học 10 - Cánh diều
- Giải sgk Sinh học 10 - Cánh diều
- Giải sgk Địa lí 10 - Cánh diều
- Giải sgk Lịch sử 10 - Cánh diều
- Giải sgk Kinh tế và Pháp luật 10 - Cánh diều
- Giải sgk Tin học 10 - Cánh diều
- Giải sgk Công nghệ 10 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 10 - Cánh diều
- Giải sgk Giáo dục quốc phòng 10 - Cánh diều

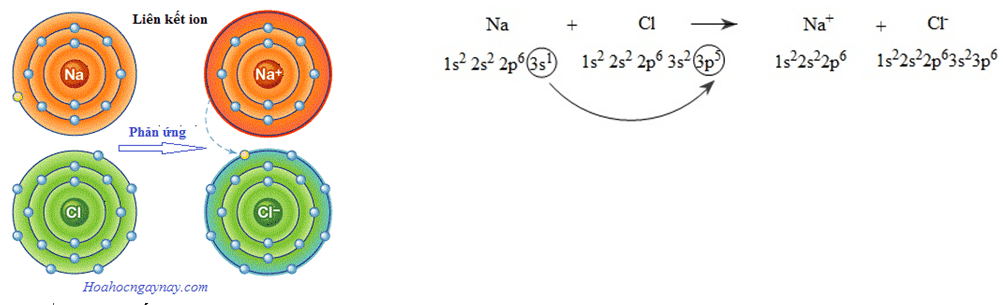








 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

