Lý thuyết Cấu trúc phân tử hợp chất hữu cơ (hay, chi tiết nhất)
Bài viết Lý thuyết Cấu trúc phân tử hợp chất hữu cơ hay, chi tiết giúp bạn nắm vứng kiến thức trọng tâm về Cấu trúc phân tử hợp chất hữu cơ.
Lý thuyết Cấu trúc phân tử hợp chất hữu cơ (hay, chi tiết nhất)
Thi online Hóa 11 KNTTThi online Hóa 11 CDThi online Hóa 11 CTST
Bài giảng: Bài 22 : Cấu trúc phân tử hợp chất hữu cơ - Cô Nguyễn Thị Nhàn (Giáo viên VietJack)
I. Thuyết cấu tạo hóa học
1. Nội dung thuyết cấu tạo hóa học
- Trong phân tử hợp chất hữu cơ, các nguyên tử liên kết với nhau theo đúng hóa trị và theo một thứ tự nhất định. Thứ tự liên kết đó gọi là cấu tạo hóa học. Sự thay đổi thứ tự liên kết đó, tức là thay đổi cấu tạo hóa học, sẽ tạo ra hợp chất khác.
Ví dụ: Công thức phân tử C2H6O có hai công thức cấu tạo (thứ tự liên kết khác nhau) ứng với 2 hợp chất sau:
H3C−O−CH3: đimethyl ete, chất khí, không tác dụng với Na.
H3C−CH2−O−H: ethyl alcohol, chất lỏng, tác dụng với Na giải phóng hiđro.
- Trong phân tử hợp chất hữu cơ, cacbon có hóa trị 4. Nguyên tử cacbon không những có thể liên kết với nguyên tử các nguyên tố khác mà còn liên kết với nhau thành mạch cacbon.
Ví dụ:
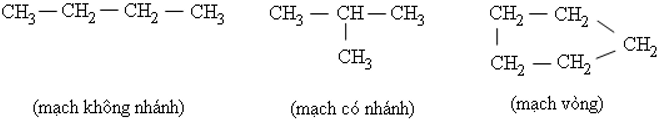
- Tính chất của các chất phụ thuộc vào thành phần phân tử (bản chất, số lượng các nguyên tử) và cấu tạo hóa học (thứ tự liên kết các nguyên tử).
Ví dụ:
- Phụ thuộc thành phần phân tử: CH4 là chất khí dễ cháy, CCl4 là chất lỏng không cháy; CH3Cl là chất khí không có tác dụng gây mê, còn CHCl3 là chất lỏng có tác dụng gây mê.
- Phụ thuộc cấu tạo hóa học: CH3CH2OH và CH3OCH3 khác nhau cả về tính chất hóa học.
2. Đồng đẳng đồng phân
a. Đồng đẳng
- Đồng đẳng là hiện tượng các chất hữu cơ có cấu tạo và tính chất hóa học tương tự nhau nhưng thành phần phân tử khác nhau một hay nhiều nhóm CH2.
- Các chất thuộc cùng dãy đồng đẳng hợp thành một dãy đồng đẳng có công thức chung.
b. Đồng phân
- Đồng phân là các chất hữu cơ có cùng công thức phân tử nhưng cấu tạo khác nhau nên tính chất hóa học khác nhau.
- Cần chú ý phân biệt đồng phân cấu tạo và đồng phân lập thể (đồng phân cis – trans).
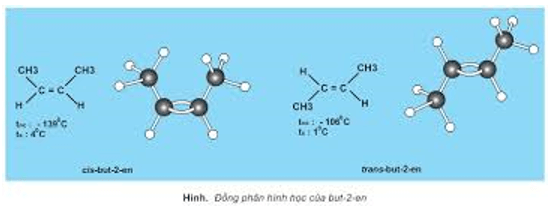
II. Liên kết trong phân tử hợp chất hữu cơ
1. Các loại liên kết trong phân tử hợp chất hữu cơ
- Liên kết thường gặp trong hợp chất hữu cơ là liên kết CHT, gồm liên kết σ và liên kết π.
- Sự tổ hợp của liên kết σ và π tạo thành liên kết đôi hoặc ba (liên kết bội).
a. Liên kết đơn (σ)
- Do 1 cặp electron tạo thành, được biểu diễn bằng 1 gạch nối giữa 2 nguyên tử.
- Liên kết σ bền.
b. Liên kết đôi (1 σ và 1 π)
- Do 2 cặp electron tạo thành, được biểu diễn bằng 2 gạch nối giữa 2 nguyên tử.
- Gồm 1σ bền và 1 π kém bền.
c. Liên kết ba (1 σ và 2 π)
- Do 3 cặp electron tạo thành, được biểu diễn bằng 3 gạch nối giữa 2 nguyên tử.
- Gồm 1σ bền và 2 π kém bền.
* Các liên kết đôi và ba gọi là liên kết bội.
- Khi nguyên tử cacbon tham gia liên kết đơn, các obitan nguyên tử hóa trị lai hóa kiểu sp3 (lai hóa tứ diện đều). Góc lai 109’28”.
- Khi nguyên tử cacbon tham gia liên kết đôi, các obitan nguyên tử hóa trị lai hóa kiểu sp2 (lai hóa đều). Góc lai hóa 120º. Ví dụ: Phân tử C2H4.
- Khi nguyên tử cacbon tham gia liên kết 3, các obitan nguyên tử hóa trị lai hóa kiểu sp (lai hóa đường thẳng). Góc lai hóa 180º. Ví dụ: Phân tử C2H2.
2. Các loại công thức cấu tạo
Cho biết trật tự liên kết của các nguyên tử trong phân tử. Khi viết CTCT phải nhất thiết đảm bảo đúng hóa trị của các nguyên tố. Có thể viết CTCT dưới dạng đầy đủ và rút gọn.
- Công thức khai triển: Biểu diễn trên mặt phẳng giấy tất cả các liên kết giữa các nguyên tử.
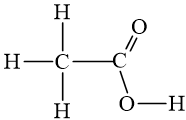
- Công thức CT thu gọn:
* Các nguyên tử hoặc nhóm nguyên tử cùng liên kết với một nguyên tử C được viết thành 1 nhóm.
* Hoặc chỉ biểu diễn liên kết giữa các nguyên tử C và với nhóm chức (mỗi đầu đoạn thẳng hoặc điểm gấp khúc là 1 cacbon, không biếu thị số nguyên tử H liên kết với cacbon).
Ví dụ: Viết công thức cấu tạo của acetic acid.
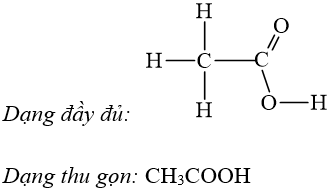
III. Đồng phân cấu tạo
1. Khái niệm đồng phân cấu tạo
Butan−1−ol và diethylete có cùng công thức phân tử C4H10O nhưng do khác nhau về cấu tạo hóa học nên khác nhau về tính chất vật lí và tính chất hóa học.
Vậy những hợp chất có cùng công thức phân tử nhưng có cấu tạo hóa học khác nhau gọi là những đồng phân cấu tạo.
2. Phân loại đồng phân cấu tạo
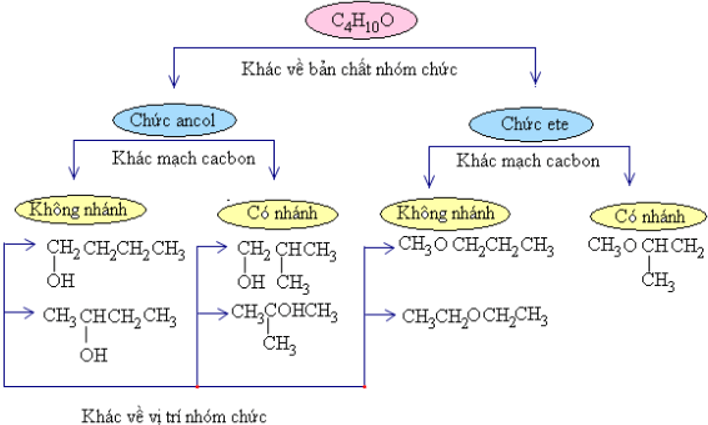
Những đồng phân khác nhau về bản chất nhóm chức gọi là đồng phân nhóm chức. Những đồng phân khác nhau về sự phân nhánh mạch cacbon gọi là đồng phân mạch cacbon. Những đồng phân khác nhau về vị trí nhóm chức gọi là đồng phân vị trí nhóm chức.
IV. Cách biểu diễn cấu trúc không gian phân tử hữu cơ
1. Công thức phối cảnh
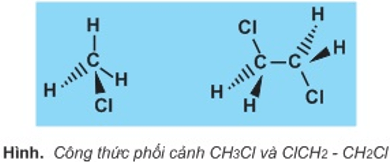
Công thức phối cảnh là một loại công thức lập thể.
Đường nét liền biểu diễn liên kết nằm trên mặt trang giấy.
Đường nét đậm biểu diễn liên kết hướng về mắt ta (ra phía trước trang giấy).
Đường nét đứt biểu diễn liên kết hướng ra xa mắt ta (ra phía sau trang giấy).
2. Mô hình phân tử
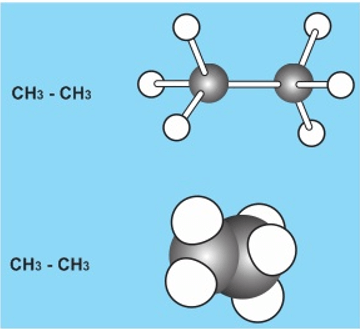
a. Mô hình rỗng
Các quả cầu tượng trưng cho các nguyên tử, các thanh nối tượng trưng cho các liên kết giữa chúng. Góc giữa hai các thanh nối bằng góc lai hóa.
b. Mô hình đặc
Các quả cầu cắt vát tượng trưng cho các nguyên tử được ghép với nhau theo đúng vị trí không gian của chúng.
V. Đồng phân lập thể
1. Khái niệm về đồng phân lập thể
- Ứng với công thức cấu tạo CHCl=CHCl có hai cách sắp xếp không gian khác nhau dẫn tới hai chất đồng phân:
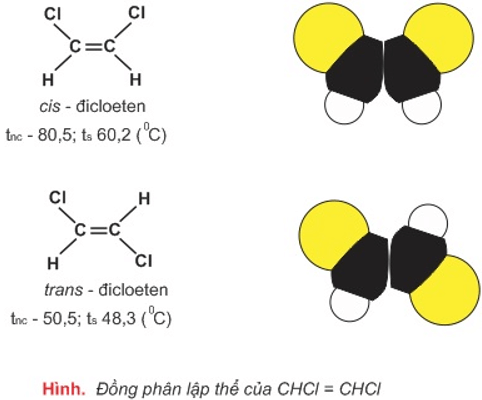
- Kết luận:
- Đồng phân lập thể là những đồng phân có cấu tạo hóa học như sau (cùng công thức cấu tạo) nhưng khác nhau về sự phân bố không gian của các nguyên tử trong phân tử (tức khác nhau về cấu trúc không gian của phân tử).
2. Quan hệ giữa đồng phân cấu tạo và đồng phân lập thể
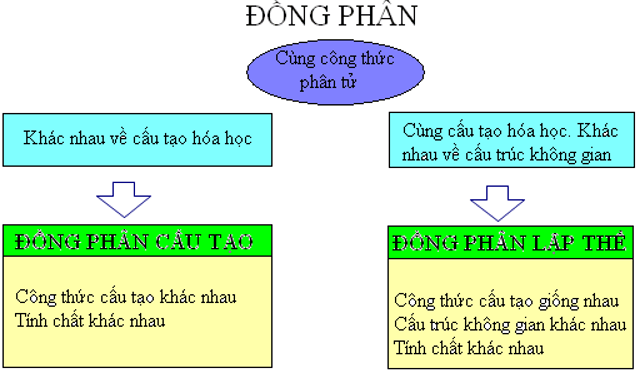
3. Cấu tạo hóa học và cấu trúc hóa học
- Cấu tạo hóa học cho ta biết các nguyên tử liên kết với nhau theo thứ tự nào, bằng liên kết đơn hay liên kết bội, nhưng không cho biết sự phân bố trong không gian của chúng. Cấu tạo hóa học được biểu diễn bởi công thức cấu tạo.
- Cấu tạo hóa học và cấu trúc không gian của phân tử hợp thành cấu trúc hóa học.
- Cấu trúc hóa học vừa cho biết cấu tạo hóa học vừa cho biết sự phân bố trong không gian của các nguyên tử trong phân tử. Cấu trúc hóa học thường được biểu diễn bởi công thức lập thể.
Thi online Hóa 11 KNTTThi online Hóa 11 CDThi online Hóa 11 CTST
Xem thêm các phần Lý thuyết Hóa học lớp 11 ôn thi Tốt nghiệp THPT hay khác:
- Lý thuyết Khái quát về hóa học hữu cơ
- Lý thuyết Công thức phân tử hợp chất hữu cơ
- Lý thuyết Phản ứng hữu cơ
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 11 Global Success
- Giải sgk Tiếng Anh 11 Smart World
- Giải sgk Tiếng Anh 11 Friends Global
- Lớp 11 - Kết nối tri thức
- Soạn văn 11 (hay nhất) - KNTT
- Soạn văn 11 (ngắn nhất) - KNTT
- Giải sgk Toán 11 - KNTT
- Giải sgk Vật Lí 11 - KNTT
- Giải sgk Hóa học 11 - KNTT
- Giải sgk Sinh học 11 - KNTT
- Giải sgk Lịch Sử 11 - KNTT
- Giải sgk Địa Lí 11 - KNTT
- Giải sgk Giáo dục KTPL 11 - KNTT
- Giải sgk Tin học 11 - KNTT
- Giải sgk Công nghệ 11 - KNTT
- Giải sgk Hoạt động trải nghiệm 11 - KNTT
- Giải sgk Giáo dục quốc phòng 11 - KNTT
- Giải sgk Âm nhạc 11 - KNTT
- Lớp 11 - Chân trời sáng tạo
- Soạn văn 11 (hay nhất) - CTST
- Soạn văn 11 (ngắn nhất) - CTST
- Giải sgk Toán 11 - CTST
- Giải sgk Vật Lí 11 - CTST
- Giải sgk Hóa học 11 - CTST
- Giải sgk Sinh học 11 - CTST
- Giải sgk Lịch Sử 11 - CTST
- Giải sgk Địa Lí 11 - CTST
- Giải sgk Giáo dục KTPL 11 - CTST
- Giải sgk Hoạt động trải nghiệm 11 - CTST
- Giải sgk Âm nhạc 11 - CTST
- Lớp 11 - Cánh diều
- Soạn văn 11 Cánh diều (hay nhất)
- Soạn văn 11 Cánh diều (ngắn nhất)
- Giải sgk Toán 11 - Cánh diều
- Giải sgk Vật Lí 11 - Cánh diều
- Giải sgk Hóa học 11 - Cánh diều
- Giải sgk Sinh học 11 - Cánh diều
- Giải sgk Lịch Sử 11 - Cánh diều
- Giải sgk Địa Lí 11 - Cánh diều
- Giải sgk Giáo dục KTPL 11 - Cánh diều
- Giải sgk Tin học 11 - Cánh diều
- Giải sgk Công nghệ 11 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 11 - Cánh diều
- Giải sgk Giáo dục quốc phòng 11 - Cánh diều
- Giải sgk Âm nhạc 11 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

