Lý thuyết Sự điện li của nước. pH. Chất chỉ thị axit - bazơ (hay, chi tiết nhất)
Bài viết Lý thuyết Sự điện li của nước. pH. Chất chỉ thị axit - bazơ hay, chi tiết giúp bạn nắm vứng kiến thức trọng tâm về Sự điện li của nước. pH. Chất chỉ thị axit - bazơ.
Lý thuyết Sự điện li của nước. pH. Chất chỉ thị axit - bazơ (hay, chi tiết nhất)
Thi online Hóa 11 KNTTThi online Hóa 11 CDThi online Hóa 11 CTST
Bài giảng: Bài 3: Sự điện li của nước. pH. Chất chỉ thị axit-bazơ - Cô Nguyễn Nhàn (Giáo viên VietJack)
I. Nước là chất điện li yếu
1. Sự điện li của nước
- Nước là chất điện li rất yếu.
- Phương trình điện li:
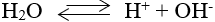
2. Tích số ion của nước
- Ở 25oC, hằng số KH2O gọi là tích số ion của nước:
KH2O = [H+].[OH-] = 10-14
⇒ [H+] = [OH-] = 10-7.
- Môi trường trung tính là môi trường trong đó [H+] = [OH-] = 10-7 M.
3. Ý nghĩa tích số ion của nước
a. Môi trường axit
Là môi trường trong đó [H+] > [OH-] hay [H+] > 10-7 M.
b. Môi trường kiềm
Là môi trường trong đó [H+] < [OH-] hay [H+] < 10-7 M.
II. Khái niệm về pH. Chất chỉ thị axit – bazơ
1. Khái niệm về pH

2. Chất chỉ thị axit – bazơ
- Là chất có màu biến đổi phụ thuộc vào giá trị pH của dung dịch.
Ví dụ: Quỳ tím, phenolphatalenin.
Bảng màu của quỳ và phenolphtalein trong dung dịch ở các khoảng pH khác nhau.
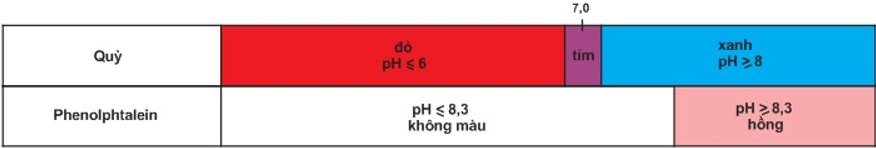
Trộn lẫn một số chất chỉ thị có màu biến đổi kế tiếp nhau theo giá trị pH, ta được hỗn hợp chất chỉ thị vạn năng. Dùng băng giấy tẩm dung dịch hỗn hợp này có thể xác định được gần đúng giá trị pH của dung dịch.
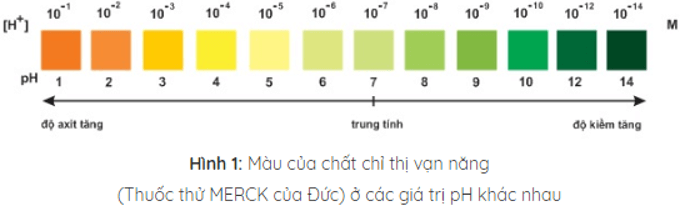
3. Bảng công thức pH trong các môi trường
| CÔNG THỨC | MÔI TRƯỜNG |
|
pH = - lg[H+] pOH = - lg[OH-] [H+].[OH-] = 10-14 pH + pOH = 14 pH = a [H+] = 10-a pOH = b [OH-] = 10-b |
pH < 7 → Môi trường axít pH > 7 → Môi trường bazơ pH = 7 → Môi trường trung tính [H+] càng lớn ↔ Giá trị pH càng bé [OH-] càng lớn ↔ Giá trị pH càng lớn |
Thi online Hóa 11 KNTTThi online Hóa 11 CDThi online Hóa 11 CTST
Xem thêm các phần Lý thuyết Hóa học lớp 11 ôn thi Tốt nghiệp THPT hay khác:
- Lý thuyết Sự điện li
- Lý thuyết Axit, bazo, muối
- Lý thuyết Phản ứng trao đổi ion trong dung dịch chất điện li
- Lý thuyết về Axit, bazơ và muối
- Lý thuyết Phân loại các chất điện li
- Dạng 1: Bài tập lý thuyết về sự điện li, chất điện li, viết phương trình điện li
- Dạng 2: Phương pháp bảo toàn điện tích
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 11 Global Success
- Giải sgk Tiếng Anh 11 Smart World
- Giải sgk Tiếng Anh 11 Friends Global
- Lớp 11 - Kết nối tri thức
- Soạn văn 11 (hay nhất) - KNTT
- Soạn văn 11 (ngắn nhất) - KNTT
- Giải sgk Toán 11 - KNTT
- Giải sgk Vật Lí 11 - KNTT
- Giải sgk Hóa học 11 - KNTT
- Giải sgk Sinh học 11 - KNTT
- Giải sgk Lịch Sử 11 - KNTT
- Giải sgk Địa Lí 11 - KNTT
- Giải sgk Giáo dục KTPL 11 - KNTT
- Giải sgk Tin học 11 - KNTT
- Giải sgk Công nghệ 11 - KNTT
- Giải sgk Hoạt động trải nghiệm 11 - KNTT
- Giải sgk Giáo dục quốc phòng 11 - KNTT
- Giải sgk Âm nhạc 11 - KNTT
- Lớp 11 - Chân trời sáng tạo
- Soạn văn 11 (hay nhất) - CTST
- Soạn văn 11 (ngắn nhất) - CTST
- Giải sgk Toán 11 - CTST
- Giải sgk Vật Lí 11 - CTST
- Giải sgk Hóa học 11 - CTST
- Giải sgk Sinh học 11 - CTST
- Giải sgk Lịch Sử 11 - CTST
- Giải sgk Địa Lí 11 - CTST
- Giải sgk Giáo dục KTPL 11 - CTST
- Giải sgk Hoạt động trải nghiệm 11 - CTST
- Giải sgk Âm nhạc 11 - CTST
- Lớp 11 - Cánh diều
- Soạn văn 11 Cánh diều (hay nhất)
- Soạn văn 11 Cánh diều (ngắn nhất)
- Giải sgk Toán 11 - Cánh diều
- Giải sgk Vật Lí 11 - Cánh diều
- Giải sgk Hóa học 11 - Cánh diều
- Giải sgk Sinh học 11 - Cánh diều
- Giải sgk Lịch Sử 11 - Cánh diều
- Giải sgk Địa Lí 11 - Cánh diều
- Giải sgk Giáo dục KTPL 11 - Cánh diều
- Giải sgk Tin học 11 - Cánh diều
- Giải sgk Công nghệ 11 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 11 - Cánh diều
- Giải sgk Giáo dục quốc phòng 11 - Cánh diều
- Giải sgk Âm nhạc 11 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

