100 câu trắc nghiệm Nguyên tử có lời giải (cơ bản - phần 3)
Với 100 câu trắc nghiệm Nguyên tử (cơ bản - phần 3) có lời giải chi tiết sẽ giúp học sinh ôn tập, biết cách làm câu trắc nghiệm Nguyên tử (cơ bản - phần 3).
100 câu trắc nghiệm Nguyên tử có lời giải (cơ bản - phần 3)
Thi online Hóa 10 KNTTThi online Hóa 10 CDThi online Hóa 10 CTST
Bài 1: Một nguyên tử có 9 electron và hạt nhân của nó có 10 neutron. Số hiệu của nguyên tử đó là bao nhiêu ?
A. 9 B. 18
C. 19 D. 28
Lời giải:
Chọn đáp án: A
Giải thích: Số hiệu nguyên tử = số hạt p = số hạt e.
Bài 2: Nguyên tử nguyên tố X có số khối bằng 23, số hiệu nguyên tử bằng 11. X có
A. số proton là 12.
B. số neutron là 12.
C. số neutron là 11.
D. tổng số neutron và proton là 22.
Lời giải:
Chọn đáp án: B
Giải thích:
Số hiệu nguyên tử = số hạt p.
Số khối A = Z + N => N = A – Z = 23 – 11 = 12 hạt
Bài 3: Một nguyên tố của nguyên tử X có tổng số hạt (p, n, e) bằng 52 và có số khối là 35. Số hiệu nguyên tử của nguyên tố X là
A. 17 B. 20
C. 18 D. 16
Lời giải:
Chọn đáp án: A.
Giải thích:
Tổng số hạt proton, neutron và electron trong 1 nguyên tử nguyên tố X là 52:
P + e + n = 52 hay 2p + n = 52 (do p = e) (1)
Số khối bằng 35
P + n = 35 (2)
Giải (1), (2) ta có p = e = 17; n =18
Bài 4: Nguyên tố A được kí hiệu như sau: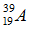
A. 19 B. 39
C. 20 D. 58
Lời giải:
Chọn đáp án: C.
Giải thích: A = Z + N => N = A – Z = 39 – 19 = 20 hạt.
Bài 5: Cấu hình e của nguyên tố canxi (Z=20) là 1s22s22p63s23p64s2. Tìm câu sai?
A. Lớp K có 2e.
B. Lớp L có 8e
C. Lớp M có 6e.
D. Lớp N có 2e.
Lời giải:
Chọn đáp án: C.
Giải thích: Lớp M có 8e.
Bài 6: Nguyên tử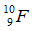
A. 9 B. 10
C. 19 D. 28
Lời giải:
Chọn đáp án: A.
Bài 7: Một nguyên tử có 9 electron ở lớp vỏ, hạt nhân của nó có 10 neutron. Số hiệu nguyên tử đó là
A. 9. B. 18.
C. 19. D. 28.
Lời giải:
Chọn đáp án: A.
Giải thích: Số hiệu nguyên tử = số hạt p = số hạt e.
Bài 8: Hạt nhân của nguyên tử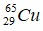
A. 65 B. 29
C. 36 D. 94
Lời giải:
Chọn đáp án: C.
Giải thích: A = Z + N => N = A – Z = 65 – 29 = 36 hạt.
Bài 9: Đồng có đồng vị 63Cu (69,1%) và 65Cu. Nguyên tử khối trung bình của đồng là:
A. 64,000(u)
B. 63,542(u)
C. 64,382(u)
D. 63,618(u)
Lời giải:
Chọn đáp án: D
Giải thích:
Bài 10: A, B là nguyên tử đồng vị. A có số khối bằng 24 chiếm 60%, nguyên tử khối trung bình của hai đồng vị là 24,4. Số khối của đồng vị B là:
A. 26 B. 25
C. 23 D. 27
Lời giải:
Chọn đáp án: B
Giải thích:
Gọi số khối của đồng vị thứ 2 là x
Đồng vị có số khối 24 chiếm 60%, vậy đồng vị còn lại chiếm 40%
Ta có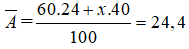
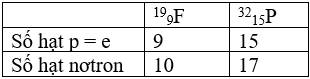
Bài 11: Một đồng vị của nguyên tử photpho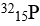
A. 32 B. 15
C. 47 D. 17
Lời giải:
Chọn đáp án: B.
Bài 12: Nguyên tử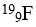
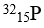
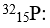
A. Hơn nguyên tử F 13p
B. Hơn nguyên tử F 6e
C. Hơn nguyên tử F 6n
D. Hơn nguyên tử F 13e
Lời giải:
Chọn đáp án: B.
Giải thích:
Bài 13: Nguyên tử X có điện tích hạt nhân là +2,7234.10-18C. Trong nguyên tử X số hạt mang điện nhiều hơn số hạt không mang điện là 16. Kí hiệu nguyên tử của X là
A. 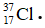
B. 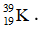
C. 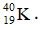
D. 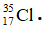
Lời giải:
Chọn đáp án: A
Giải thích:
Điện tích hạt nhân = số p . (+1,602.10-19) = +2,7234.10-18C
Số p = 17, số n = 17 + 16 = 35
Bài 14: Tống số hạt p, n, e trong nguyên tử của một nguyên tố X là 20. Trong đó, số hạt không mang điện nhiều hơn số hạt mang điện dương là 2 đơn vị. Số khối A của X:
A. 14. B. 12.
C. 16. D. 22.
Lời giải:
Chọn đáp án: A
Giải thích:
Tổng số hạt proton, neutron và electron trong 1 nguyên tử nguyên tố X là 20:
p + e + n = 20 hay 2p + n = 20 (do p = e) (1)
Số hạt không mang điện (n) nhiều hơn số hạt mang điện dương (p) là 2 hạt
n - p = 2 (2)
Giải (1), (2) ta có p = e = 6; n =8
Số khối của X = Z + N = p + n =14
Bài 15: Một nguyên tử nguyên tố R có tổng số hạt mang điện và không mang điện là 34, trong đó số hạt mang điện gấp 1,833 lần số hạt không mang điện. Số hạt proton trong nguyên tố R là
A. 12 B. 11
C. 23 D. 14
Lời giải:
Chọn đáp án: B.
Giải thích:
Tổng số hạt proton, neutron và electron trong 1 nguyên tử nguyên tố R là 34:
p + e + n = 34 hay 2p + n = 34 (do p = e) (1)
Số mang điện (p và e) gấp 1,833 lần số hạt không mang điện (n)
p + e = 1,833n hay 2p = 1,833n (do p = e) (2)
Giải (1), (2) ta có p = e =11 ; n = 12
Bài 16: Nguyên tử các nguyên tố X, Y, Z có cấu hình electron là
X : 1s22s22p63s23p4
Y : 1s22s22p63s23p6
Z : 1s22s22p63s23p64s2
Trong các nguyên tố X, Y, Z nguyên tố kim loại là
A. X. B. Y.
C. Z. D. X và Y.
Lời giải:
Chọn đáp án: C.
Giải thích: Kim loại là những nguyên tố có 1, 2, 3 electron lớp ngoài cùng.
Bài 17: Cấu hình electron nào dưới đây không đúng?
A. C (Z = 6): [He] 2s22p2
B. Cr (Z = 24): [Ar] 3d54s1
C. O2− (Z = 8): [He] 2s22p4
D. Fe (Z = 26): [Ar] 3d64s2
Lời giải:
Chọn đáp án: C
Giải thích: Cấu hình của O: [He] 2s22p4 → O2-: [He] 2s22p6
Bài 18: Nhận định nào không đúng ? Hai nguyên tử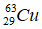
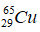
A. là đồng vị của nhau.
B. có cùng số electron.
C. có cùng số neutron.
D. có cùng số hiệu nguyên tử
Lời giải:
Chọn đáp án: C.
Giải thích: 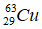
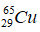
Bài 19: Tổng số hạt proton, neutron, electron trong nguyên tử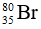
A. 115. B. 80.
C. 35. D. 60.
Lời giải:
Chọn đáp án: A.
Giải thích:
Br có số hạt p = e = 35.
Số hạt n = 80 – 35 = 45.
Tổng số hạt = p + n + e = 115 hạt.
Bài 20: Câu nào sau đây sai?
A. Các đồng vị phải có số khối khác nhau.
B. Các đồng vị phải có số neutron khác nhau.
C. Các đồng vị phải có cùng điện tích hạt nhân.
D. Các đồng vị phải có số electron khác nhau
Lời giải:
Chọn đáp án: D.
Giải thích: Đồng vị có cùng số p = e.
Bài 21: Những nguyên tử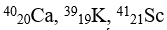
A. Số hiệu nguyên tử
B. Số e
C. Số neutron
D. Số khối
Lời giải:
Chọn đáp án: C.
Bài 22: Một nguyên tử có 8P, 8E và 8N. Chọn nguyên tư đồng vị với nó.
A. 8P, 8N, 9E.
B. 8P, 9N, 9E.
C. 9P, 8N, 9E.
D. 8P, 9N, 8E.
Lời giải:
Chọn đáp án: D.
Bài 23: Lớp E nào có số E tối đa là 18 E.
A. n=1.
B. n=2.
C. n=3.
D. n=4.
Lời giải:
Chọn đáp án: C.
Giải thích: Lớp M (n=3).
Bài 24: Nguyên tử 27X có cấu hình 1s22s22p63s2 3p1. Hạt nhân nguyên tử X có.
A. 14N, 13P, 13E
B. 13P, 14N.
C. 13N, 14P.
D. 13P, 14E, 13N
Lời giải:
Chọn đáp án: B
Bài 25: Ion M3+ có cấu hình electron phân lớp ngoài cùng là 3d5. Vậy cấu hình electron của M là
A. 1s22s22p63s23p64s23d8
B. 1s22s22p63s23p63d64s2
C. 1s22s22p63s23p63d8
D. 1s22s22p63s23p63d54s24p1
Lời giải:
Chọn đáp án: B.
Giải thích: Nguyên tử M đã nhường đi 3 electron để tạo ion M3+
Bài 26: Ion X2- và M3+ đều có cấu hình electron là 1s22s22p6. X, M là những nguyên tử nào sau đây ?
A. F, Ca
B. O, Al
C. S, Al
D. O, Mg
Lời giải:
Chọn đáp án: B.
Giải thích:
Cấu hình electron của X: 1s22s22p4 (Oxi)
Cấu hình electron của M: 1s22s22p63s23p1 (Al)
Bài 27: Lớp e ngoài cùng của kim loại kiềm được biểu thị chung là:
A. np1.
B. ns2
C. ns2np1.
D. Tất cả đều sai.
Lời giải:
Chọn đáp án: D
Giải thích: Kim loại kiềm có 1 electron lớp ngoài cùng, cấu hình phù hợp là ns1
Bài 28: Số proton, neutron, electron trong nguyên tử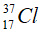
A. 17, 35, 18
B. 17, 18, 18
C. 35, 17, 18
D. 17, 20, 17
Lời giải:
Chọn đáp án: D
Giải thích:
Nguyên tử Clo có p = Z = e = 17 (hạt)
N = A- Z = 37 – 17 = 20 (hạt)
Bài 29: Nhận định nào sau đây đúng khi nói về 3 nguyên tử: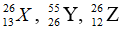
A. X và Y có cùng số n
B. X, Z là 2 đồng vị của cùng một nguyên tố hóa học.
C. X, Y thuộc cùng 1 nguyên tố hóa học.
D. X, Z có cùng số khối.
Lời giải:
Chọn đáp án: D.
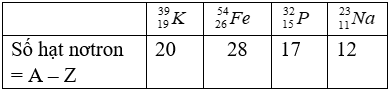
Bài 30: Hạt nhân của nguyên tử nào có số hạt neutron là 28?
A. 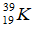
B. 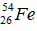
C. 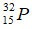
D. 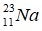
Lời giải:
Chọn đáp án: B.
Giải thích:
Thi online Hóa 10 KNTTThi online Hóa 10 CDThi online Hóa 10 CTST
Xem thêm các dạng bài tập Hóa học lớp 10 có trong đề thi Tốt nghiệp THPT khác:
- 100 câu trắc nghiệm Nguyên tử có lời giải (cơ bản - phần 1)
- 100 câu trắc nghiệm Nguyên tử có lời giải (cơ bản - phần 2)
- 100 câu trắc nghiệm Nguyên tử có lời giải (nâng cao - phần 1)
- 100 câu trắc nghiệm Nguyên tử có lời giải (nâng cao - phần 2)
- 100 câu trắc nghiệm Nguyên tử có lời giải (nâng cao - phần 3)
Để học tốt lớp 10 các môn học sách mới:
- Giải bài tập Lớp 10 Kết nối tri thức
- Giải bài tập Lớp 10 Chân trời sáng tạo
- Giải bài tập Lớp 10 Cánh diều
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 10 Global Success
- Giải Tiếng Anh 10 Friends Global
- Giải sgk Tiếng Anh 10 iLearn Smart World
- Giải sgk Tiếng Anh 10 Explore New Worlds
- Lớp 10 - Kết nối tri thức
- Soạn văn 10 (hay nhất) - KNTT
- Soạn văn 10 (ngắn nhất) - KNTT
- Soạn văn 10 (siêu ngắn) - KNTT
- Giải sgk Toán 10 - KNTT
- Giải sgk Vật lí 10 - KNTT
- Giải sgk Hóa học 10 - KNTT
- Giải sgk Sinh học 10 - KNTT
- Giải sgk Địa lí 10 - KNTT
- Giải sgk Lịch sử 10 - KNTT
- Giải sgk Kinh tế và Pháp luật 10 - KNTT
- Giải sgk Tin học 10 - KNTT
- Giải sgk Công nghệ 10 - KNTT
- Giải sgk Hoạt động trải nghiệm 10 - KNTT
- Giải sgk Giáo dục quốc phòng 10 - KNTT
- Lớp 10 - Chân trời sáng tạo
- Soạn văn 10 (hay nhất) - CTST
- Soạn văn 10 (ngắn nhất) - CTST
- Soạn văn 10 (siêu ngắn) - CTST
- Giải Toán 10 - CTST
- Giải sgk Vật lí 10 - CTST
- Giải sgk Hóa học 10 - CTST
- Giải sgk Sinh học 10 - CTST
- Giải sgk Địa lí 10 - CTST
- Giải sgk Lịch sử 10 - CTST
- Giải sgk Kinh tế và Pháp luật 10 - CTST
- Giải sgk Hoạt động trải nghiệm 10 - CTST
- Lớp 10 - Cánh diều
- Soạn văn 10 (hay nhất) - Cánh diều
- Soạn văn 10 (ngắn nhất) - Cánh diều
- Soạn văn 10 (siêu ngắn) - Cánh diều
- Giải sgk Toán 10 - Cánh diều
- Giải sgk Vật lí 10 - Cánh diều
- Giải sgk Hóa học 10 - Cánh diều
- Giải sgk Sinh học 10 - Cánh diều
- Giải sgk Địa lí 10 - Cánh diều
- Giải sgk Lịch sử 10 - Cánh diều
- Giải sgk Kinh tế và Pháp luật 10 - Cánh diều
- Giải sgk Tin học 10 - Cánh diều
- Giải sgk Công nghệ 10 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 10 - Cánh diều
- Giải sgk Giáo dục quốc phòng 10 - Cánh diều

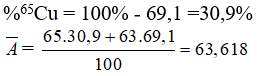





 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

