Bài tập về tính acid của carboxylic acid (cách giải + bài tập)
Chuyên đề phương pháp giải bài tập về tính acid của carboxylic acid lớp 11 chương trình sách mới hay, chi tiết với bài tập tự luyện đa dạng giúp học sinh ôn tập, biết cách làm bài tập về tính acid của carboxylic acid.
Bài tập về tính acid của carboxylic acid (cách giải + bài tập)
Thi online Hóa 11 KNTTThi online Hóa 11 CDThi online Hóa 11 CTST
A. Lý thuyết và phương pháp giải
Carboxylic acid thể hiện tính acid yếu. Bài toán thường gặp:
1. Carboxylic acid phản ứng với dung dịch kiềm:
- Tổng quát:
R(COOH)a + aNaOH → R(COONa)a + aH2O
số nhóm COOH =
- Với carboxylic acid đơn chức:
RCOOH + NaOH → RCOONa + H2O
- Áp dụng định luật bảo toàn khối lượng:
macid + mNaOH = mmuối + ()
- Giấm ăn là dung dịch acetic acid (CH3COOH) từ 2 – 5%.
2. Carboxylic acic phản ứng với muối carbonate:
- Với muối hydrogencarbonat
Tổng quát:
R(COOH)a + aNaHCO3 → R(COONa)a + aCO2↑ + aH2O
⇒ Số nhóm COOH =
Trường hợp acid đơn chức:
RCOOH + NaHCO3 → RCOONa + CO2↑ + H2O
⇒
- Với muối carbonat
2RCOOH + Na2CO3 → 2RCOONa + CO2↑ + H2O
2RCOOH + CaCO3 → (RCOO)2Ca + CO2↑ + H2O
B. Ví dụ minh hoạ
Ví dụ 1. Giấm được sử dụng khá phổ biến để chế biến thức ăn. Bạn Mai muốn xác định nồng độ acetic acid có trong giấm ăn bằng cách sử dụng dung dịch sodium hydroxyde 0,1M để chuẩn độ. Bạn lấy mẫu giấm ăn đó để làm thí nghiệm và kết quả chuẩn độ 3 lần như bảng sau:
Thí nghiệm |
Thể tích giấm (mL) |
Thể tích dung dịch NaOH 0,1 M cần dùng (mL) |
1 |
5,0 |
25,0 |
2 |
5,0 |
25,0 |
3 |
5,0 |
24,9 |
Hãy giúp bạn Mai xác định nồng độ mol của acetic acid trong giấm.
Hướng dẫn giải
Thể tích trung bình của dung dịch NaOH cần dùng:
Nồng độ acetic acid có trong giấm ăn là:
Ví dụ 2. Cho 4,32 gam acid hữu cơ X đơn chứa tác dụng hết với Na2CO3, thu được 5,64 gam muối của acid hữu cơ. Xác định công thức cấu tạo của X.
Hướng dẫn giải
Gọi công thức tổng quát của X là RCOOH.
Áp dụng phương pháp tăng giảm khối lượng, ta có:
(R + 44 + 23).x – (R + 45).x = 5,64 – 4,32 x = 0,06
R + 45 = = 72 R = 27 (C2H3-)
Vậy công thức cấu tạo của X là C2H3COOH hay CH2=CH-COOH.
C. Bài tập tự luyện
Câu 1. Cho dung dịch acetic acid có nồng độ x% tác dụng vừa đủ với dung dịch NaOH 20% thu được dung dịch muối sodium acetate có nồng độ 10,25%. Giá trị của X là
A. 10%.
B. 15%.
C. 18,67%.
D. 20%.
Hướng dẫn giải
Đáp án đúng là : A
Gọi a là số mol CH3COOH phản ứng.
Phương trình hóa học:
Câu 2: Để trung hòa 6,72 gam một carboxylic acid Y (no, đơn chức), cần dùng 200 gam dung dịch NaOH 2,24%. Công thức của Y là
A. C2H5COOH.
B. CH3COOH.
C. C3H7COOH.
D. HCOOH.
Hướng dẫn giải
Đáp án đúng là: B
RCOOH + NaOH → RCOONa + H2O
0,112 ← 0,112 mol
Câu 3: Trung hòa 10,4 gam carboxylic acid X bằng dung dịch NaOH, thu được 14,8 gam muối. Công thức của X là
A. C3H7COOH.
B. HOOC-CH2-COOH.
C. HOOC-COOH.
D. C2H5COOH.
Hướng dẫn giải
Đáp án đúng là: B
R(COOH)a + aNaOH → R(COONa)a + aH2O
Ta có: nacid = nmuối
Với a = 1 MR = 7 Vô lí.
Với a = 2 MR = 14 R là -CH2- X: HOOC – CH2 – COOH.
Câu 4. Cho 3,6 gam carboxylic acid no, đơn chức X tác dụng hoàn toàn với 500 mL dung dịch gồm KOH 0,12 M và NaOH 0,12 M. Cô cạn dung dịch thu được 8,28 gam hỗn hợp chất rắn khan. Công thức của X là
A. C2H5COOH.
B. CH3COOH.
C. HCOOH.
D. C3H7COOH.
Hướng dẫn giải
Đáp án đúng là: B
nNaOH = nKOH = 0,06 mol
BTKL:
MRCOOH = CH3COOH.
Câu 5: Trung hoà 5,48 gam hỗn hợp gồm acetic acid, phenol và benzoic acid cần dùng 600 mL dung dịch NaOH 0,1M. Cô cạn dung dịch sau phản ứng, thu được hỗn hợp chất rắn khan có khối lượng là
A. 8,64 gam.
B. 4,90 gam.
C. 6,80 gam.
D. 6,84 gam.
Hướng dẫn giải
Đáp án đúng là: C
nNaOH = 0,06 mol.
Tăng giảm khối lượng: mrắn khan = mhh + 22nNaOH = 5,48 + 22.0,06 = 6,8 gam.
Câu 6. Cho một dung dịch chứa 5,76 gam một carboxylic acid X đơn chức, mạch hở tác dụng hết với CaCO3 thu được 7,28 gam muối carboxylate. Công thức cấu tạo của X là
A.CH2=CHCOOH.
B. CH3COOH.
C.HC≡CCOOH.
D.CH3CH2COOH.
Hướng dẫn giải
Đáp án đúng là: A
Gọi công thức của X là RCOOH.
2RCOOH + CaCO3 (RCOO)2Ca + CO2 + H2O
Ta có: nacid = 2.nmuối
= 2. MR = 27 (C2H3- hay CH2=CH-)
Vậy X có công thức là: CH2=CHCOOH.
Câu 7: Hỗn hợp X gồm hai carboxylic acid đơn chức, đồng đẳng kế tiếp. Cho 5,4 gam X phản ứng hoàn toàn với dung dịch NaHCO3 dư, thu được 2,479 lít khí CO2 (đkc). Công thức của hai acid trong X là
A. C3H7COOH và C4H9COOH.
B. CH3COOH và C2H5COOH.
C. C2H5COOH và C3H7COOH.
D. HCOOH và CH3COOH.
Hướng dẫn giải
Đáp án đúng là: D
Gọi công thức chung của 2 acid là RCOOH.
Câu 8. Cho 30 gam hỗn hợp 3 acid gồm HCOOH, CH3COOH, CH2=CH-COOH tác dụng vừa hết với dung dịch NaHCO3 thu được 14,874 lít CO2 (đkc), khối lượng muối có trong dung dịch sau phản ứng là
A. 43,2 gam.
B. 56,4 gam.
C. 54 gam.
D. 43,8 gam.
Hướng dẫn giải
Đáp án đúng là: A
Gọi công thức chung của 3 acid là RCOOH
BTKL: 30 + 84.0,6 = mmuối = 0,6.44 + 0,6.18 Þ mmuối = 43,2 gam.
Câu 9. Hỗn hợp X gồm hai carboxylic acid đơn chức, đồng đẳng kế tiếp. Cho 6,5 gam X phản ứng hoàn toàn với dung dịch NaHCO3 dư, thu được 2,479 lít khí CO2 (đkc). Công thức của hai acid trong X là
A. C3H7COOH và C4H9COOH.
B. CH3COOH và C2H5COOH.
C. C2H5COOH và C3H7COOH.
D. HCOOH và CH3COOH.
Hướng dẫn giải
Đáp án đúng là: B
Gọi công thức chung của 2 acid là RCOOH.
Câu 10. Cho m gam một carboxylic acid X (mạch carbon không phân nhánh) tác dụng với NaHCO3 dư được 2,479 lít CO2 (đkc). Mặt khác, cũng m gam acid trên tác dụng với Ca(OH)2 dư được 9,1 gam muối. X là
A. formic acid.
B. acetic acid.
C. oxalic acid.
D. acrylic acid.
Hướng dẫn giải
Đáp án đúng là: D
X không phân nhánh Þ X là carboxylic đơn chức hoặc hai chức.
Trường hợp 1: X là carboxylic acid đơn chức.
Mmuối =
Vậy X là acrylic acid.
Đã chọn được đáp án đúng nên không cần xét trường hợp còn lại.
Thi online Hóa 11 KNTTThi online Hóa 11 CDThi online Hóa 11 CTST
Xem thêm các dạng bài tập Hóa học 11 hay, chi tiết khác:
- Bài tập về phản ứng tạo ether của alcohol
- Bài tập về phản ứng tách nước tạo alkene của alcohol
- Bài tập điều chế ethanol
- Bài toán điều chế phenol và dẫn xuất của phenol
- Bài toán về phản ứng tráng bạc của aldehyde
- Bài tập về phản ứng ester hóa
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 11 Global Success
- Giải sgk Tiếng Anh 11 Smart World
- Giải sgk Tiếng Anh 11 Friends Global
- Lớp 11 - Kết nối tri thức
- Soạn văn 11 (hay nhất) - KNTT
- Soạn văn 11 (ngắn nhất) - KNTT
- Giải sgk Toán 11 - KNTT
- Giải sgk Vật Lí 11 - KNTT
- Giải sgk Hóa học 11 - KNTT
- Giải sgk Sinh học 11 - KNTT
- Giải sgk Lịch Sử 11 - KNTT
- Giải sgk Địa Lí 11 - KNTT
- Giải sgk Giáo dục KTPL 11 - KNTT
- Giải sgk Tin học 11 - KNTT
- Giải sgk Công nghệ 11 - KNTT
- Giải sgk Hoạt động trải nghiệm 11 - KNTT
- Giải sgk Giáo dục quốc phòng 11 - KNTT
- Giải sgk Âm nhạc 11 - KNTT
- Lớp 11 - Chân trời sáng tạo
- Soạn văn 11 (hay nhất) - CTST
- Soạn văn 11 (ngắn nhất) - CTST
- Giải sgk Toán 11 - CTST
- Giải sgk Vật Lí 11 - CTST
- Giải sgk Hóa học 11 - CTST
- Giải sgk Sinh học 11 - CTST
- Giải sgk Lịch Sử 11 - CTST
- Giải sgk Địa Lí 11 - CTST
- Giải sgk Giáo dục KTPL 11 - CTST
- Giải sgk Hoạt động trải nghiệm 11 - CTST
- Giải sgk Âm nhạc 11 - CTST
- Lớp 11 - Cánh diều
- Soạn văn 11 Cánh diều (hay nhất)
- Soạn văn 11 Cánh diều (ngắn nhất)
- Giải sgk Toán 11 - Cánh diều
- Giải sgk Vật Lí 11 - Cánh diều
- Giải sgk Hóa học 11 - Cánh diều
- Giải sgk Sinh học 11 - Cánh diều
- Giải sgk Lịch Sử 11 - Cánh diều
- Giải sgk Địa Lí 11 - Cánh diều
- Giải sgk Giáo dục KTPL 11 - Cánh diều
- Giải sgk Tin học 11 - Cánh diều
- Giải sgk Công nghệ 11 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 11 - Cánh diều
- Giải sgk Giáo dục quốc phòng 11 - Cánh diều
- Giải sgk Âm nhạc 11 - Cánh diều

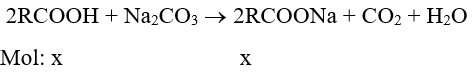
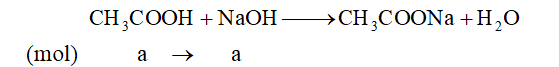
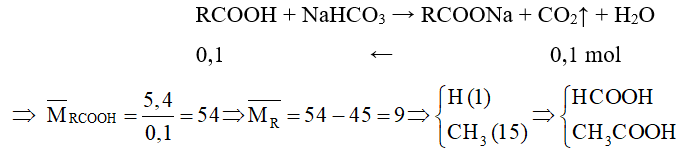
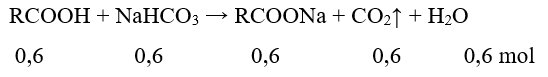
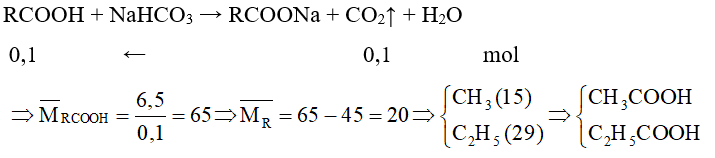
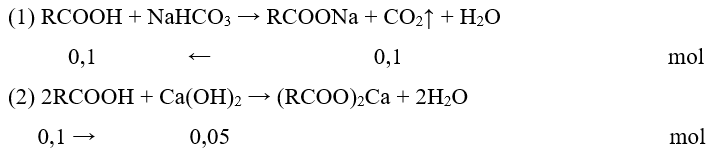





 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

