Phenol lớp 11 (Chuyên đề dạy thêm Hóa 11)
Tài liệu Phenol Hóa học lớp 11 gồm các dạng bài tập từ cơ bản đến nâng cao với phương pháp giải chi tiết và bài tập tự luyện đa dạng giúp Giáo viên có thêm tài liệu giảng dạy Hóa học 11.
Phenol lớp 11 (Chuyên đề dạy thêm Hóa 11)
Thi online Hóa 11 KNTTThi online Hóa 11 CDThi online Hóa 11 CTST
Xem thử chuyên đề Hóa học 11 KNTT
Chỉ từ 450k mua trọn bộ Chuyên đề dạy thêm Hóa học 11 (cả 3 sách) bản word có lời giải chi tiết:
- B1: gửi phí vào tk:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official - nhấn vào đây để thông báo và nhận giáo án
I. KHÁI NIỆM: Phenol là những hợp chất hữu cơ trong phân tử có nhóm -OH liên kết trực tiếp với nguyên tử carbon của vòng benzene.
II. ĐẶC ĐIỂM CẤU TẠO
- Trong phân tử phenol, liên kết O-H của phenol phân cực mạnh, nên phenol thể hiện tính acid yếu.
- Phenol có thể tham gia phản ứng thế nguyên tử hydrogen của vòng benzene.
III. TÍNH CHẤT VẬT LÍ
- Ở điều kiện thường, phenol là chất rắn không màu, nóng chảy ở 43 oC, sôi ở 181,8 oC.
- Phenol dễ bị chảy rữa khi để ngoài không khí ẩm
- Phenol tạo được liên kết H với nước, nhưng ít tan trong nước ở điều kiện thường, tan nhiều khi đun nóng (tan vô hạn ở 66oC), tan tốt trong các dung môi hữu cơ như ethanol, ether và acetone.
- Phenol rất độc, gây bỏng khi tiếp xúc với da.
IV. TÍNH CHẤT HÓA HỌC
1) Phản ứng thế nguyên tử H của nhóm -OH (tính acid của phenol)
- Trong dung dịch nước, phenol phân li theo cân bằng:
- Phenol là acid yếu, không làm đổi mày quỳ tím.
+ Tính acid: C6H5OH > H2CO3 (nấc 2): C6H5OH + Na2CO3 C6H5ONa + NaHCO3.
+ Tính acid: H2CO3 (nấc 1) > C6H5OH: C6H5ONa + CO2 + H2O C6H5OH + NaHCO3.
- Phenol có thể phản ứng được với kim loại kiềm, dung dịch base.
Ví dụ:
|
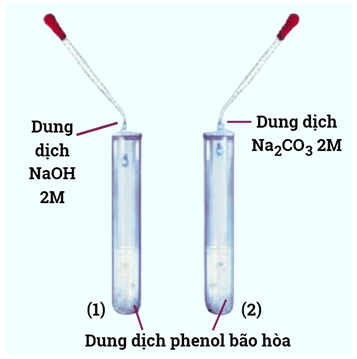
Thí nghiệm 1: Phenol phản ứng với dung dịch NaOH và với dung dịch Na2CO3. Dụng cụ: Ống nghiệm, ống hút nhỏ giọt, giá đỡ, găng tay, kính bảo hộ. Hóa chất: phenol, dung dịch NaOH 2 M, dung dịch Na2CO3 2M, nước cất. Tiến hành: Bước 1: Lắc đều hỗn hợp phenol lỏng với nước để tạo huyền phù. Lấy lần lượt 1 mL phenol dạng huyền phù cho vào ống nghiệm, đánh số thứ tự (1) và (2). |
|
|
Bước 2: Thêm tiếp 1 mL dung dịch NaOH vào ống nghiệm (1), 1 mL dung dịch Na2CO3 vào ống nghiệm (2). Lắc đều và để ổn định 2 ống nghiệm. Bước 3: Sục khí CO2 vào ống nghiệm (1) và ống nghiệm (2). Quảng cáo
Hiện tượng và các phương trình hóa học | |
Bước 1: Phenol ít tan trong nước ở điều kiện thường do đó ban đầu dung dịch có màu trắng đục.
Bước 2: Phenol phản ứng với các dung dịch NaOH, Na2CO3 tạo thành các muối tan nên sau phản ứng thu được dung dịch trong suốt.
Bước 3: Dung dịch trong hai ống nghiệm vẩn đục trở lại.
C6H5ONa + CO2 + H2O C6H5OH + NaHCO3.
5. Phản ứng thế ở vòng thơm
Phản ứng thế ưu tiên vào vị trí 2, 4 và 6 (ortho và para)
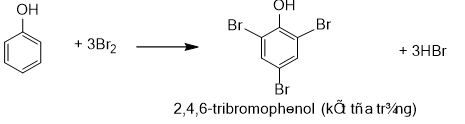
a)Phản ứng bromine hóa
Do ảnh hưởng của nhóm -OH, phản ứng thế nguyên tử của hydrogen ở vòng benzene của phenol xảy ra dễ dàng hơn so với benzene.
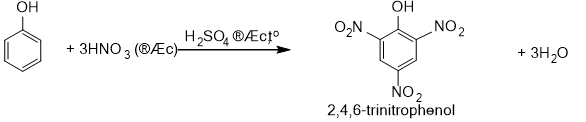
b)Phản ứng nitro hóa
6. Ứng dụng của phenol
- Dung dịch phenol ở nồng độ thấp được sử dụng như thuốc sát trùng, diệt nấm, vi khuẩn, vius, thuốc tăng trưởng thực vật.
- Sản xuất phẩm nhuộm, thuốc nổ (2,4,6-trinitrophenol), chất diệt cỏ, diệt nấm mốc.
- Sản xuất mĩ phẩm, tơ sợi, chất dẻo, tổng hợp dược phẩm (aspirin, paracetamol),…
7. Điều chế
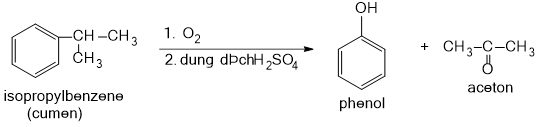
Phenol được tổng hợp từ cumene (isopropylbenzene) bằng phản ứng oxi hóa khử bởi oxygen rồi thủy phân trong môi trường acid thu được phenol và acetone
- Ngoài ra, phenol còn được điều chế từ nhựa than đá.
A. CÁC DẠNG CÂU HỎI TỰ LUẬN
Câu 1: Hãy giải thích tại sao phenol có thể phản ứng được với dung dịch NaOH còn alcohol thì không phản ứng với dung dịch NaOH
Câu 2: So sánh điều kiện phản ứng bromine hoá vào vòng benzene của phenol và benzene. Từ đó, rút ra nhận xét khả năng thế nguyên tử hydrogen của vòng benzene của phenol so với benzene.
Câu 3: Hãy xác định công thức cấu tạo của hợp chất hữu cơ X, biết X có công thức phân tử C7H8O, có chức vòng benzene và phản ứng được với dung dịch NaOH.
Câu 4: Hợp chất hữu cơ X thuộc loại phenol, có công thức phân tử là C8H10O. Số đồng phân cấu tạo của X là bao nhiêu
Câu 5: Viết phương trình hoá học của phản ứng xảy ra khi cho 4 – methylphenol tác dụng với nước bromine.
Câu 6: Cho các chất có công thức sau: C6H5OH, C6H5CH3, C6H5Cl và các giá trị nhiệt độ sôi (không theo thứ tự) là 110 oC, 132 oC, 182 oC. Hãy dự đoán nhiệt độ sôi tương ứng với mỗi chất trên. Giải thích.
Câu 7: a)Viết công thức phân tử và công thức cấu tạo của phenol đơn giản nhất.
b) Phenol phản ứng với dung dịch potassium hydroxide. Viết phương trình hóa học của phản ứng.
Câu 8: Viết công thức cấu tạo của các đồng phân phenol có công thức C7H8O. Gọi tên các đồng phân đó
Câu 9: Hãy dẫn ra các phương trình hóa học với bromine; dung dịch HNO3 (đặc) để chứng minh phản ứng thế nguyên tử H ở vòng benzene trong phenol dễ hơn benzene.
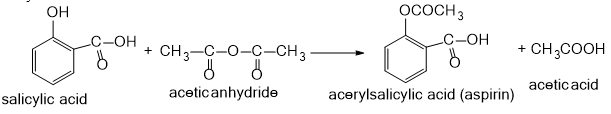
Câu 10: Aspirin được dùng trong dùng để hạ sốt và giảm đau nhẹ đến trung bình do tình trạng đau nhức cơ, răng, cảm lạnh đau đầu và sưng tấy do viêm khớp phương trình hóa học điều chế Aspirin từ salicylic acid
a) Salicylic acid chứa những nhóm chức nào?
b) Nhóm chức nào của salicylic acid đã tham gia phản ứng trên?
Câu 11: Thực hiện các thí nghiệm sau:
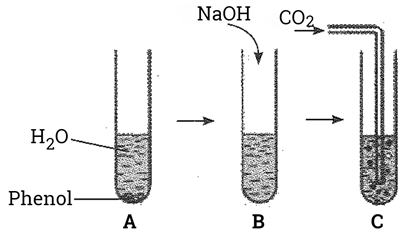
- Cho phenol vào ống nghiệm, thêm nước và lắc đều ống nghiệm thấy dung dịch có màu trắng đục (Hình A) .
- Cho dung dịch NaOH vào ống nghiệm thấy dung dịch chuyển sang trong suốt (Hình B) .
- Sục khí CO2 vào ống nghiệm thấy dung dịch chuyển màu trắng đục như ban đầu (Hình C) .
Giải thích hiện tượng trong các thí nghiệm trên và viết các phương trình hóa học.
Câu 12: Trình bày cách phân biệt các dung dịch sau: dung dịch phenol, dung dịch ethanol, dung dịch glycerol.
Câu 13: Picric acid có nhiều ứng dụng trong y học (định lượng creatinine để chấn đoản và theo dõi tình trạng suy thận, khử trùng và làm khô da khi điều trị bỏng,…), trong quân sự (sản xuất đạn, thuốc nổ,…), trong phòng thí nghiệm (nhuộm mẫu, làm thuốc thử,…).
a) Viết phương trình hóa học của phản ứng điều chế picric acid từ phenol.
b) Giải thích vì sao trong phòng thí nghiệm thường bảo quản picric acid trong lọ dưới một lớp nước và trong quá trình làm việc với picric acid, tránh để acid tiếp xúc với kim loại?
Câu 14: Cho các hợp chất hữu cơ có công thức cấu tạo sau:
Viết phương trình hóa học của phản ứng giữa hợp chất này với các chất sau:
a) Na; b) Dung dịch NaOH;
c) Dung dịch Na2CO3; d) Dung dịch bromine.
Câu 15: Picric acid (2,4,6-trinitrophenol) trước đây được sử dụng làm thuốc nổ. Để tổng hợp picric acid, người ta cho 47 g phenol phản ứng với hỗn hợp HNO3 đặc/H2SO4 đặc, dư. Tính khối lượng picric acid thu được, biết hiệu suất phản ứng là 65%.
Câu 16: Trong phân tử phenol có sự ảnh hưởng qua lại giữa nhóm –OH và gốc –C6H5; gốc –C6H5 làm tính acid của phenol mạnh hơn so với alcohol và nhóm –OH làm cho phản ứng thế nguyên tử hydrogen của vòng benzene dễ dàng hơn so với benzene. Hãy viết các phương trình phản ứng minh họa nhận định trên.
Câu 17: Trong công nghiệp, ngoài phương pháp điều chế từ cumene hoặc từ nhựa than đá, người ta còn thực hiện điều chế bằng phản ứng thủy phân dẫn xuất chlorobenzene với dung dịch NaOH đặc, ở nhiệt độ 3500C, áp suất cao (quy trình Dow), sản phẩm hữu cơ là muối sodium phenolate, acid hóa bằng dung dịch HCl, thu được phenol.
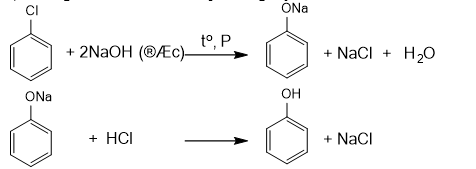
a) Viết phương trình hóa học của các phản ứng xảy ra.
b) Tại sao khi thủy phân chlobenzene không taọ thành sản phẩm trực tiếp phenol, mà tạo thành sodium phenolate?
Giải
a) Phương trình hóa học của các phản ứng xảy ra là
b) Chlorobenzene tác dụng NaOH, xảy ra phản ứng thế Cl bằng nhóm –OH tạo thành phenol, là một acid, phenol tác dụng với NaOH tạo thành muối sodium phenolate ngay sau đó.
Câu 18: Phân tử chất A có một nguyên tử oxygen và một vòng benzene. Trong A, phần trăm khối lượng các nguyên tố C, H và O lần lượt là: 77,78%; 7,41% và 14,81%.
a) Tìm công thức phân tử của A.
b) Cho một lượng chất A vào ống nghiệm đựng nước, thấy A không tan. Thêm tiếp dung dịch NaOH vào ống nghiệm, khuấy nhẹ, thấy A tan dần. Tìm công thức cấu tạo có thể có của A.
c) Chất B (phân tử có vòng benzene) là một trong số các đồng phân của A. Chất B không tác dụng với Na, không tác dụng với NaOH. Tìm công thức cấu tạo và gọi tên B.
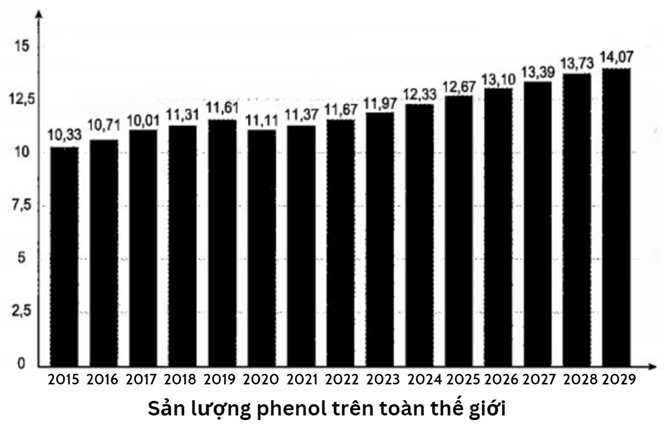
Câu 19: Thị trường tiêu thụ phenol trên thế giới khoảng 11,37 triệu tấn trong năm 2021, dự kiến sẽ tăng lên 14,07 triệu tấn vào năm 2029. Phenol được sử dụng để sản xuất nhiều loại hóa chất như bisphenol A, nhựa phenolfomaldehyde, picric acid và các chất khác. Khoảng 90% lượng phenol được sản xuất từ cumene (bằng phương pháp cumene, chu trình cumene,…).
Để cung cấp đủ sản lượng tiêu thụ của phenol trong năm 2021, khối lượng cumene đã đùng để sản xuất phenol là bao nhiêu? (Chỉ tính trên lượng phenol đã tiêu thụ, không bao gồm lượng cumene thực tế sản xuất phenol chưa tiêu thụ).
Câu 20:
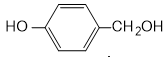
|
Trong vỏ quả cây vanilla có hợp chất mùi thơm dễ chịu, tên thường là vanillin. Công thức cấu tạo của vanillin là a) Viết công thức phân tử của vanillin. b) Dự đoán khả năng tan trong nước, trong ethanol và trong dung dịch kiềm như NaOH, KOH của vanillin. c) Mẫu vanillin đủ tiêu chuẩn dùng trong công nghiệp sản xuất dược phẩm và thực phẩm cần có trên 99% về khối lượng là vanillin. |
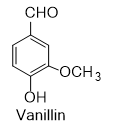 |
Để định lượng một mẫu vanillin, người ta làm như sau: Hòa tan 0,120 gam mẫu trong 20 mL ethanol 96% và thêm 60 mL nước cất, thu được dung dịch X. Biết X phản ứng vừa đủ với 7,82 mL dung dịch NaOH nồng độ 0,1M và tạp chất trong mẫu không phản ứng với NaOH. Mẫu vanillin trên có đủ tiêu chuẩn dùng trong công nghiệp sản xuất dược phẩm và thực phẩm không?
B. CÁC DẠNG CÂU HỎI TRẮC NGHIỆM
Câu 21: Phenol là hợp chất có chứa vòng benzene, công thức cấu tạo của phenol là
Câu 22: Ở điều kiện thường, chất tồn tại ở thể rắn là
A. ethanol.
B. benzene.
C. phenol.
D. toluene.
Câu 23: Chất nào sau đây là chất rắn ở điều kiện thường?
A.Phenol.
B. Ethanol.
C. toluene.
D. glycerol.
Câu 24: Phenol không phản ứng với chất nào sau đây?
A.NaHCO3.
B. Na.
C. NaOH.
D. Br2.
Câu 25: Trong các chất sau, chất nào thuộc loại phenol?
Câu 26: Trong nghiệp, phenol được điều chế chủ yếu từ chất nào sau đây?
A. benzene.
B. Cumene.
C. Chlorobenzene.
D. Than đá.
Câu 27: Phản ứng với chất/dung dịch nào sau đây chứng minh tính acid của phenol (C6H5OH) mạnh hơn ethanol?
A. Na.
B. Dung dịch NaOH.
C. Dung dịch bromine.
D. HNO3 đặc/H2SO4 đặc.
Câu 28: Phản ứng với chất/dung dịch nào sau đây chứng minh phenol (C6H5OH) có tính acid mạnh hơn nấc 2 của carbonic acid?
A. Na.
B. Dung dịch NaOH.
C. Dung dịch Na2CO3.
D. Dung dịch Br2.
Câu 29: Trong đặc điểm cấu tạo của phenol, cặp electron trên nguyên tử oxygen bị hút một phần vào hệ thống vòng benzene, làm giàu mật độ electron ở các vị trí
A.ortho, meta.
B. meta, para.
C. ortho, meta, para.
D. ortho, para.
................................
................................
................................
Thi online Hóa 11 KNTTThi online Hóa 11 CDThi online Hóa 11 CTST
Xem thêm Chuyên đề dạy thêm Hóa học lớp 11 các chủ đề hay khác:
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 11 Global Success
- Giải sgk Tiếng Anh 11 Smart World
- Giải sgk Tiếng Anh 11 Friends Global
- Lớp 11 - Kết nối tri thức
- Soạn văn 11 (hay nhất) - KNTT
- Soạn văn 11 (ngắn nhất) - KNTT
- Giải sgk Toán 11 - KNTT
- Giải sgk Vật Lí 11 - KNTT
- Giải sgk Hóa học 11 - KNTT
- Giải sgk Sinh học 11 - KNTT
- Giải sgk Lịch Sử 11 - KNTT
- Giải sgk Địa Lí 11 - KNTT
- Giải sgk Giáo dục KTPL 11 - KNTT
- Giải sgk Tin học 11 - KNTT
- Giải sgk Công nghệ 11 - KNTT
- Giải sgk Hoạt động trải nghiệm 11 - KNTT
- Giải sgk Giáo dục quốc phòng 11 - KNTT
- Giải sgk Âm nhạc 11 - KNTT
- Lớp 11 - Chân trời sáng tạo
- Soạn văn 11 (hay nhất) - CTST
- Soạn văn 11 (ngắn nhất) - CTST
- Giải sgk Toán 11 - CTST
- Giải sgk Vật Lí 11 - CTST
- Giải sgk Hóa học 11 - CTST
- Giải sgk Sinh học 11 - CTST
- Giải sgk Lịch Sử 11 - CTST
- Giải sgk Địa Lí 11 - CTST
- Giải sgk Giáo dục KTPL 11 - CTST
- Giải sgk Hoạt động trải nghiệm 11 - CTST
- Giải sgk Âm nhạc 11 - CTST
- Lớp 11 - Cánh diều
- Soạn văn 11 Cánh diều (hay nhất)
- Soạn văn 11 Cánh diều (ngắn nhất)
- Giải sgk Toán 11 - Cánh diều
- Giải sgk Vật Lí 11 - Cánh diều
- Giải sgk Hóa học 11 - Cánh diều
- Giải sgk Sinh học 11 - Cánh diều
- Giải sgk Lịch Sử 11 - Cánh diều
- Giải sgk Địa Lí 11 - Cánh diều
- Giải sgk Giáo dục KTPL 11 - Cánh diều
- Giải sgk Tin học 11 - Cánh diều
- Giải sgk Công nghệ 11 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 11 - Cánh diều
- Giải sgk Giáo dục quốc phòng 11 - Cánh diều
- Giải sgk Âm nhạc 11 - Cánh diều


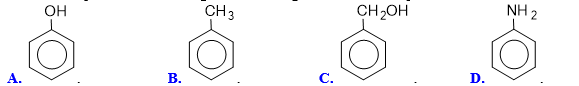
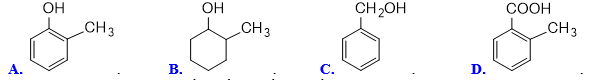





 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

