Cách giải Bài tập về Phenol trong đề thi Đại học (có lời giải)
Bài viết Cách giải Bài tập về Phenol trong đề thi Đại học với phương pháp giải chi tiết giúp học sinh ôn tập, biết cách làm bài tập về Phenol trong đề thi Đại học.
Cách giải Bài tập về Phenol trong đề thi Đại học (có lời giải)
Thi online Hóa 11 KNTTThi online Hóa 11 CDThi online Hóa 11 CTST
Phương pháp:
+ Tác dụng với Na
C6H5OH + Na → C6H5ONa + 1/2H2
+ Tác dụng với dung dịch kiềm
C6H5OH + NaOH → C6H5ONa + H2O
+ Phản ứng với dung dịch brom
C6H5OH + 3Br2 → C6H2Br3OH↓ + 3HBr
+ Phản ứng với nitric acid
Phản ứng thế nitro xảy ra tương tự phản ứng thế brom:
C6H5OH + 3HNO3 to→ C6H2(NO2)3OH + 3H2O
Ví dụ minh họa
Ví dụ 1 : Số hợp chất thơm có công thức phân tử C7H8O vừa tác dụng được với Na, vừa tác dụng với NaOH là
A. 1. B. 2. C. 3. D. 4.
Hướng dẫn giải:
Đáp án C
Hợp chất thơm vừa phản ứng được với Na, vừa phản ứng được với NaOH và phenol
Ứng với CTPT này có 5 đồng phân
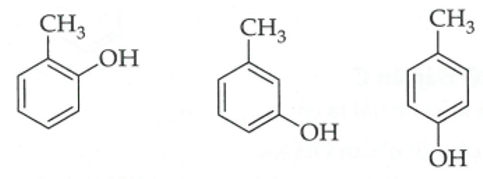
Ví dụ 2 : Số chất ứng với công thức phân tử C7H8O (là dẫn xuất của benzene) đều tác dụng được Na sinh khí H2 nhưng không tác dụng với dung dịch NaOH là
A. 2. B. 4. C. 3. D. 1.
Hướng dẫn giải:
Đáp án D
Phản ứng được với Na nhưng không phản ứng được với NaOH
Hợp chất có nguyên tử H linh động nhưng không thể hiện tính axit → OHancol
Có duy nhất cấu tạo thỏa mãn với điều kiện đề bài
Ứng với CTPT này có 5 đồng phân
Ví dụ 3 : X có công thức đơn giản nhất trùng với công thức phân tử. Số đồng phân cấu tạo thuộc loại hợp chất thơm ứng với công thức phân tử của X là
A. 5. B. 4 C. 6. D. 3.
Hướng dẫn giải:
Đáp án A
mC : mH : mO = 21 : 2 : 4
=> nC : nH : nO = 1,75 : 2 : 0,25 = 7 : 8 : 1
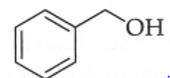
Ứng với CTPT này có 5 đồng phân:
Ví dụ 4 : Một dung dịch X chứa 5,4 gam chất đồng đẳng của phenol đơn chức. Cho dung dịch X phản ứng với nước brom (dư) thu được 17,25 gam hợp chất chứa ba nguyên tử brom trong phân tử, giả sử phản ứng xảy ra hoàn toàn. Công thức phân tử chất đồng đẳng của phenol là
A. C7H7OH. B. C8H9OH.
C. C9H11OH. D. C9H11OH.
Hướng dẫn giải:
Đáp án A
Gọi số mol Br2 là x mo1
Áp dụng BTKL:
5,4 + 160x = 17,25 + 81x => x = 0,15
=> nX = 0,05 mol
=> M = 5,4/0,05 = 108 => C7H7OH
Ví dụ 5 : Cho 15,5 gam hỗn hợp 2 phenol A và B liên tiếp nhau trong dãy đồng đẳng của phenol tác dụng vừa đủ với 0,5 lít dung dịch NaOH 0,3M. Công thức phân tử của 2 phenol và % khối lượng của hỗn hợp lần lượt là :
A. C7H7OH (69,68%) và C8H9OH (30,32%).
B. C6H5OH (69,68%) và C7H7OH (30,32%).
C. C6H5OH (30,32%) và C7H7OH(69,68%).
D. Kết quả khác.
Hướng dẫn giải:
Gọi công thức trung bình của 2 phenol là:
nNaOH = 0,15 mol;
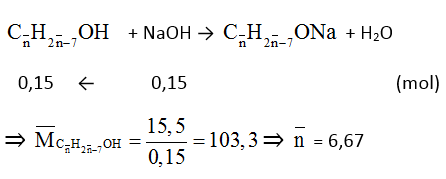
⇒ A: C6H5OH (x mol); B: C7H7OH (y mol)
Ta có: x + y = 0,15 mol;
94x + 108y= 15,5
⇒ x = 0,05 mol; y = 0,1 mol
%mC6H5OH = 0,05.94/15,5.100% = 30,32%
⇒ Đáp án C
Ví dụ 6 : Để điều chế axit picric, người ta cho 14,1 gam phenol tác dụng với HNO3 đặc, H2SO4 đặc. Biết lượng axit HNO3 đã lấy dư 25% so với lượng cần thiết. Số mol HNO3 cần dùng và khối lượng axit picric tạo thành là :
A. 0,5625 mol ; 34,75 gam. C. 0,5625 mol ; 34,35 gam.
B. 0,45 mol ; 42,9375 gam. D. 0,45 mol ; 42,9375 gam.
Hướng dẫn giải:
C6H5OH + 3HNO3 H2SO4→ C6H2(NO2)3OH(axit picric)+ 3H2O
Pt: 94 → 189 → 229 (g)
Theo đề bài m phenol = 14,1g
⇒ mHNO3 = 14,1.189/94 = 28,35g ⇒ nHNO3 = 0,45mol
⇒ nHNO3 dùng = 0,45 + 25%.0,45 = 0,5625 mol
maxit picric = 14,1.229/94 = 34,35g
⇒ Đáp án C
Ví dụ 7 : Một hỗn hợp X gồm ethyl alcohol và phenol tác dụng với Na dư cho ra hỗn hợp hai muối có tổng khối lượng là 25,2 gam. Cũng lượng hỗn hợp ấy tác dụng vừa đủ với 100 ml dung dịch NaOH 1M. Số mol của chất trong hỗn hợp X và thể tích H2 bay ra (đkc) trong phản ứng giữa X và Na là :
A. 0,2 mol ancol ; 0,1 mol phenol ; 3,36 lít H2.
B. 0,18 mol ancol ; 0,1 mol phenol ; 5,376 lít H2.
C. 0,1 mol ancol ; 0,1 mol phenol ; 2,24 lít H2.
D. 0,2 mol ancol ; 0,2 mol phenol ; 4,48 lít H2.
Hướng dẫn giải:
Khi tác dụng với Na:
C2H5OH + Na → C2H5ONa + 1/2 H2
x y 0,5y (mol)
C6H5OH + Na → C6H5ONa + 1/2 H2
y y 0,5y (mol)
mmuối = mC2H5ONa + mC6H5ONa = 68x + 116y = 25,2g (1)
Khi tác dụng với NaOH, chỉ có phenol tác dụng:
C6H5OH + NaOH → C6H5ONa + H2O
nC6H5OH = nNaOH = 0,1 mol = y
⇒ x = 0,2 mol; VH2 = 22,4.0,5(x+y) = 3,36 lít⇒ Đáp án A
Thi online Hóa 11 KNTTThi online Hóa 11 CDThi online Hóa 11 CTST
Xem thêm các dạng bài tập Hóa học lớp 11 có trong đề thi Tốt nghiệp THPT khác:
- 2 dạng bài tập Dẫn xuất halogen trong đề thi Đại học (có lời giải)
- 6 dạng bài tập về Ancol trong đề thi Đại học (có lời giải)
- Dạng 1: Bài tập lý thuyết về dẫn xuất halogen, ancol, phenol
- Dạng 2: Cách viết đồng phân, gọi tên dẫn xuất halogen
- Dạng 3: Cách viết đồng phân, gọi tên Ancol, Phenol
- Dạng 4: Bài tập về dẫn xuất halogen
- Dạng 5: Ancol phản ứng với kim loại kiềm
- Dạng 6: Phenol phản ứng với kim loại kiềm và dung dịch kiềm
- Dạng 7: Phản ứng tách nước của Ancol
- Dạng 8: Phản ứng oxi hóa ancol
- Dạng 9: Độ rượu - Điều chế, nhận biết Ancol
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 11 Global Success
- Giải sgk Tiếng Anh 11 Smart World
- Giải sgk Tiếng Anh 11 Friends Global
- Lớp 11 - Kết nối tri thức
- Soạn văn 11 (hay nhất) - KNTT
- Soạn văn 11 (ngắn nhất) - KNTT
- Giải sgk Toán 11 - KNTT
- Giải sgk Vật Lí 11 - KNTT
- Giải sgk Hóa học 11 - KNTT
- Giải sgk Sinh học 11 - KNTT
- Giải sgk Lịch Sử 11 - KNTT
- Giải sgk Địa Lí 11 - KNTT
- Giải sgk Giáo dục KTPL 11 - KNTT
- Giải sgk Tin học 11 - KNTT
- Giải sgk Công nghệ 11 - KNTT
- Giải sgk Hoạt động trải nghiệm 11 - KNTT
- Giải sgk Giáo dục quốc phòng 11 - KNTT
- Giải sgk Âm nhạc 11 - KNTT
- Lớp 11 - Chân trời sáng tạo
- Soạn văn 11 (hay nhất) - CTST
- Soạn văn 11 (ngắn nhất) - CTST
- Giải sgk Toán 11 - CTST
- Giải sgk Vật Lí 11 - CTST
- Giải sgk Hóa học 11 - CTST
- Giải sgk Sinh học 11 - CTST
- Giải sgk Lịch Sử 11 - CTST
- Giải sgk Địa Lí 11 - CTST
- Giải sgk Giáo dục KTPL 11 - CTST
- Giải sgk Hoạt động trải nghiệm 11 - CTST
- Giải sgk Âm nhạc 11 - CTST
- Lớp 11 - Cánh diều
- Soạn văn 11 Cánh diều (hay nhất)
- Soạn văn 11 Cánh diều (ngắn nhất)
- Giải sgk Toán 11 - Cánh diều
- Giải sgk Vật Lí 11 - Cánh diều
- Giải sgk Hóa học 11 - Cánh diều
- Giải sgk Sinh học 11 - Cánh diều
- Giải sgk Lịch Sử 11 - Cánh diều
- Giải sgk Địa Lí 11 - Cánh diều
- Giải sgk Giáo dục KTPL 11 - Cánh diều
- Giải sgk Tin học 11 - Cánh diều
- Giải sgk Công nghệ 11 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 11 - Cánh diều
- Giải sgk Giáo dục quốc phòng 11 - Cánh diều
- Giải sgk Âm nhạc 11 - Cánh diều

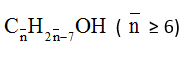





 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

