Chuyên đề Khí lí tưởng lớp 12 (Chuyên đề dạy thêm Vật Lí 12)
Tài liệu chuyên đề Khí lí tưởng lớp 12 trong Chuyên đề dạy thêm Vật Lí 12 gồm các dạng bài tập từ cơ bản đến nâng cao với phương pháp giải chi tiết và bài tập tự luyện đa dạng giúp Giáo viên có thêm tài liệu giảng dạy Vật Lí 12.
Chuyên đề Khí lí tưởng lớp 12 (Chuyên đề dạy thêm Vật Lí 12)
Chỉ từ 300k mua trọn bộ Chuyên đề dạy thêm Vật Lí 12 (sách mới) bản word có lời giải chi tiết:
- B1: gửi phí vào tk:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official - nhấn vào đây để thông báo và nhận giáo án
Chủ đề 1: Mô hình động học phân tử chất khí
I – Tóm tắt lý thuyết
1. Chuyển động và tương tác của các phân tử khí
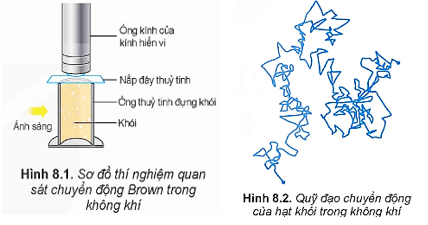
a. Chuyển động Brown trong chất khí.
Chuyển động Brown không chỉ xảy ra trong chất lỏng mà xảy ra cả trong chất khí.
Kết luận:
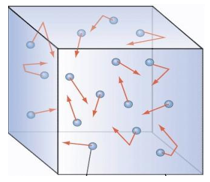
- Chất khí được cấu tạo từ các phân tử chuyển động hỗn loạn, không ngừng.
- Nhiệt độ của khí càng cao thì tốc độ chuyển động hỗn loạn của các phân tử khí càng lớn.
Ở điều kiện tiêu chuẩn (T = 273K và p = 1atm), các phân tử khí chuyển động với tốc độ trung bình khoảng 400m/s.
b. Tương tác giữa các phân tử khí
Giữa các phân tử khí cũng có lực đẩy và lực hút, gọi chung là lực liên kết. Vì khoảng cách giữa các phân tử khí rất lớn nên lực liên kết giữa các phân tử khí rât yếu so với thể lỏng và thể rắn.
2. Mô hình động lực học phân tử chất khí
Nội dung mô hình động học phân tử chất khí:
- Chất khí được cấu tạo từ các phân tử có kích thước rất nhỏ so với khoảng cách giữa chúng.
- Các phân tử khí chuyển động hỗn loạn không ngừng; chuyển động này càng nhanh thì nhiệt độ chất khí càng cao.
- Khi chuyển động hỗn loạn các phân tử khí va chạm vào thành bình tác dụng lực, gây áp suất lên thành bình.
3. Khí lí tưởng
Ta có thể coi một chất khí ở điều kiện nhiệt độ và áp suất khí quyển bình thường gần đúng là một khí lí tưởng.
Mô hình khí lí tưởng gồm các nội dung sau:
- Các phân tử khí ở xa nhau, khoảng cách giữa chúng rất lớn so với kích thước mỗi phân tử nên có thể bỏ qua kích thước của chúng.
- Khi chưa va chạm, lực tương tác giữa các phân tử khí rất yếu, nên có thể bỏ qua.
- Giữa hai va chạm liên tiếp, phân tử khí lí tưởng chuyển động thẳng đều.
- Khi va chạm vào thành bình chứa, phân tử khí truyền động lượng cho thành bình và bị bật ngược trở lại.
Va chạm của các phân tử khí với nhau và với thành bình là va chạm hoàn toàn đàn hồi.
4. Lượng chất
Lượng chất chứa trong một vật được xác định dựa vào số phân tử được chứa trong vật đó.
Đơn vị đo lượng chất là mol và được định nghĩa như sau:
Mol là lượng chất trong đó chứa số phân tử (hoặc nguyên tử) bằng
NA ≈ 6,02.1023 mol-1
NA được gọi là số Avogadro (số phân tử trong 1 mol chất).
Khối lượng mol của một chất là khối lượng của 1 mol chất đó, được kí hiệu là M.
Như vậy, nếu một mẫu vật chất có khối lượng m, chứa N phân tử thì số mol n của mẫu vật đó được xác định:
Thể tích của một mol một chất gọi là thể tích mol của chất ấy ở đktc (0°C, 1atm). Thể tích mol của mọi chất khí đều bằng nhau và bằng 22,4 lít (0, 0224 m3).
Chủ đề 2: Định luật Boyle
Dạng 1 - Xác định áp suất và thể tích trong quá trình đẳng nhiệt
I – Tóm tắt lý thuyết
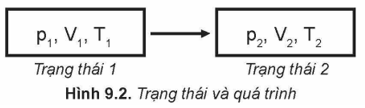
1. Các thông số trạng thái của một lượng khí
- Trạng thái của một lượng khí được xác định bằng 3 thông số trang thái: Áp suất (p); Thể tích (V); Nhiệt độ (T)
T là nhiệt độ tuyệt đối (K): T (K) = toC + 273
- Lượng khí có thể chuyển từ trạng thái này sang trạng thái khác bằng các quá trình biến đổi trạng thái. Khi biến đổi trạng thái mà còn một thông số không đổi thì các quá trình này gọi là đẳng quá trình.
2. Định luật Boyle
- Quá trình đẳng nhiệt: là quá trình biến đổi trạng thái của một khối lượng khí xác định trong đó nhiệt độ được giữ không đổi.
- Định luật Boyle:
Khi nhiệt độ của một khối lượng khí xác định giữ không đổi thì áp suất gây ra bởi khí tỉ lệ nghịch với thể tích của nó
Biểu thức: pV = hằng số
Trong đó : p là áp suất (mmHg, bar, atm, Pa, N/m2 )
V là thể tích (lít = dm3, m3, cm3, mm3 )
Chú ý :
- Nếu gọi p1, V1 là áp suất và thể tích của một lượng khí ở trạng thái 1
- p2, V2 là áp suất và thể tích của một lượng khí ở trạng thái 2
Thì theo định luật Boyle ta có: p1V1 = p2V2.
Đơn vị đổi:
1atm = 1bar = 760mmHg = 105Pa = 105N/m2
1m3 = 103dm3 = 103lít = 106cm3 = 109 mm3
Một số ví dụ về quá trình đẳng nhiệt trong đời sống:
Chủ đề 3: Định luật Charles
I – Tóm tắt lý thuyết
1. Quá trình đẳng áp:
Quá trình biến đổi trạng thái của một khối lượng khí xác định khi giữ áp suất không đổi gọi là quá trình đẳng áp.
2. Định luật Charles
- Nội dung định luật: Khi áp suất của một khối lượng khí xác định giữ không đổi thì thể tích của khí tỉ lệ thuận với nhiệt độ tuyệt đối của nó.
- Biểu thức:
Nếu gọi V1, T1 lần lượt là thể tích, nhiệt độ tuyệt đối ở trạng thái 1; V2, T2 lần lượt là thể tích, nhiệt độ tuyệt đối ở trạng thái 2 thì:
Đồ thị biểu diễn định luật Charles:
3. Chú ý
- Khí lí tưởng tuân theo đúng định luật Boyle và Charles.
- Khí thực ở điều kiện bình thường (áp suất không quá lớn, nhiệt độ không quá thấp) có thể coi gần đúng tuân theo định luật Boyle và Charles.
- Nội năng của khí lí tưởng chỉ phụ thuộc vào nhiệt độ: n mol khí lí tưởng có nhiệt độ thay đổi từ T1 đến T2 thì nội năng của nó biến thiên một lượng ΔU = n.c.(T2 - T1); trong đó c là nhiệt dung riêng phân tử (đẳng tích) của chất khí.
II – Bài tập luyện tập
1. Câu trắc nhiệm nhiều phương án lựa chọn ( 4,5 điểm )
Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
(Mỗi câu trả lời đúng thí sinh được 0,25điểm)
Câu 1: Trong quá trình nung nóng đẳng áp một khối lượng khí xác định, khoảng cách giữa các phân tử khí
A. tăng lên.
B. giảm đi.
C. không đổi.
D. giảm đến cực tiểu rồi tăng lên.
Câu 2: Trong hệ toạ độ V - T, đường biểu diễn nào sau đây là đường đẳng áp?
A. Đường thẳng song song với trục hoành.
B. Đường thẳng song song với trục tung.
C. Đường hypebol.
D. Đường thẳng kéo dài đi qua gốc tọa độ.
Câu 3: Quá trình biến đổi trạng thái trong đó áp suất được giữ không đổi gọi là quá trình
A. đẳng áp
B. đẳng tích.
C. đẳng nhiệt
D. đoạn nhiệt.
Câu 4: Giữ áp suất của một khối lượng khí nhất định không đổi và giảm nhiệt độ thì khối lượng riêng của khí
A. tăng lên.
B. giảm đi.
C. không đổi.
D. tăng đến cực đại rồi giảm đi.
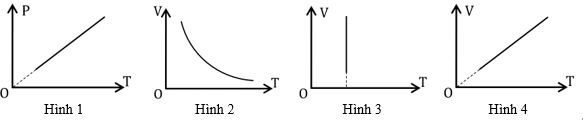
Câu 5: Đồ thị nào sau đây phù hợp với quá trình đẳng áp?
A. hình 2
B. hình 1
C. hình 4
D. hình 3
................................
................................
................................
Xem thêm Chuyên đề dạy thêm Vật Lí lớp 12 các chương hay khác:
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 12 Global Success
- Giải sgk Tiếng Anh 12 Smart World
- Giải sgk Tiếng Anh 12 Friends Global
- Lớp 12 Kết nối tri thức
- Soạn văn 12 (hay nhất) - KNTT
- Soạn văn 12 (ngắn nhất) - KNTT
- Giải sgk Toán 12 - KNTT
- Giải sgk Vật Lí 12 - KNTT
- Giải sgk Hóa học 12 - KNTT
- Giải sgk Sinh học 12 - KNTT
- Giải sgk Lịch Sử 12 - KNTT
- Giải sgk Địa Lí 12 - KNTT
- Giải sgk Giáo dục KTPL 12 - KNTT
- Giải sgk Tin học 12 - KNTT
- Giải sgk Công nghệ 12 - KNTT
- Giải sgk Hoạt động trải nghiệm 12 - KNTT
- Giải sgk Giáo dục quốc phòng 12 - KNTT
- Giải sgk Âm nhạc 12 - KNTT
- Giải sgk Mĩ thuật 12 - KNTT
- Lớp 12 Chân trời sáng tạo
- Soạn văn 12 (hay nhất) - CTST
- Soạn văn 12 (ngắn nhất) - CTST
- Giải sgk Toán 12 - CTST
- Giải sgk Vật Lí 12 - CTST
- Giải sgk Hóa học 12 - CTST
- Giải sgk Sinh học 12 - CTST
- Giải sgk Lịch Sử 12 - CTST
- Giải sgk Địa Lí 12 - CTST
- Giải sgk Giáo dục KTPL 12 - CTST
- Giải sgk Tin học 12 - CTST
- Giải sgk Hoạt động trải nghiệm 12 - CTST
- Giải sgk Âm nhạc 12 - CTST
- Lớp 12 Cánh diều
- Soạn văn 12 Cánh diều (hay nhất)
- Soạn văn 12 Cánh diều (ngắn nhất)
- Giải sgk Toán 12 Cánh diều
- Giải sgk Vật Lí 12 - Cánh diều
- Giải sgk Hóa học 12 - Cánh diều
- Giải sgk Sinh học 12 - Cánh diều
- Giải sgk Lịch Sử 12 - Cánh diều
- Giải sgk Địa Lí 12 - Cánh diều
- Giải sgk Giáo dục KTPL 12 - Cánh diều
- Giải sgk Tin học 12 - Cánh diều
- Giải sgk Công nghệ 12 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 12 - Cánh diều
- Giải sgk Giáo dục quốc phòng 12 - Cánh diều
- Giải sgk Âm nhạc 12 - Cánh diều




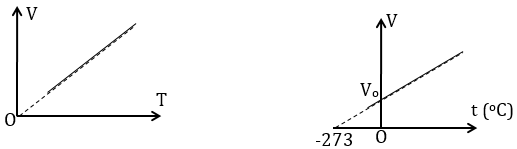





 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

