Lý thuyết Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng (Hóa 10 Chân trời sáng tạo Bài 15)
Với tóm tắt lý thuyết Hóa học 10 Bài 15: Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng sách Chân trời sáng tạo hay nhất, chi tiết sẽ giúp học sinh lớp 10 nắm vững kiến thức trọng tâm, ôn luyện để học tốt môn Hóa 10.
Lý thuyết Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng (Hóa 10 Chân trời sáng tạo Bài 15)
(199k) Xem Khóa học Hóa 10 CTST
I. Tốc độ phản ứng
1. Khái niệm tốc độ phản ứng hóa học
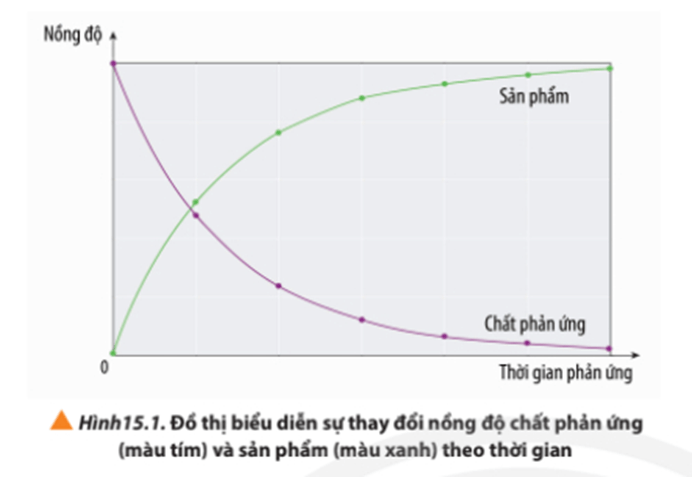
- Tốc độ phản ứng của phản ứng hóa học là đại lượng đặc trưng cho sự biến thiên nồng độ của một trong các chất phản ứng hoặc sản phẩm trong một đơn vị thời gian.
- Tốc độ phản ứng kí hiệu là v, có đơn vị: (đơn vị nồng độ)/ (đơn vị thời gian).
- Tốc độ trung bình của phản ứng là tốc độ được tính trong một khoảng thời gian phản ứng.
2. Tính tốc độ trung bình của phản ứng hóa học
- Cho phản ứng tổng quát: aA + bB → cC + dD
Biểu thức tốc độ trung bình của phản ứng:
Trong đó:
: tốc độ trung bình của phản ứng
∆C = C2 – C1: sự biến thiên nồng độ
∆t = t2 – t1 : biến thiên thời gian
C1, C2 là nồng độ của một chất tại hai thời điểm tương ứng t1 và t2.
- Ví dụ: Trong phản ứng hóa học: Mg (s) + 2HCl (aq) → MgCl2 (aq) + H2 (g)
Sau 40 giây, nồng độ của dung dịch HCl giảm từ 0,8M về còn 0,6M. Tốc độ trung bình của phản ứng theo nồng độ HCl trong 40 giây là:
II. Biểu thức tốc độ phản ứng
- Các phản ứng diễn ra với tốc độ khác nhau tùy thuộc vào nhiều yếu tố: nồng độ, nhiệt độ, áp suất đối với chất tham gia là chất khí, bề mặt tiếp xúc, chất xúc tác, cường độ ánh sáng, thể của chất, dung môi hòa tan các chất phản ứng, …
- Năm 1864, hai nhà bác học Guldberg và Waage khi nghiên cứu sự phụ thuộc của tốc độ vào nồng độ đã đưa ra định luật tác dụng khối lượng: Ở nhiệt độ không đổi, tốc độ phản ứng tỉ lệ với tích số nồng độ các chất tham gia phản ứng với số mũ thích hợp.
- Biểu thức tốc độ phản ứng:
Xét phản ứng đơn giản có dạng: aA + bB → cC + dD
+ Mối quan hệ giữa nồng độ và tốc độ tức thời của phản ứng hóa học được biểu diễn bằng biểu thức:
+ Trong đó:
k là hằng số tốc độ phản ứng;
CA; CB là nồng độ (M) chất A, B tại thời điểm đang xét.
- Ví dụ: Xét phản ứng:
2CO (g) + O2 (g) 2CO2 (g)
Biểu thức tốc độ tức thời của phản ứng viết theo định luật là:
Chú ý:
+ Khi nồng độ chất phản ứng bằng đơn vị (1M) thì k = v, vậy k là tốc độ phản ứng và được gọi là tốc độ riêng, đây là ý nghĩa của hằng số tốc độ phản ứng.
+ Hằng số k chỉ phụ thuộc vào bản chất của chất phản ứng và nhiệt độ.
+ Định luật tác dụng khối lượng chỉ đúng cho các phản ứng đơn giản, đó là phản ứng một chiều, chỉ qua một giai đoạn từ chất phản ứng tạo ra sản phẩm.
(199k) Xem Khóa học Hóa 10 CTST
Xem thêm tóm tắt lý thuyết Hóa học lớp 10 Chân trời sáng tạo hay khác:
Lý thuyết Hóa 10 Bài 13: Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học
Lý thuyết Hóa 10 Bài 14: Tính biến thiên enthalpy của phản ứng hóa học
Lý thuyết Hóa 10 Bài 16: Các yếu tố ảnh hưởng đến tốc độ phản ứng hóa học
Lý thuyết Hóa 10 Bài 17: Tính chất vật lí và hóa học các đơn chất nhóm VIIA
Lý thuyết Hóa 10 Bài 18: Hydrogen halide và một số phản ứng của ion halide
Xem thêm các tài liệu học tốt lớp 10 hay khác:
- Giải sgk Hóa học 10 Chân trời sáng tạo
- Giải Chuyên đề Hóa học 10 Chân trời sáng tạo
- Giải SBT Hóa học 10 Chân trời sáng tạo
- Giải lớp 10 Chân trời sáng tạo (các môn học)
- Giải lớp 10 Kết nối tri thức (các môn học)
- Giải lớp 10 Cánh diều (các môn học)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Soạn văn 10 (hay nhất) - CTST
- Soạn văn 10 (ngắn nhất) - CTST
- Soạn văn 10 (siêu ngắn) - CTST
- Giải Toán 10 - CTST
- Giải Tiếng Anh 10 Global Success
- Giải Tiếng Anh 10 Friends Global
- Giải sgk Tiếng Anh 10 iLearn Smart World
- Giải sgk Tiếng Anh 10 Explore New Worlds
- Giải sgk Vật lí 10 - CTST
- Giải sgk Hóa học 10 - CTST
- Giải sgk Sinh học 10 - CTST
- Giải sgk Địa lí 10 - CTST
- Giải sgk Lịch sử 10 - CTST
- Giải sgk Kinh tế và Pháp luật 10 - CTST
- Giải sgk Hoạt động trải nghiệm 10 - CTST






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

