Lý thuyết Đại cương về polymer (Hóa 12 Cánh diều Bài 8)
Với tóm tắt lý thuyết Hóa 12 Bài 8: Đại cương về polymer sách Cánh diều hay nhất, chi tiết sẽ giúp học sinh lớp 12 nắm vững kiến thức trọng tâm, ôn luyện để học tốt môn Hóa học 12.
Lý thuyết Đại cương về polymer (Hóa 12 Cánh diều Bài 8)
I. KHÁI NIỆM VÀ DANH PHÁP
1. Khái niệm
Polymer là những hợp chất có khối lượng phân tử lớn, do nhiều đơn vị nhỏ (còn gọi là mắt xích) liên kết với nhau tạo nên.
Ví dụ: Polyethylene: 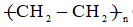
Chú ý:
- Hệ số n được gọi là hệ số polymer hóa hay độ polymer hóa. Giá trị của n còng lớn, phân tử khối của polymer càng cao. Vì vật liệu polymer thường là hỗn hợp của nhiều phân tử polymer có hệ số polymer hoá khác nhau nên người ta hay dùng khái niệm hệ số polymer hoá trung bình.
- Các phân tử phản ứng với nhau tạo nên polymer được gọi là monomer.
2. Danh pháp
- Tên của polymer được hình thành như sau:
- Khi tên của monomer gồm hai từ trở lên hoặc polymer được hình thành từ hai loại monomer trở lên thì tên của monomer được đặt trong dấu ngoặc đơn.
II. TÍNH CHẤT VẬT LÍ
- Ở điều kiện thường, hầu hết những polymer là những chất rắn và không bay hơi. Các polymer có nhiệt độ nóng chảy nằm trong một khoảng khá rộng.
- Đa số các polymer nóng chảy tạo thành chất lỏng nhớt, khi để nguội sẽ rắn lại được gọi là chất nhiệt dẻo (PE, PP, PVC,…). Một số polymer khi đun nóng không nóng chảy mà bị phân huỷ gọi là chất nhiệt rắn (PPF,…).
- Đa số các polymer không tan trong dung môi thông thường. Một số polymer tan được trong dung môi thích hợp, tạo ra dung dịch nhớt.
- Mỗi polymer có tính chất cơ lí riêng, từ đó được ứng dụng làm những vật liệu khác nhau:
|
Polymer |
Tính chất cơ lí |
Ứng dụng |
|
PE, PP |
Tính dẻo |
Chế tạo chất dẻo |
|
Polyisoprene |
Tính đàn hồi |
Chế tạo cao su |
|
Capron; nylon-6,6 |
Kéo thành sợi dai, bền |
Chế tạo tơ |
|
Poly(methyl methacrylate) |
Trong suốt, không giòn |
Chế tạo thuỷ tinh hữu cơ |
|
PE, PVC, PPF |
Cách điện, cách nhiệt |
Chế tạo vật liệu cách điện, cách nhiệt |
III. TÍNH CHẤT HOÁ HỌC
Polymer có thể tham gia các phản ứng giữ nguyên mạch, phân cắt mạch hoặc tăng mạch.
1. Phản ứng giữ nguyên mạch polymer
- Các nhóm thế gắn vào mạch polymer có thể tham gia phản ứng mà không làm thay đổi mạch polymer.
Ví dụ: Poly(vinyl acetate) bị thuỷ phân trong môi trường kiềm.
- Những polymer có liên kết đôi trong mạch có thể tham gia phản ứng cộng vào liên kết đôi mà không làm thay đổi mạch polymer.
Ví dụ: Polyisoprene phản ứng với hydrogen chloride
2. Phản ứng cắt mạch polymer
- Các polymer có nhóm chức trong mạch dễ bị thuỷ phân, chẳng hạn tinh bột, cellulose, capron, nylon-6,6,…
Ví dụ:
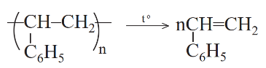
- Một số polymer bị phân huỷ nhiệt thành các polymer mạch ngắn, cuối cùng tạo ra monomer ban đầu. Phản ứng này được gọi là phản ứng depolymer hoá
Ví dụ:
3. Phản ứng tăng mạch polymer
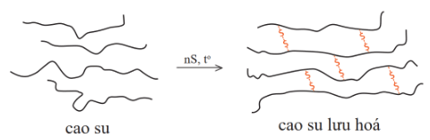
- Ở điều kiện thích hợp (về nhiệt độ, áp suất và có mặt xúc tác), các mạch polymer có thể phản ứng với nhau để tạo thành mạch dài hơn hoặc tạo thành mạng lưới (như phản ứng lưu hoá cao su).
- Phản ứng nối các mạch polymer lại với nhau thành mạng không gian được gọi là phản ứng khâu mạch polymer. Polymer khâu mạch có mạng không gian nên khó nóng chảy, khó hoà tan và bền hơn so với polymer chưa khâu mạch.
IV. ĐIỀU CHẾ
Polymer thường được điều chế bằng phản ứng trùng hợp hoặc trùng ngưng.
1. Phản ứng trùng hợp
- Phản ứng trùng hợp là phản ứng kết hợp nhiều phân tử nhỏ (monomer) giống nhau hay tương tự nhau tạo thành phân tử lớn (polymer).
Ví dụ:
- Điều kiện về cấu tạo của monomer có thể tham gia phản ứng trùng hợp là trong phân tử phải có các liên kết bội hoặc vòng kém bền.
2. Phản ứng trùng ngưng
- Phản ứng trùng ngưng là quá trình kết hợp nhiều phân tử nhỏ (monomer) lại thành phân tử lớn (polymer), đồng thời giải phóng phân tử nhỏ khác (ví dụ H2O).
Ví dụ:
- Điều kiện về cấu tạo để monomer tham gia phản ứng trùng ngưng là trong phân tử phải có ít nhất hai nhóm chức có khả năng phản ứng để tạo liên kết.
Xem thêm tóm tắt lý thuyết Hóa học lớp 12 Cánh diều hay khác:
Xem thêm các tài liệu học tốt lớp 12 hay khác:
- Giải sgk Hóa học 12 Cánh diều
- Giải Chuyên đề học tập Hóa 12 Cánh diều
- Giải SBT Hóa học 12 Cánh diều
- Giải lớp 12 Cánh diều (các môn học)
- Giải lớp 12 Kết nối tri thức (các môn học)
- Giải lớp 12 Chân trời sáng tạo (các môn học)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Soạn văn 12 Cánh diều (hay nhất)
- Soạn văn 12 Cánh diều (ngắn nhất)
- Giải sgk Toán 12 Cánh diều
- Giải Tiếng Anh 12 Global Success
- Giải sgk Tiếng Anh 12 Smart World
- Giải sgk Tiếng Anh 12 Friends Global
- Giải sgk Vật Lí 12 - Cánh diều
- Giải sgk Hóa học 12 - Cánh diều
- Giải sgk Sinh học 12 - Cánh diều
- Giải sgk Lịch Sử 12 - Cánh diều
- Giải sgk Địa Lí 12 - Cánh diều
- Giải sgk Giáo dục KTPL 12 - Cánh diều
- Giải sgk Tin học 12 - Cánh diều
- Giải sgk Công nghệ 12 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 12 - Cánh diều
- Giải sgk Giáo dục quốc phòng 12 - Cánh diều
- Giải sgk Âm nhạc 12 - Cánh diều

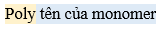

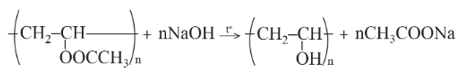
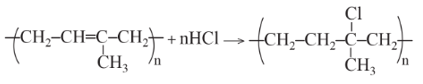
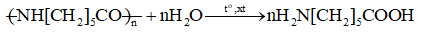
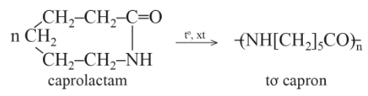
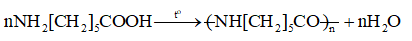





 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

