Cách hoàn thành phương trình hóa học về Halogen (hay, chi tiết)
Bài viết Cách hoàn thành phương trình hóa học về Halogen với phương pháp giải chi tiết giúp học sinh ôn tập, biết cách làm bài tập Cách hoàn thành phương trình hóa học về Halogen.
Cách hoàn thành phương trình hóa học về Halogen (hay, chi tiết)
Thi online Hóa 10 KNTTThi online Hóa 10 CDThi online Hóa 10 CTST
A. Phương pháp & Ví dụ
Lý thuyết và Phương pháp giải
- Nắm vững các tính chất hóa học của các halogen và hợp chất của chúng
- Một số tính chất đặc trưng cần lưu ý:
+ Halogen là những phi kim điển hình. Đi từ flo đến iot, tính oxi hoá giảm dần. Các halogen đứng trước đẩy halogen đứng sau nó ra khỏi dung dịch muối halogen.
+ Flo có độ âm điện lớn nhất nên trong tất cả các hợp chất chỉ có số oxi hoá 1. Các nguyên tố halogen khác, ngoài số oxi hoá –1 còn có các số oxi hoá +1, +3, +5, +7.
+ Tính khử của HX: Tăng dần từ HF < HCl < HBr < HI.
+ Tính axit của dung dịch HX: Tính axit tăng dần từ HF < HCl < HBr < HI.
+ Tính axit của HXO4 : Giảm dần từ HClO4 > HBrO4 > HIO4.
Ví dụ minh họa
Ví dụ 1. Hoàn thành chuỗi phản ứng sau:
a) MnO2 → Cl2 → HCl → Cl2 → CaCl2 → Ca(OH) 2 → Clorua vôi
b, KMnO4 → Cl2 → KCl → Cl2 → hypochlorous acid
→ NaClO → NaCl → Cl2 → FeCl3
Lời giải:
a, MnO2 + 4HCl → MnCl2 + Cl2 + 2H2 O
H2 + Cl2 → 2HCl
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2 O
Ca + Cl2 → CaCl2
CaCl2 + NaOH → Ca(OH)2 + NaCl
Cl2 + Ca(OH) 2 → CaOCl2 + H2O
b, 2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2 O
Cl2 + 2K → 2 KCl
2KCl → 2K + Cl2
Cl + H2 O → HCl+ HClO
Cl2 + 2NaOH → NaCl + NaClO + H2 O
NaClO + 2HCl → Cl2 + NaCl + H2 O
2NaCl + 2H2 O → H2 + 2NaOH + Cl2
2Fe + 3Cl2 → 2FeCl3
Ví dụ 2. Cân bằng các phản ứng oxi hóa – khử sau:
a) KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O
b) KClO3 + HCl → KCl + Cl2 + H2O
c) KOH + Cl2 → KCl + KClO3 + H2O
d) Cl2 + SO2 + H2O → HCl + H2SO4
e) Fe3O4 + HCl → FeCl2 + FeCl3 + H2O
f) CrO3 + HCl → CrCl3 + Cl2 + H2O
g) Cl2 + Ca(OH) 2 → CaCl2 + Ca(OCl)2 + H2O
Lời giải:
a, 2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2 O
b, KClO3 + 6HCl → KCl + 3Cl2 + 3H2 O
c, 6KOH + 3Cl2 → 5KCl + KClO3 + 3H2 O
d, Cl2 + SO2 + 2H2O → 2HCl + H2 SO4
e, Fe3 O4 + 8HCl → FeCl2 + 2FeCl3 + 4H2O
f, 2CrO3 + 12HCl → 2CrCl3 + 3Cl2 + 6H2 O
g, 2Cl2 + 2Ca(OH) 2 → CaCl2 + Ca(OCl)2 + 2H2O
Ví dụ 3: Hoàn thành các phương trình hóa học theo sơ đồ sau, ghi rõ điều kiện phản ứng(nếu có):
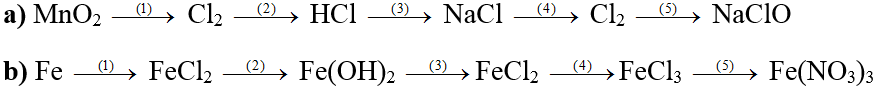
Lời giải:
a, 1. MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
2. Cl2 + SO2 + 2H2 O → 2HCl + H2SO4
3. 2Na + 2HCl → 2NaCl + H2
4. 2NaCl + 2H2 O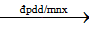
5. Cl2 + 2NaOH → NaCl + NaClO + H2 O
b, 1. Fe + HCl → FeCl2 + H2
2. FeCl2 + NaOH → Fe(OH) 2 + NaCl
3. Fe(OH) 2 + 2HCl → FeCl2 + 2H2O
4. 2FeCl2 + Cl2 → 2FeCl3
5. FeCl3 + 3AgNO3 → Fe(NO3)3 + 3AgCl
B. Bài tập trắc nghiệm
Câu 1. Viết phương trình hóa học của phản ứng thực hiện các biến hóa dưới đây, ghi tên các chất và điều kiện của phản ứng.
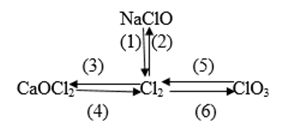
Lời giải:
Đáp án:
(1 ) Cl2 + 2NaOH → NaCl + NaClO + H2O
(2) NaClO + 2HCl → NaCl + Cl2 + H2O
(3) Cl2 + Ca(OH)2 rắn → CaOCl2 + H2O
(4) CaOCl2 + 2HCl → CaCl2 + Cl2 + H2O
(5) 3Cl2 + 6KOH → 5KCl + KClO3 + 3H2O
(6) KClO3 +6HCl → 3Cl2 + KCl + 3 H2O
Câu 2. Hoà tan khí Cl2 vào dung dịch KOH đặc, nóng, dư. Dung dịch thu được có các chất thuộc dãy nào dưới đây ?
A. KCl, KClO3, Cl2. B. KCl, KClO3, KOH, H2O.
C. KCl, KClO, KOH, H2O. D. KCl, KClO3.
Lời giải:
Đáp án: B
3Cl2+ 6 KOH → 5KCl + KClO3 + 3H2O
Câu 3. Hoà tan khí Cl2 vào dung dịch KOH loãng, nguội, dư. Dung dịch thu được có các chất thuộc dãy nào dưới đây ?
A. KCl, KClO3, Cl2. B. KCl, KClO3, KOH, H2O.
C. KCl, KClO, KOH, H2O. D. KCl, KClO3.
Lời giải:
Đáp án: C
Cl2+ 2 KOH → KCl + KClO + 3H2O
Câu 4. Cho các chất sau : KOH (1), Zn (2), Ag (3), Al(OH)3 (4), KMnO4 (5), K2SO4 (6). Axit HCl tác dụng được với các chất :
A. (1), (2), (4), (5). B. (3), (4), (5), (6).
C. (1), (2), (3), (4). D. (1), (2), (3), (5).
Lời giải:
Đáp án: A
HCl + KOH → KCl + H2O
Zn + 2HCl → ZnCl2 + H2
Al(OH)3 + 3HCl → AlCl3 + 3H2O
2KMnO4 + 16HCl → 5Cl2 + 2KCl + 2MnCl2 +8 H2O
Câu 5. Cho các chất sau : CuO (1), Zn (2), Ag (3), Al(OH)3 (4), KMnO4 (5), PbS (6), MgCO3 (7), AgNO3 (8), MnO2 (9), FeS (10). Axit HCl không tác dụng được với các chất :
A. (1), (2). B. (3), (4). C. (5), (6). D. (3), (6).
Lời giải:
Đáp án: D
Do Ag đứng sau H2 trong dãy hoạt động hóa học nên không tác dụng được với axit HCl vàH2SO4 loãng
PbS là muối không tan trong axit nên không phản ứng
FeS cũng là muối không tan nhưng tan được trong axit.
*Một số lưu ý về muối sunfua
- Tan trong nước: Na2S, K2S, (NH4)2S, BaS,…
- Không tan trong nước nhưng tan trong HCl, H2SO4 loãng: FeS, ZnS, MnS,…
- Không tan trong nước và không tan trong HCl, H2SO4 loãng: CuS, PbS, Ag2S, SnS, CdS, HgS…
- Không tồn tại trong nước: MgS, Al2S3, …
Câu 6. Cho các phản ứng :
(1) O3 + dung dịch KI →
(2) F2 + H2O -to→
(3) MnO2 + HCl đặc -to→
(4) Cl2 + dung dịch H2S →
Các phản ứng tạo ra đơn chất là :
A. (1), (2), (3). B. (1), (3), (4).
C. (2), (3), (4). D. (1), (2), (4).
Lời giải:
Đáp án: A
(1) O3 + 2KI + H2O → I2 + O2 + 2KOH
(2) 2F2 + 2H2O -to→ O2 + 4HF
(3) MnO2 + 4HCl đặc -to→ Cl2 + MnCl2 + 2H2O
(4) 4Cl2 + H2S + 4H2O → H2SO4 + 8HCl
Câu 7. Cho sơ đồ chuyển hóa:
Fe3O4 + dung dịch HI (dư) X + Y + H2O
Biết X và Y là sản phẩm cuối cùng của quá trình chuyển hóa. Các chất X và Y là :
A. Fe và I2. B. FeI3 và FeI2.
C. FeI2 và I2. D. FeI3 và I2.
Lời giải:
Đáp án: C
Fe3O4 + 8 HI 3FeI2 + I2 + 4H2O
Câu 8. Cho sơ đồ:
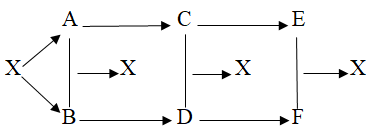
Viết các phản ứng xảy ra theo sơ đồ trên với X là NaCl.
Lời giải:
Đáp án:
2NaCl -đp→ 2Na + Cl2
2Na + Cl2 → 2NaCl
2Na + 2H2O → 2NaOH + H2
Cl2 + H2 → 2HCl
NaOH + HCl → NaCl + H2O
2NaOH + H2SO4 → Na2SO4 + 2H2O
2HCl + Ba(OH)2 → BaCl2 + 2H2O
Na2SO4 + BaCl2 → BaSO4↓ + 2NaCl
C. Bài tập tự luyện
Câu 1: Viết các phương trình phản ứng xảy ra (nếu có) khi lần lượt cho các cặp chất sau tác dụng với nhau:
a) NaCl + ZnBr2.
b) HBr + NaI.
c) AgNO3 + ZnBr2.
d) HCl + Fe(OH)2.
Câu 2: Sục khí Cl2 qua dung dịch Na2CO3 thấy có khí CO2 thoát ra. Hãy viết phương trình hóa học của các phản ứng xảy ra.
Câu 3: Hoàn thành chuỗi phản ứng sau:
Câu 4: Một mol chất nào sau đây khi tác dụng với HCl cho lượng chlorine lớn nhất?
A. MnO2.
B. KMnO4.
C. KClO3.
D. CaOCl2.
Câu 5: Phản ứng nào sau đây không xảy ra?
A. H2O + F2 →
B. KBr + Cl2 →
C. KBr + I2 →
D. KI + Br2 →
Thi online Hóa 10 KNTTThi online Hóa 10 CDThi online Hóa 10 CTST
Xem thêm các dạng bài tập Hóa học lớp 10 có trong đề thi Tốt nghiệp THPT khác:
Để học tốt lớp 10 các môn học sách mới:
- Giải bài tập Lớp 10 Kết nối tri thức
- Giải bài tập Lớp 10 Chân trời sáng tạo
- Giải bài tập Lớp 10 Cánh diều
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 10 Global Success
- Giải Tiếng Anh 10 Friends Global
- Giải sgk Tiếng Anh 10 iLearn Smart World
- Giải sgk Tiếng Anh 10 Explore New Worlds
- Lớp 10 - Kết nối tri thức
- Soạn văn 10 (hay nhất) - KNTT
- Soạn văn 10 (ngắn nhất) - KNTT
- Soạn văn 10 (siêu ngắn) - KNTT
- Giải sgk Toán 10 - KNTT
- Giải sgk Vật lí 10 - KNTT
- Giải sgk Hóa học 10 - KNTT
- Giải sgk Sinh học 10 - KNTT
- Giải sgk Địa lí 10 - KNTT
- Giải sgk Lịch sử 10 - KNTT
- Giải sgk Kinh tế và Pháp luật 10 - KNTT
- Giải sgk Tin học 10 - KNTT
- Giải sgk Công nghệ 10 - KNTT
- Giải sgk Hoạt động trải nghiệm 10 - KNTT
- Giải sgk Giáo dục quốc phòng 10 - KNTT
- Lớp 10 - Chân trời sáng tạo
- Soạn văn 10 (hay nhất) - CTST
- Soạn văn 10 (ngắn nhất) - CTST
- Soạn văn 10 (siêu ngắn) - CTST
- Giải Toán 10 - CTST
- Giải sgk Vật lí 10 - CTST
- Giải sgk Hóa học 10 - CTST
- Giải sgk Sinh học 10 - CTST
- Giải sgk Địa lí 10 - CTST
- Giải sgk Lịch sử 10 - CTST
- Giải sgk Kinh tế và Pháp luật 10 - CTST
- Giải sgk Hoạt động trải nghiệm 10 - CTST
- Lớp 10 - Cánh diều
- Soạn văn 10 (hay nhất) - Cánh diều
- Soạn văn 10 (ngắn nhất) - Cánh diều
- Soạn văn 10 (siêu ngắn) - Cánh diều
- Giải sgk Toán 10 - Cánh diều
- Giải sgk Vật lí 10 - Cánh diều
- Giải sgk Hóa học 10 - Cánh diều
- Giải sgk Sinh học 10 - Cánh diều
- Giải sgk Địa lí 10 - Cánh diều
- Giải sgk Lịch sử 10 - Cánh diều
- Giải sgk Kinh tế và Pháp luật 10 - Cánh diều
- Giải sgk Tin học 10 - Cánh diều
- Giải sgk Công nghệ 10 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 10 - Cánh diều
- Giải sgk Giáo dục quốc phòng 10 - Cánh diều

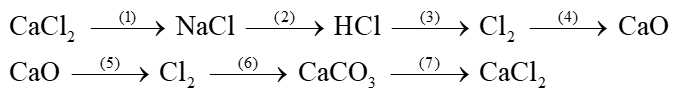





 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

