100 câu trắc nghiệm hydrocarbon không no có lời giải (nâng cao - phần 2)
Với 100 câu trắc nghiệm hydrocarbon không no (nâng cao - phần 2) có lời giải chi tiết sẽ giúp học sinh ôn tập, biết cách làm câu trắc nghiệm hydrocarbon không no (nâng cao - phần 2).
100 câu trắc nghiệm hydrocarbon không no có lời giải (nâng cao - phần 2)
Thi online Hóa 11 KNTTThi online Hóa 11 CDThi online Hóa 11 CTST
Bài giảng: Phương pháp giải bài toán đốt cháy hydrocarbon - Cô Nguyễn Thị Nhàn (Giáo viên VietJack)
Bài 1: Đốt cháy hoàn toàn 2,24 lít khí X (đktc) gồm buta–1,3–diene và etan sau đó dẫn toàn bộ sản phẩm cháy hấp thụ vào dung dịch H2SO4 đặc thì khối lượng dung dịch axit tăng thêm bao nhiêu gam ?
A. 3,6 g. B. 5,4 g. C. 9,0 g. D. 10,8 g.
Lời giải:
Đáp án B
Hướng dẫn
nH2O = 3.nX = 3.0,1 = 0,3 mol ⇒ m↑ = mH2O = 0,3.18 = 5,4 gam
Bài 2: Đốt cháy hoàn toàn m gam alkanediene X, thu được 11,2 lít CO2 (đktc) và 5,4 gam H2O. Cho m gam X tác dụng với dung dịch Br2, số mol Br2 tối đa tham gia phản ứng là
A. 0,10mol B. 0,20 mol
C. 0,30mol D. 0,05mol
Lời giải:
Đáp án B
Hướng dẫn
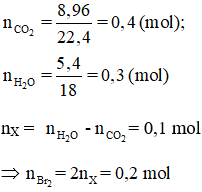
Bài 3: Một hỗn hợp khí X gồm 2 olefin là đồng đẳng kế tiếp nhau. Nếu cho 1,792 lít hỗn hợp X (ở 0℃, 2,5 at) qua bình chứa dung dịch brom thì thấy khối lượng của bình tăng lên 7 gam. Công thức phân tử của 2 olefin là:
A. C2H4 và C3H6
B. C3H6 và C4H8
C. C3H8 và C3H6
D. C4H8 và C5H10
Lời giải:
Đáp án A
Hướng dẫn
Số mol của hỗn hợp:
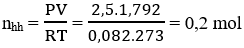
Khối lượng bình brom tăng = khối lượng hỗn hợp
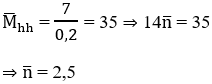
⇒ 2 alkene là C2H4 và C3H6
Bài 4: 2,24 lít hỗn hợp X gồm buta–1,3–diene và penta–1–3-diene (đktc) có thể tác dụng hết tối đa bao nhiêu lít dung dịch brom 0,10 M ?
A. 2 lít. B. 1 lít.
C. 1,5 lít. D. 2,5 lít.
Lời giải:
Đáp án A
Hướng dẫn nBr2 = 2nX = 0,2 mol ⇒ VBr2 = 0,2/0,1 = 2 lít
Bài 5: Hỗn hợp khí X gồm H2 và một alkene có khả năng cộng HBr cho sản phẩm hữu cơ duy nhất. Tỉ khối của X so với hidro bằng 0,1. Đun nóng X có xúc tác Ni, sau khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Y không làm mất màu nước brom; tỉ khối của Y so với H2 bằng 13. Công thức cấu tạo của alkene là:
A. CH3 – CH = CH – CH3
B. CH2 = CH – CH2 – CH3
C. CH2 = C(CH3)2
D. CH2 = CH2
Lời giải:
Đáp án A
Hướng dẫn
Giả sử có 1 mol hỗn hợp X gồm H2 và alkene : CnH2n
Ta có:
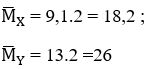
Áp dụng ĐLBTKL ta có: mhh X = mhh Y ⇔ 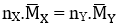
⇔ 1.18,2 = nY.26 ⇒ nY = 0,7 mol.
Phương trình phản ứng:
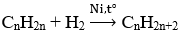
Ta có: nX = 1 mol; nY= 0,7 mol
⇒ Số mol H2 pứ = số mol CnH2n = 1 - 0,7 = 0,3 mol
⇒ số mol H2 ban đầu = 0,3 + 0,4 = 0,7 mol
Ta có: 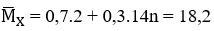
X + HBr cho 1 sản phẩm duy nhất ⇒ X là but-2-en
Bài 6: Hỗn hợp khí X gồm 0,3 mol H2 và 0,1 mol propen. Nung X một thời gian với xúc tác Ni thu được hỗn hợp khí Y có tỉ khối so với H2 là 16. Tính số mol H2 phản ứng?
A. 0,15 mol B. 0,2 mol
C. 0,25 mol D. 0,3 mol
Lời giải:
Đáp án C
Hướng dẫn
mX = 0,3.2 + 0,1.42 = 4,8 g ⇒ nY = 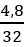
Bài 7: Hỗn hợp X gồm C2H2 và H2 có cùng số mol. Lấy một lượng hỗn hợp X cho qua chất xúc tác nung nóng, thu được hỗn hợp Y gồm C2H4, C2H6, C2H2 và H2. Sục Y vào dung dịch brom (dư) thì khối lượng bình brom tăng 10,8 gam và thoát ra 4,48 lít hỗn hợp khí (đktc) có tỉ khối so với H2 là 8. Thể tích O2(đktc) cần để đốt cháy hoàn toàn hỗn hợp Y là:
A. 33,6 lít. B. 22,4 lít.
C. 44,8 lít. D. 26,88 lít.
Lời giải:
Đáp án A
Hướng dẫn mX = 10,8 + 16.0,2 = 14 g
mX = mC2H2 + mH2 = 26x + 2x = 28x = 14 ⇒ x = 0,5 mol;
nO2 = 0,5nH2 + 2,5nC2H2 = 0,5 + 2,5.0,5 = 1,5 mol ⇒ V = 33,6 lít
Bài 8: Đốt cháy hoàn toàn 1 thể tích A gồm C2H6 và C2H2 thu được CO2 và H2O có tỉ lệ mol là 1:1. Phần trăm thể tích mỗi khí trong hỗn hợp đầu lần lượt là
A. 50%, 50% B. 30%, 70%
C. 25% ,75% D. 70% ,30%
Lời giải:
Đáp án A
Hướng dẫn
Giả sử nA = 1 mol ; nC2H6 = x và nC2H2 = y; nH2O = nCO2 = 2 mol; x + y = 1 và 3x + y = 2 ⇒ x = 0,5 và y = 0,5 ⇒ %V = % số mol
Bài 9: Hỗn hợp X gồm propin và alkyne A có tỉ lệ mol 1:1. Lấy 0,3 mol X tác dụng với dd AgNO3/NH3 dư thu được 46,2 gam kết tủa. Vậy A là:
A. acetylene B. but-2-yne.
C. But-1-yne D. Pent-1-yne.
Lời giải:
Đáp án C
Hướng dẫn
npropin = nA = 0,15 mol; m↓ = 0,15.147 + m↓A ⇒ m↓A = 46,2 – 22,05 = 22,05 ⇒ M↓ = 22,05/0,15 = 161 ⇒ alkyne A là: C4H6 (but-1-yne)
Bài 10: Cho hỗn hợp X gồm alkene và hiđro có tỉ khối so với heli bằng 3,33. Cho X đi qua bột niken nung nóng đến khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp Y có tỉ khối so với heli là 4. CTPT của X là :
A. C2H4 B. C3H6.
C. C4H8 D. C5H10
Lời giải:
Đáp án D
Hướng dẫn
Vì 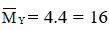
Áp dụng định luật bảo toàn khối lượng ta có :
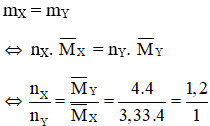
Chọn nX = 1,2 mol và nY =1 mol ⇒ nH2 (pư) = nCnH2n = nX – nY = 0,2 mol
⇒ Ban đầu trong X có 0,2 mol CnH2n và 1 mol H2
Ta có : 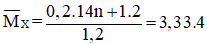
Bài 11: 1 mol hydrocarbon X đốt cháy cho ra 5 mol CO2, 1mol X phản ứng với 2 mol AgNO3/NH3. Xác định CTCT của X.
A. CH2=CH-CH2-C≡C-H
B. HC≡C-CH2- C≡C-H
C. CH2=CH-CH=CH-CH3
D. CH2=C=CH-CH-CH2
Lời giải:
Đáp án B
Hướng dẫn
CTPT X là CxHy; x = 5 ⇒ có 5 nguyên tử C; X có 2 liên kết 3 ở đầu mạch.
Bài 12: Đốt cháy hoàn toàn 4,48 lít hỗn hợp C2H4 và C3H6 có tỉ khối hơi so với oxi là 1,09375, rồi cho toàn bộ sản phẩm vào 500ml dung dịch NaOH 1,8M thì thu được sản phẩm và nồng độ mol tương ứng là:
A. NaHCO3 0,2M và Na2CO3 0,8M
B. Na2CO3 0,6M và NaOH 0,1M dư.
C. NaHCO3 0,02M và Na2CO3 0,8M
D. Chỉ thu được Na2CO3 0,4M.
Lời giải:
Đáp án A
Hướng dẫn Dựa vào tỉ khối ta tính được khối lượng mỗi chất và số mol
nCO2 = 0,2.2,5 = 0,5 (mol) và nNaOH = 0,9 mol
Tỉ lệ: 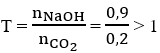
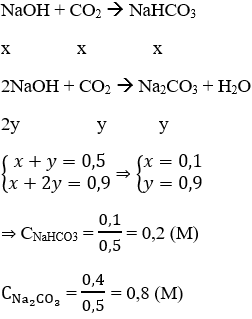
Bài 13: Hỗn hợp X gồm H2, C2H4 và C3H6 có tỉ khối so với H2 là 9,25. Cho 22,4 lít X (đktc) vào bình kín có sẵn một ít bột Ni. Đun nóng bình một thời gian, thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 10. Tổng số mol H2 đã phản ứng là
A. 0,070 mol B. 0,015 mol
C. 0,075 mol D. 0,050 mol
Lời giải:
Đáp án C
Hướng dẫn mX = 18,5.1 = 18,5 g; nY = 18,5/20 = 0,925 mol ⇒ nH2 pư = 1 – 0,925 = 0,075 mol
Bài 14: Cho hydrocarbon X phản ứng với brom(trong dung dịch) theo tỷ lệ mol 1 : 1 thì được chất hữu cơ Y(chứ 74,08% brom về khối lượng). Khi X phản ứng với HBr thì thu được hai sản phẩm hữu cơ khác nhau. Tên gọi của X là
A. but-1-en B.etilen
C. but-2-en D. propilen
Lời giải:
Đáp án A
Hướng dẫn X + Br2 → Y (CxHyBr2)
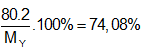
Do phản ứng với HCl tạo 2 sp khác nhau nên X là but-1-en
Bài 15: Cho 3,12 gam alkyne X phản ứng với 0,1 mol H2 (xúc tác Pd/PbCO3, to), thu được hỗn hợp Y chỉ có hai hydrocarbon. Công thức phân tử của X là
A. C2H2 B. C5H8 C. C4H6 D. C3H4.
Lời giải:
Đáp án A
Hướng dẫn
nalkyne > 0,1 mol; MX < 31,2 ⇒ X là C2H2
Bài 16: Dẫn 8,96 lít hỗn hợp khí X gồm methane và etilen vào dung dịch brom dư, thấy dung dịch nhạt màu và còn lại 2,24 lít khí thoát ra. (Thể tích các khí đều do(đktc)). Thành phần phần trăm thể tích của methane trong X là
A. 25,0% B. 50,0%
C. 60,0% D. 37,5%
Lời giải:
Đáp án A
Hướng dẫn
Chất khí thoát ra là CH4 ⇒ thể tích CH4 là 2,24 lít
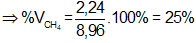
Bài 17: Đốt cháy hoàn toàn m gam hydrocarbon ở thể khí, mạch hở, nhẹ hơn không khí thu được 7,04 gam CO2. Sục m gam hydrocarbon này vào nước brom dư đến khi phản ứng hoàn toàn, thấy có 25,6 gam brom phản ứng. Giá trị của m là:
A. 2 gam B. 4 gam.
C. 10 gam D. 2,08 gam
Lời giải:
Đáp án D
Hướng dẫn
Hydrocarbon là C2H2 (vì M < Mkk; nBr2 = 2nalkyne)
nBr2 = 0,16 mol; nCO2 = 0,16 mol; nalkyne = 0,08 mol; m = 0,08.26 = 2,08 gam.
Bài 18: Dẫn 11,2 lít hh khí X (gồm acetylene và propin) vào dd AgNO3/NH3 dư (các phản ứng xảy ra hoàn toàn), sau phản ứng thu được 92,1 gam kết tủa. % số mol của acetylene trong X là.
A.70% B. 30% C. 60% D. 40%
Lời giải:
Đáp án D
Hướng dẫn
Gọi số mol của acetylene và propin lần lượt là: x và y mol; x + y = 0,5 mol; 240x + 147y = 92,1 ⇒ x = 0,2 và y = 0,3 ; %nacetylene = 0,2.100%/0,5 = 40%
Bài 19: Cho H2 và 1 olefin có thể tích bằng nhau qua niken đun nóng ta được hỗn hợp A. Biết tỉ khối hơi của A đối với H2 là 23,2. Hiệu suất phản ứng hiđro hoá là 75%. Công thức phân tử olefin là :
A. C2H4 B. C3H6.
C. C4H8 D. C5H10.
Lời giải:
Đáp án C
Hướng dẫn dẫn
Theo giả thiết ta chọn : nH2 = nCnH2n = 1 mol
Phương trình phản ứng :
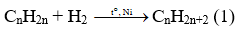
Theo (1) ta thấy, sau phản ứng số mol khí giảm một lượng đúng bằng số mol H2 phản ứng. Hiệu suất phản ứng là 75% nên số mol H2 phản ứng là 0,75 mol. Như vậy sau phản ứng tổng số mol khí là 1+1 – 0,75 = 1,25 mol.
Áp dụng định luật bảo toàn khối lượng ta có : khối lượng của H2 và CnH2n ban đầu bằng khối lượng của hỗn hợp A.
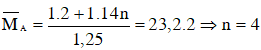
Vậy công thức phân tử olefin là C4H8.
Bài 20: Sau khi tách hidro, hỗn hợp etan và propane tạo thành hỗn hợp etilen và propilen. Khối lượng trung bình của hỗn hợp etilen và propilen nhỏ hơn khối lượng trung bình của hỗn hợp ban đầu là 6,55%. Vậy % etan và propane trong hỗn hợp ban đầu là:
A. 96,18% và 3,82%
B. 98,3% và 1,7%
C. 80% và 20%
D. 95,5% và 4,5%
Lời giải:
Đáp án A
Hướng dẫn
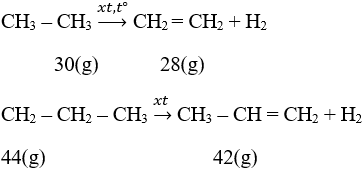
Giả sử ban đầu có 1 mol hỗn hợp; số mol C2H6 là x và C3H8 là 1 – x
M1 = 30x + 44(1 – x)
M2 = 28x + 42(1 – x)
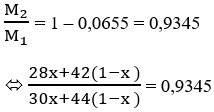
⇒ X = 0,9618
⇒ % C2H6 = 96,18%; % C3H8 = 3,82%
Bài 21: Hỗn hợp X có tỉ khối so với H2 là 21 gồm propan, propene và propin. Khi đốt cháy hoàn toàn 0,1 mol X, tổng khối lượng của CO2 và H2O thu được là
A. 18,60 gam. B. 18,96 gam.
C. 20,40 gam. D. 16,80 gam.
Lời giải:
Đáp án A
Hướng dẫn nCO2 = 3nX = 3.0,1 = 0,3 mol; mX = 0,1.21.2 = 4,2 gam
⇒ nH2O = (4,2 – 0,3.12)/2 = 0,3 mol;
m = mCO2 + mH2O = 0,3.44 + 0,3.18 = 18,6 gam
Bài 22: Hỗn hợp khí X gồm hiđro và một alkene. Nung nóng 24,64 lít hỗn hợp X (đktc), có Ni làm xúc tác. Sau phản ứng thu được 25,3 gam hỗn hợp khí Y.Tỷ khối của X so với H2 là:
A. 10,5 gam B. 11,5 gam
C. 12 gam D. 12,5 gam
Lời giải:
Đáp án B
Hướng dẫn
nX = 26,64/22,4 = 1,1 mol; MX.nX = mX = mY ⇒ MX = 25,3/1,1 = 23; dX/H2 = 23/2 = 11,5
Bài 23: Dẫn 6,72 lít một alkyne X qua dung dịch AgNO3/NH3 dư thấy thu được 44,1g kết tủa. CTPT của X là:
A. C2H2 B. C3H4.
C. C5H8 D. C4H6.
Lời giải:
Đáp án B
Hướng dẫn nX = 0,3 mol ⇒ Mkết tủa = 44,1/0,3 = 147 ⇒ alkyne là C3H4.
Bài 24: Dẫn 3,36 lít hỗn hợp X gồm methane và acetylene vào lượng dư dung dịch AgNO3 trong NH3, thu được m gam kết tủa và có 1,12 lít khí thoát ra. (Thể tích các khí đo (đktc)). Giá trị của m là
A.12,0 B. 24,0 C.13,2 D. 36,0
Lời giải:
Đáp án B
Hướng dẫn
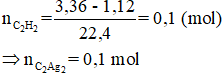
⇒ m = 0,1.240 = 24 (gam)
Bài 25: Cho hỗn hợp X gồm etilen và H2 có tỉ khối so với H2 bằng 4,25. Dẫn X qua bột Ni nung nóng (hiệu suất phản ứng hidro hóa alkene bằng 75%), được hỗn hợp Y. Vậy tỉ khối của hỗn hợp Y so với H2 bằng:
A. 5,44
B. 5,23
C. 5.67
D. 6.76
Lời giải:
Đáp án B
Đáp án Gọi a, b là số mol C2H4 và H2 trước phản ứng.
Ta có: 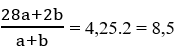
⇔ 28a + 2b = 8,5a + 8,5b ⇔ 19,5a = 6,5b ⇒ a = b/3 hay b = 3a

Bài 26: Hỗn hợp khí X gồm etilen và propin. Cho a mol X tác dụng với dung dịch AgNO3 trong NH3, thu được 17,64 gam kết tủa. Mặt khác a mol X phản ứng tối đa với 0,34 mol H2. Giá trị của a là
A.0,46 B. 0,22 C.0,34 D. 0,32
Lời giải:
Đáp án B
Hướng dẫn
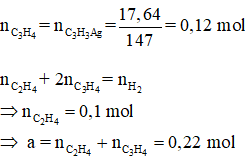
Bài 27: Cho 3,12 gam alkyne X phản ứng với 0,1 mol H2 (xúc tác Pd/PdCO3, t°), thu được hỗn hợp Y chỉ có hai hydrocarbon. Công thức phân tử của X là
A. C2H2
B. C5H8
C. C4H6
D. C3H4
Lời giải:
Đáp án A
Hướng dẫn
Gọi CTTQ alkyne X: CnH2n-2 (n ≥ 2)
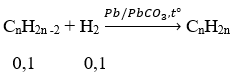
Sau phản ứng thu được 2 hydrocarbon ⇒ alkyne X dư
⇒ nX > 0,1 ⇒ MX < 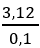
Bài 28: Cho 13,8 gam chất hữu cơ X có công thức phân tử C7H8 tác dùng với một lượng dư dung dịch AgNO3 trong NH3, thu được 45,9 gam kết tủa. X có bao nhiêu đồng phân cấu tạo thỏa mãn chất trên?
A. 5 B. 4 C. 6 D. 2
Lời giải:
Đáp án B
Hướng dẫn
C7H8 + nAgNO3 + nNH3 → C7H8-nAgn + nNH4NO3
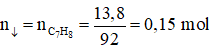
⇒ X có 2 liên kết ba đầu mạch, có 4 cấu tạo:
HC≡C–CH2–CH2–CH2–C≡CH; HC≡C–CH(CH3)–CH2–C≡CH;
HC≡C–CH(C2H5)–C≡CH; HC≡C–C(CH3)2–C≡CH
Bài 29: Hỗn hợp khí A chứa eilen và H2. Tỉ khối của A đối với hiđro là 7,5. Dẫn A đi qua chất xuc tác Ni nung nóng thu được hh khí B có tỉ khối đối với hiđro là 9,0. Hiệu suất phản ứng cộng hiđro của etilen là:
A. 33,3% B. 66,7% C. 25% D. 50%
Lời giải:
Đáp án A
Hướng dẫn
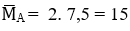
Giả sử nA = 1 mol → mB = mA = 15. 1 = 15 g ; nC2H4 : nH2 = 1:1
Mà 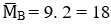
→ 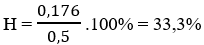
Bài 30: Dẫn alkyne X vào lượng dư dung dịch Br2, khối lượng bình đựng dung dịch Br2 tăng 2 gam và có 0,1 mol Br2 đã tham gia phản ứng. Đốt cháy hoàn toàn cũng lượng X trên, hấp thụ sản phẩm cháy vào dung dịch Ca(OH)2 dư, thu được m gam kết tủa. Giá trị của m là
A. 15 B. 25 C. 30 D. 20
Lời giải:
Đáp án A
Hướng dẫn
nBr2 = 2nX ⇒ nX = 0,05 mol ⇒ 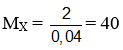
nCaCO3 = nCO2 = 0,05.3 = 0,15 (mol)
→ m↓ = 0,15.100 = 15 gam
Thi online Hóa 11 KNTTThi online Hóa 11 CDThi online Hóa 11 CTST
Xem thêm các dạng bài tập Hóa học lớp 11 có trong đề thi Tốt nghiệp THPT khác:
- Dạng 1: Bài tập tính chất hóa học của alkene, alkadien, alkyne
- Dạng 2: Dạng bài tập Đồng phân, danh pháp của alkene, alkadien, alkyne
- 100 câu trắc nghiệm hydrocarbon không no có lời giải (cơ bản - phần 1)
- 100 câu trắc nghiệm hydrocarbon không no có lời giải (cơ bản - phần 2)
- 100 câu trắc nghiệm hydrocarbon không no có lời giải (cơ bản - phần 3)
- 100 câu trắc nghiệm hydrocarbon không no có lời giải (nâng cao - phần 1)
- 100 câu trắc nghiệm hydrocarbon không no có lời giải (nâng cao - phần 3)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 11 Global Success
- Giải sgk Tiếng Anh 11 Smart World
- Giải sgk Tiếng Anh 11 Friends Global
- Lớp 11 - Kết nối tri thức
- Soạn văn 11 (hay nhất) - KNTT
- Soạn văn 11 (ngắn nhất) - KNTT
- Giải sgk Toán 11 - KNTT
- Giải sgk Vật Lí 11 - KNTT
- Giải sgk Hóa học 11 - KNTT
- Giải sgk Sinh học 11 - KNTT
- Giải sgk Lịch Sử 11 - KNTT
- Giải sgk Địa Lí 11 - KNTT
- Giải sgk Giáo dục KTPL 11 - KNTT
- Giải sgk Tin học 11 - KNTT
- Giải sgk Công nghệ 11 - KNTT
- Giải sgk Hoạt động trải nghiệm 11 - KNTT
- Giải sgk Giáo dục quốc phòng 11 - KNTT
- Giải sgk Âm nhạc 11 - KNTT
- Lớp 11 - Chân trời sáng tạo
- Soạn văn 11 (hay nhất) - CTST
- Soạn văn 11 (ngắn nhất) - CTST
- Giải sgk Toán 11 - CTST
- Giải sgk Vật Lí 11 - CTST
- Giải sgk Hóa học 11 - CTST
- Giải sgk Sinh học 11 - CTST
- Giải sgk Lịch Sử 11 - CTST
- Giải sgk Địa Lí 11 - CTST
- Giải sgk Giáo dục KTPL 11 - CTST
- Giải sgk Hoạt động trải nghiệm 11 - CTST
- Giải sgk Âm nhạc 11 - CTST
- Lớp 11 - Cánh diều
- Soạn văn 11 Cánh diều (hay nhất)
- Soạn văn 11 Cánh diều (ngắn nhất)
- Giải sgk Toán 11 - Cánh diều
- Giải sgk Vật Lí 11 - Cánh diều
- Giải sgk Hóa học 11 - Cánh diều
- Giải sgk Sinh học 11 - Cánh diều
- Giải sgk Lịch Sử 11 - Cánh diều
- Giải sgk Địa Lí 11 - Cánh diều
- Giải sgk Giáo dục KTPL 11 - Cánh diều
- Giải sgk Tin học 11 - Cánh diều
- Giải sgk Công nghệ 11 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 11 - Cánh diều
- Giải sgk Giáo dục quốc phòng 11 - Cánh diều
- Giải sgk Âm nhạc 11 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

