Lý thuyết Hợp chất của sắt (hay, chi tiết nhất)
Bài viết Lý thuyết Hợp chất của sắt hay, chi tiết giúp bạn nắm vững kiến thức trọng tâm về Hợp chất của sắt.
Lý thuyết Hợp chất của sắt (hay, chi tiết nhất)
Thi online Hóa 12 KNTTThi online Hóa 12 CDThi online Hóa 12 CTST
Bài giảng: Bài 32: Hợp chất của sắt - Cô Nguyễn Thị Thu (Giáo viên VietJack)
I. SẮT (II)
1. Oxit FeO
- Là chất rắn, đen, không tan trong nước.
- FeO tác dụng với dung dịch HNO3 được muối sắt (III).
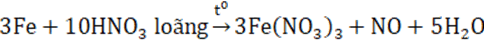
- Phương trình ion rút gọn như sau:
3FeO + NO3- + 10H+ → 3Fe3+ + NO + 5H2O
Điều chế: dùng H hay CO khử sắt (III) oxit ở 5000C:
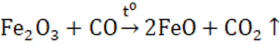
2. Hidroxit Fe(OH)2
Tác dụng với dung dịch kiềm tạo kết tủa màu trắng hơi xanh, rồi hóa nâu đỏ.
Fe2+ + 2OH- → Fe(OH)2↓ (trắng xanh)
Chú ý: Muốn có Fe(OH)2 tinh khiết phải điều chế trong điều kiện không có không khí.
3. Muối sắt (II)
Muối sắt (II) dễ bị oxi hóa thành muối sắt (III) bởi các chất oxi hóa.
FeCl2 + Cl2 → 2FeCl3
Điều chế: cho Fe (hoặc FeO, Fe(OH)2) tác dụng với HCl hoặc H2SO4 loãng:
Fe + 2HCl → FeCl2 + H2
FeO + H2SO4 → FeSO4 + H2
Chú ý: dung dịch muối sắt (II) điều chế được cần dùng ngay, vì trong không khí muối sắt (II) sẽ chuyển dần thành muối sắt (III).
II. SẮT (III)
1. Oxit Fe2O3
- Sắt (III) oxit là bazơ nên dễ tan trong các dung dịch axit mạnh.
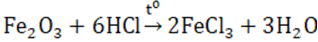
Ở nhiệt độ cao, Fe2O3 bị CO khử hoặc H2 khử thành Fe.
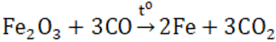
Điều chế: phân hủy Fe(OH)3 ở nhiệt độ cao.
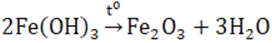
2. Hidroxit Fe(OH)3
Fe(OH)3 không tan trong nước nhưng dễ tan trong dung dịch axit.
2Fe(OH)3 + 3H2SO4 → Fe2(SO4)3 + 6H2O
Điều chế: cho dung dịch kiềm tác dụng với muối sắt (III).
FeCl3 + 3NaOH → Fe(OH)3 + 3NaCl
3. Muối sắt (III)
Các muối sắt (III) có tính oxi hóa, dễ bị khử thành muối sắt (II).
Fe + 2FeCl3 → 3FeCl2
Bột đồng tan trong dung dịch muối sắt (III).
Cu + 2FeCl3 (vàng nâu) → CuCl2 + FeCl2
⇒ Dung dịch CuCl2 (màu xanh) và dung dịch FeCl2 (không màu) nên dung dịch thu được có màu xanh.
Thi online Hóa 12 KNTTThi online Hóa 12 CDThi online Hóa 12 CTST
Xem thêm các phần Lý thuyết Hóa học lớp 12 ôn thi Tốt nghiệp THPT hay khác:
- Lý thuyết Crom
- Lý thuyết Hợp chất của Crom
- Lý thuyết Sắt
- Lý thuyết Hợp chất của sắt
- Lý thuyết Hợp kim của sắt
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 12 Global Success
- Giải sgk Tiếng Anh 12 Smart World
- Giải sgk Tiếng Anh 12 Friends Global
- Lớp 12 Kết nối tri thức
- Soạn văn 12 (hay nhất) - KNTT
- Soạn văn 12 (ngắn nhất) - KNTT
- Giải sgk Toán 12 - KNTT
- Giải sgk Vật Lí 12 - KNTT
- Giải sgk Hóa học 12 - KNTT
- Giải sgk Sinh học 12 - KNTT
- Giải sgk Lịch Sử 12 - KNTT
- Giải sgk Địa Lí 12 - KNTT
- Giải sgk Giáo dục KTPL 12 - KNTT
- Giải sgk Tin học 12 - KNTT
- Giải sgk Công nghệ 12 - KNTT
- Giải sgk Hoạt động trải nghiệm 12 - KNTT
- Giải sgk Giáo dục quốc phòng 12 - KNTT
- Giải sgk Âm nhạc 12 - KNTT
- Giải sgk Mĩ thuật 12 - KNTT
- Lớp 12 Chân trời sáng tạo
- Soạn văn 12 (hay nhất) - CTST
- Soạn văn 12 (ngắn nhất) - CTST
- Giải sgk Toán 12 - CTST
- Giải sgk Vật Lí 12 - CTST
- Giải sgk Hóa học 12 - CTST
- Giải sgk Sinh học 12 - CTST
- Giải sgk Lịch Sử 12 - CTST
- Giải sgk Địa Lí 12 - CTST
- Giải sgk Giáo dục KTPL 12 - CTST
- Giải sgk Tin học 12 - CTST
- Giải sgk Hoạt động trải nghiệm 12 - CTST
- Giải sgk Âm nhạc 12 - CTST
- Lớp 12 Cánh diều
- Soạn văn 12 Cánh diều (hay nhất)
- Soạn văn 12 Cánh diều (ngắn nhất)
- Giải sgk Toán 12 Cánh diều
- Giải sgk Vật Lí 12 - Cánh diều
- Giải sgk Hóa học 12 - Cánh diều
- Giải sgk Sinh học 12 - Cánh diều
- Giải sgk Lịch Sử 12 - Cánh diều
- Giải sgk Địa Lí 12 - Cánh diều
- Giải sgk Giáo dục KTPL 12 - Cánh diều
- Giải sgk Tin học 12 - Cánh diều
- Giải sgk Công nghệ 12 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 12 - Cánh diều
- Giải sgk Giáo dục quốc phòng 12 - Cánh diều
- Giải sgk Âm nhạc 12 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

