Bài tập muối tác dụng với bazơ và cách giải
Với Bài tập muối tác dụng với bazơ và cách giải môn Hóa học lớp 9 sẽ giúp học sinh nắm vững lý thuyết, biết phương pháp giải các dạng bài tập từ đó có kế hoạch ôn tập hiệu quả để đạt kết quả cao trong các bài thi môn Hóa học 9.
Bài tập muối tác dụng với bazơ và cách giải
Thi online KHTN 9 KNTTThi online KHTN 9 CDThi online KHTN 9 CTST

I. Lý thuyết và phương pháp giải:
- Phản ứng giữa dung dịch bazơ và dung dịch muối là phản ứng trao đổi.
- Phương trình phản ứng hóa học tổng quát:
Muối + bazơ → muối mới + bazơ mới
Ví dụ: FeCl2 + 2KOH → 2KCl + Fe(OH)2↓
Lưu ý:
- Điều kiện xảy ra phản ứng:
+ Chất tham gia phản ứng phải tan.
+ Sản phẩm thường có kết tủa tạo thành.
- Phản ứng đặc biệt của Al(OH)3 khi tác dụng với bazơ dư:
3NaOH + AlCl3 → Al(OH)3 ↓ + 3NaCl (1)
NaOH (dư) + Al(OH)3 → NaAlO2 + 2H2O (2)
Hay:
4NaOH (dư) + AlCl3 → NaAlO2 + 3NaCl + 2H2O (3)
- Phương pháp giải
+ Bước 1: Xử lí số liệu đề bài cho và viết phương trình phản ứng hóa học.
+ Bước 2: Đặt ẩn, lập hệ phương trình (nếu cần).
+ Bước 3: Giải hệ phương trình (nếu có) và tính toán theo yêu cầu đề bài.
II. Ví dụ minh họa
Ví dụ 1: Dung dịch KOH có thể phản ứng với tất cả các muối có trong dãy nào sau đây?
A. NaCl, MgCl2, CuCl2. B. K2SO4, MgSO4, CuSO4.
C. NaNO3, Mg(NO3)2, FeCl3. D. CuCl2, MgSO4, FeCl3.
Lời giải:
Đáp án D
Loại A do NaCl không phản ứng với KOH.
Loại B do K2SO4 không phản ứng với KOH.
Loại C do NaNO3 không phản ứng với KOH.
Ví dụ 2: Cho m gam KOH nguyên chất vào 250g nước được dd A. Cho dd A tác dụng với dd Cu(NO3)2 lấy dư, thu được 19,6 g kết tủa. Tính C% của dd A?
Lời giải:
Phương trình phản ứng hóa học:
2KOH + Cu(NO3)2 →2 KNO3 + Cu(OH)2 ↓
n↓= nCu(OH)2 =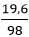 = 0,2 mol
= 0,2 mol
Theo phương trình phản ứng hóa học ta có:
nKOH = 2nCu(OH)2= 2.0,2 = 0,4 mol
⇒ mKOH = 0,4.56 = 22,4g
⇒ C% dung dịch A =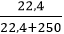 .100 = 8,22%
.100 = 8,22%

III. Bài tập tự luyện
Bài 1: Nhỏ từ từ dung dịch NaOH vào dung dịch CuCl2 đến khi kết tủa không tạo thêm nữa thì dừng lại. Lọc kết tủa rồi đem nung đến khối lượng không đổi. Thu được chất rắn nào sau đây:
A. Cu
B. CuO
C. Cu2O
D. Cu(OH)2.
Bài 2: Cho a g Na2CO3 vào dung dịch Ca(OH)2, sau phản ứng thu được 20g kết tủa. Vậy a có giá trị
A. 21,2 g
B. 20 g
C. 34,8 g
D. 18,2 g
Bài 3: Cặp chất nào sau đây không thể tồn tại trong cùng một dung dịch?
A. Ba(OH)2 và NaCl.
B. Ca(OH)2 và KNO3.
B. KOH và NaNO3.
D. Ba(OH)2 và CuCl2.
Bài 4: Cho 10,6 gam dung dịch Na2CO3 20% tác dụng hết với một lượng dư dung dịch Ba(OH)2. Sau khi phản ứng kết thúc thấy thu được m gam kết tủa. Giá trị của m là
A. 3,49 gam.
B. 3,94 gam.
C. 7,88 gam.
D. 1,97 gam.
Bài 5. Có các dung dịch muối sau: FeCl3; CuCl2; NaCl; MgCl2; AlCl3. Dung dịch nào sau đây có thể nhận biết được các chất trên?
A. Quỳ tím. B. Dung dịch Ba(NO3)2.
C. Dung dịch AgNO3. D. Dung dịch NaOH.
Bài 6: Trộn dung dịch có chứa 0,1 mol CuSO4 và một dung dịch chứa 0,3 mol NaOH, lọc kết tủa, rửa sạch rồi đem nung đến khối lượng không đổi thu được m g chất rắn. Giá trị m là:
A. 8 g
B. 4 g
C. 6 g
D. 12 g
Bài 7: Hòa tan 6,2 g Na2O vào nước được 2 lít dung dịch A. Cho 2 lít dung dịch A tác dụng vừa đủ với 2 lít dung dịch MgSO4. Nồng độ mol của dung dịch thu được là. (Coi thể tích dung dịch thay đổi không đáng kể)
A .0,01M
B. 0,025M
C. 0,03M
D. 0,04M
Câu 8: Cho dung dịch Ca(OH)2 10% tác dụng với dung dịch muối nhôm (III) clohidric dư. Biết 300ml dung dịch HCl 2M trung hòa hết dung dịch Ca(OH)2 10% như trên. Tính khối lượng kết tủa sinh ra?
A. 23,4g
B. 35,1g
C. 17,55g
D. 46,8 g
Bài 9: Cho m gam NaOH nguyên chất vào 252g nước được dung dịch A. cho dung dịch A tác dụng với dung dịch Cu(NO3)2 có dư, thu được 58,8g kết tủa Cu(OH)2. Hãy tính m.
A. 56g
B. 34g
C. 47g
D. 48g
Bài 10: Trộn 13,44 gam dung dịch KOH 25% với 32,5 gam dung dịch FeCl3 20%. Sau khi phản ứng xảy ra hoàn toàn thì khối lượng kết tủa thu được là
A. 3 gam.
B. 3,14 gam.
C. 4,14 gam.
D. 2,14 gam.
Đáp án minh họa
1B |
2A |
3D |
4B |
5D |
6A |
7B |
8A |
9D |
10D |
Thi online KHTN 9 KNTTThi online KHTN 9 CDThi online KHTN 9 CTST
Xem thêm các dạng bài tập Hóa học lớp 9 có đáp án, hay khác:
Xem thêm các loạt bài Để học tốt Hóa học 9 hay khác:
- Giải bài tập Hóa học 9
- Giải sách bài tập Hóa 9
- Đề thi Hóa học 9
- Wiki 200 Tính chất hóa học
- Wiki 3000 Phản ứng hóa học quan trọng
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Chuyên đề: Lý thuyết - Bài tập Hóa học lớp 9 có đáp án được biên soạn bám sát nội dung chương trình sgk Hóa học 9.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 9 Global Success
- Giải sgk Tiếng Anh 9 Smart World
- Giải sgk Tiếng Anh 9 Friends plus
- Lớp 9 Kết nối tri thức
- Soạn văn 9 (hay nhất) - KNTT
- Soạn văn 9 (ngắn nhất) - KNTT
- Giải sgk Toán 9 - KNTT
- Giải sgk Khoa học tự nhiên 9 - KNTT
- Giải sgk Lịch Sử 9 - KNTT
- Giải sgk Địa Lí 9 - KNTT
- Giải sgk Giáo dục công dân 9 - KNTT
- Giải sgk Tin học 9 - KNTT
- Giải sgk Công nghệ 9 - KNTT
- Giải sgk Hoạt động trải nghiệm 9 - KNTT
- Giải sgk Âm nhạc 9 - KNTT
- Giải sgk Mĩ thuật 9 - KNTT
- Lớp 9 Chân trời sáng tạo
- Soạn văn 9 (hay nhất) - CTST
- Soạn văn 9 (ngắn nhất) - CTST
- Giải sgk Toán 9 - CTST
- Giải sgk Khoa học tự nhiên 9 - CTST
- Giải sgk Lịch Sử 9 - CTST
- Giải sgk Địa Lí 9 - CTST
- Giải sgk Giáo dục công dân 9 - CTST
- Giải sgk Tin học 9 - CTST
- Giải sgk Công nghệ 9 - CTST
- Giải sgk Hoạt động trải nghiệm 9 - CTST
- Giải sgk Âm nhạc 9 - CTST
- Giải sgk Mĩ thuật 9 - CTST
- Lớp 9 Cánh diều
- Soạn văn 9 Cánh diều (hay nhất)
- Soạn văn 9 Cánh diều (ngắn nhất)
- Giải sgk Toán 9 - Cánh diều
- Giải sgk Khoa học tự nhiên 9 - Cánh diều
- Giải sgk Lịch Sử 9 - Cánh diều
- Giải sgk Địa Lí 9 - Cánh diều
- Giải sgk Giáo dục công dân 9 - Cánh diều
- Giải sgk Tin học 9 - Cánh diều
- Giải sgk Công nghệ 9 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 9 - Cánh diều
- Giải sgk Âm nhạc 9 - Cánh diều
- Giải sgk Mĩ thuật 9 - Cánh diều






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

