Chuyên đề bồi dưỡng HSG Hóa học 9 Phi kim (có lời giải)
Bài viết Chuyên đề bồi dưỡng HSG Hóa học 9 Phi kim gồm các dạng bài tập từ cơ bản đến nâng cao với phương pháp giải chi tiết và bài tập tự luyện đa dạng giúp Giáo viên có thêm tài liệu ôn thi Học sinh giỏi Hóa 9.
Chuyên đề bồi dưỡng HSG Hóa học 9 Phi kim (có lời giải)
Chỉ từ 300k mua trọn Chuyên đề bồi dưỡng HSG Hóa học 9 sách mới bản word có lời giải chi tiết:
- B1: gửi phí vào tk:
1133836868- CT TNHH DAU TU VA DV GD VIETJACK - Ngân hàng MB (QR) - B2: Nhắn tin tới Zalo VietJack Official - nhấn vào đây để thông báo và nhận giáo án
A. TÓM TẮT KIẾN THỨC
I. Tính chất vật lý của phi kim
- Ở dạng tự do và điều kiện thường phi kim tồn tại cả 3 trạng thái: rắn, lỏng, khí.
+ Ví dụ: trạng thái rắn: carbon; trạng thái lỏng: bromine; trạng thái khí: oxygen, Hydrogen.
- Phi kim thường không có ánh kim, không dẫn nhiệt, không dẫn điện (nếu có thì rất kém )…
II. Tính chất hóa học của phi kim
1. Tác dụng với kim loại (đã học phần kim loại)
2. Phi kim tác dụng với hydrogen
3. Phi kim loại tác dụng với oxygen
- Nhiều phi kim tác dụng với oxygen tạo ra oxide.
Chú ý:
- Trong các phi kim fluorine hoạt động mạnh nhất, sau đó là oxygen và chlorine.
- S, P, C, Si.. là những phi kim họat động yếu hơn.
III. Sự khác nhau giữa kim loại và phi kim
1. Sự khác nhau về tính chất vật lí
a. Tính dẫn điện
- Trong khi các kim loại dẫn điện tốt thì phi kim thường không dẫn điện. Siliconon tinh khiết là chất bán dẫn. Than chì có tính dẫn điện nhưng yếu hơn kim loại.
b. Nhiệt độ nóng chảy, nhiệt độ sôi
Đơn chất |
Nhiệt độ nóng chảy (oC) |
Nhiệt độ sôi (oC) |
Đợn chất |
Nhiệt độ nóng chảy (oC) |
Nhiệt độ sôi (oC) |
Oxgyen |
- 218 |
-183 |
Aluminium |
660,3 |
2518 |
Chlorine |
-101,5 |
-34 |
Iron |
1535 |
2861 |
Sulfur |
106,8 |
444,7 |
Copper |
1084,6 |
2561,5 |
Phosphorus trắng |
44,2 |
280,3 |
Gold |
1064,2 |
2856 |
- Phần lớn các phi kim có nhiệt độ nóng chảy, nhiệt độ sôi thấp hơn kim loại. Ở nhiệt độ thường, trong khi hầu hết các kim loại ở thể rắn (riêng thuỷ ngân ở thể lỏng) thì phi kim có thể tồn tại ở thể khí (hydrogen, nitrogen, oxygen, fluorine, chlorine,...), thể lỏng (bromine) hay thể rắn (carbon, siliconon, phosphorus, sulfur,...).
c. Khối lượng riêng
- Phần lớn phi kim có khối lượng riêng nhỏ hơn kim loại.
2. Sự khác nhau về tính chất hoá học
a. Phản ứng của kim loại với phi kim
- Trong phản ứng hoá học, các kim loại dễ nhường electron để tạo ra ion dương, còn các phi kim dễ nhận electron tạo ion âm.
- Ví dụ:
- Liên kết được hình thành trong phân tử hợp chất tạo bởi kim loại và phi kim là liên kết ion.
b. Phản ứng của phi kim và kim loại với oxygen
- Kim loại tác dụng với oxygen thường tạo thành oxide base, trong khi phi kim tác dụng với oxygen thường tạo thành oxide acid.
Ví dụ:
IV. Một số phi kim quan trọng
1. Chlorine
a. Tính chất vật lý
- Chlorine là chất khí màu vàng lục, mùi hắc, nặng hơn không khí. Chlorine ít tan trong nước.
- Chlorine là khí độc, khi hít nhiều có thể tử vong.
b. Tính chất hóa học (bổ sung kiến thức quan trọng)
* Cl2 tác dụng nước:
+ Chloine tác dụng với nước tạo thành nước chlorine có màu vàng lục bao gồm các chất: Cl2, HCl và HClO:
+ Phương trình hóa học:
ð Khi cho quỳ tím vào nước chlorine: ban đầu quỳ tím chuyển thành màu đỏ do acid, nhưng nhanh chóng bị mất màu do tác dụng oxi hóa mạnh của hypochloro acid (HClO)
* Cl2 tác dụng với dung dịch NaOH:
ð Hỗn hợp sản phẩm này gọi là nước Javen, nước Javen cũng có tính tẩy màu, tiệt trùng vì NaClO (Sodium hypochlorite) là chất oxi hóa mạnh.
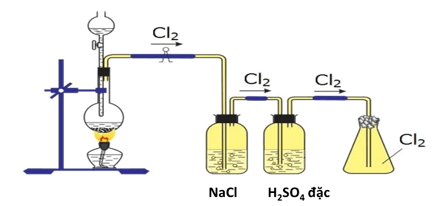
c. Điều chế
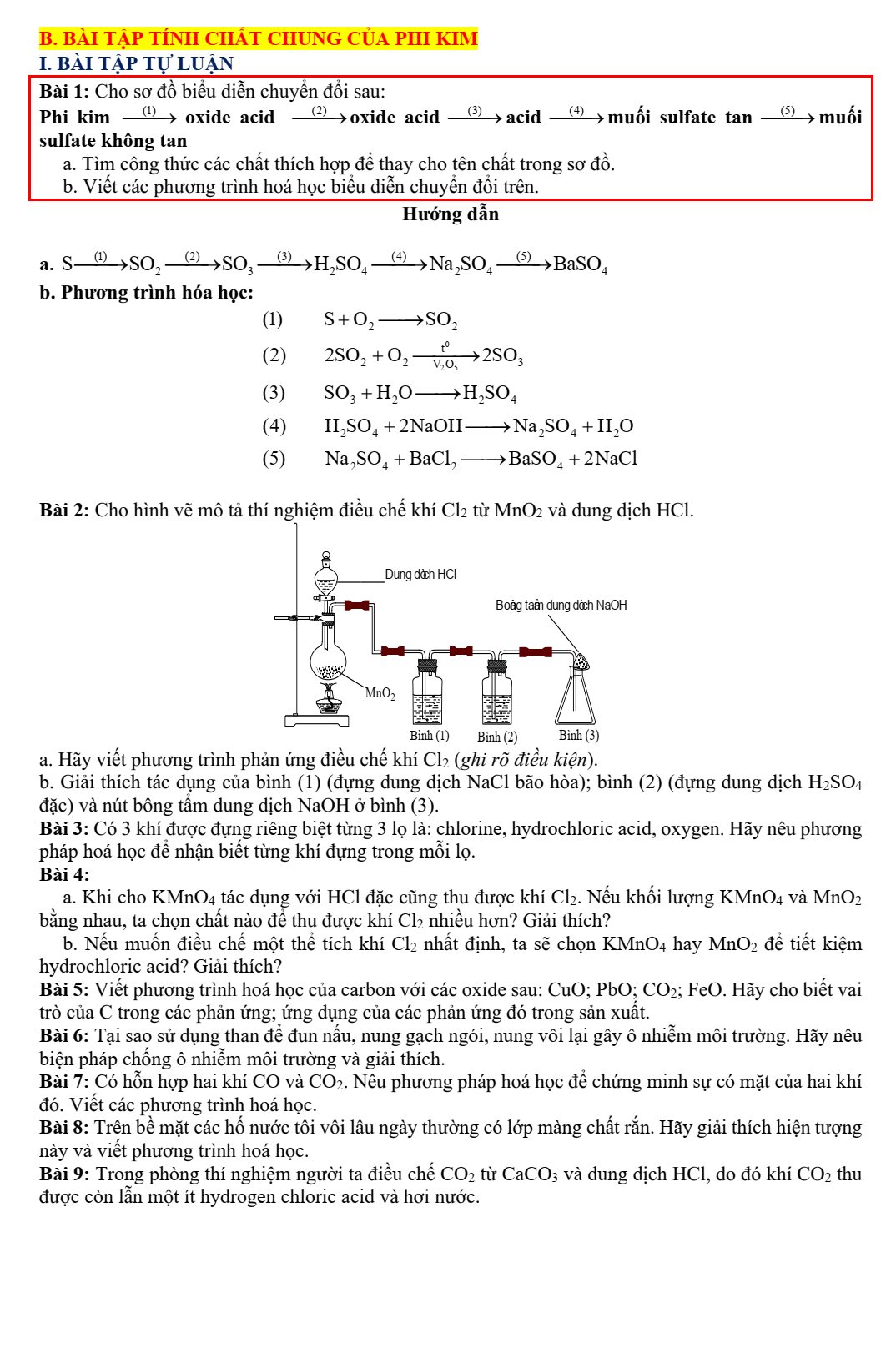
- Trong phòng thí nghiệm: (khí Cl2 được điều chế bằng cách cho HCl đậm đặc tác dụng với MnO2 hoặc KMnO4)
- Trong công nghiệp: (khí Cl2 được điều chế bằng cách điện phân dung dịch muối ăn có màng ngăn)
c. Ứng dụng:
- Chlorine có nhiều ứng dụng trong cuộc sống và trong các ngành công nghiệp như khử trùng nước sinh hoạt; sản xuất nước Javel, chất tẩy rửa,...; tẩy trắng vải, sợi, bột giấy.....; sản xuất chất dẻo, ...
2. Carbon
a. Các dạng thù hình của carbon
- Trong tự nhiên, đơn chất carbon tồn tại ở các dạng chính như: kim cương, than chì (graphite), carbon vô định hình (than gỗ, than xương, mồ hóng,...).
Kim cương |
Than đá |
Carbon vô định hình |
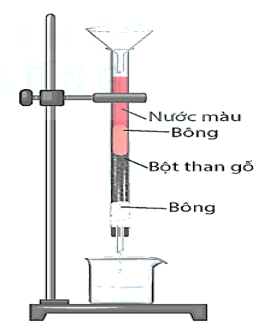
- Các loại than như than gỗ, than xương,... có khả năng giữ trên bề mặt của nó các phân tử chất khí, chất tan trong dung dịch. Tính chất này được gọi là tính hấp phụ. Dựa vào tính hấp phụ, carbon ở dạng than hoạt tính được dùng trong mặt nạ phòng độc, chất khử màu, khử mùi.
b. Tính chất hóa học (bổ sung kiến thức)
- Cacbon vô định hình là một phi kim hoạt động yếu
- Tác dụng với kim loại phản ứng rất khó khăn:
- Tác dụng với hidro phản ứng rất khó khăn:
- Cháy trong oxi và tỏa nhiệt:
ð Tính chất đặc biệt của cacbon là tính khử, ở nhiệt độ cao cacbon khử nhiều oxit kim loại thành kim loại tự do.
c. Ứng dụng
- Carbon còn có rất nhiều các ứng dụng khác như: than cốc dùng làm nhiên liệu, nguyên liệu trong công nghiệp luyện kim,...; than chì làm điện cực, chất bôi trơn, ruột bút chì,...; kim cương làm đồ trang sức, mũi khoan, dao cắt kính;...
3. Carbon oxide
- Kí hiệu hóa học: CO
- Phân tử khối: 28 (gam/mol)
a. Tính chất vật lý
Carbon oxide là chất khí không màu, ít tan trong nước, nhẹ hơn không khí, rất bền với nhiệt. CO là khí độc (vì CO kết hợp với chất hemoglobin trong máu thành hợp chất bền, làm cho hemoglobin mất tác dụng vận chuyển khí oxi đi khắp cơ thể người và động vật)
b. Tính chất hóa học: CO là oxide trung tính, CO là chất khử
- CO không tác dụng với axit, kiềm ở nhiệt độ thường.
- CO không tạo muối.
- CO khử được nhiều oxide kim loại ở nhiệt độ cao tạo thành kim loại tự do:
- CO cháy trong oxi:
4. Sulfur (sulfur)
- Sulfur là nguyên liệu quan trọng cho nhiều ngành công nghiệp
- Ứng dụng:
+ Lưu hóa cao su: Bản chất của quá trình lưu hóa cao su là quá trình tạo các cầu nối sulfur giữa các mạch cao su để hình thành một mạng lưới có kết cấu chắc chắn, đàn hồi hơn. Vì vậy, lưu hoá cao su là quá trình quan trọng để sản xuất các sản phẩm từ cao su như lốp xe, ống dẫn, dây cáp, đệm, quần áo bảo hộ,...
+ Sản xuất dược phẩm;
+ Sản xuất sulfuric acid;
+ Sản xuất pháo hoa, diêm;
+ Sản xuất thuốc diệt nấm.
................................
................................
................................
Xem thêm các Chuyên đề bài tập bồi dưỡng Học sinh giỏi Hóa học lớp 9 có đáp án hay khác:
Xem thêm các loạt bài Để học tốt Hóa học 9 hay khác:
- Giải bài tập Hóa học 9
- Giải sách bài tập Hóa 9
- Đề thi Hóa học 9
- Wiki 200 Tính chất hóa học
- Wiki 3000 Phản ứng hóa học quan trọng
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Loạt bài Chuyên đề: Lý thuyết - Bài tập Hóa học lớp 9 có đáp án được biên soạn bám sát nội dung chương trình sgk Hóa học 9.
Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 9 Global Success
- Giải sgk Tiếng Anh 9 Smart World
- Giải sgk Tiếng Anh 9 Friends plus
- Lớp 9 Kết nối tri thức
- Soạn văn 9 (hay nhất) - KNTT
- Soạn văn 9 (ngắn nhất) - KNTT
- Giải sgk Toán 9 - KNTT
- Giải sgk Khoa học tự nhiên 9 - KNTT
- Giải sgk Lịch Sử 9 - KNTT
- Giải sgk Địa Lí 9 - KNTT
- Giải sgk Giáo dục công dân 9 - KNTT
- Giải sgk Tin học 9 - KNTT
- Giải sgk Công nghệ 9 - KNTT
- Giải sgk Hoạt động trải nghiệm 9 - KNTT
- Giải sgk Âm nhạc 9 - KNTT
- Giải sgk Mĩ thuật 9 - KNTT
- Lớp 9 Chân trời sáng tạo
- Soạn văn 9 (hay nhất) - CTST
- Soạn văn 9 (ngắn nhất) - CTST
- Giải sgk Toán 9 - CTST
- Giải sgk Khoa học tự nhiên 9 - CTST
- Giải sgk Lịch Sử 9 - CTST
- Giải sgk Địa Lí 9 - CTST
- Giải sgk Giáo dục công dân 9 - CTST
- Giải sgk Tin học 9 - CTST
- Giải sgk Công nghệ 9 - CTST
- Giải sgk Hoạt động trải nghiệm 9 - CTST
- Giải sgk Âm nhạc 9 - CTST
- Giải sgk Mĩ thuật 9 - CTST
- Lớp 9 Cánh diều
- Soạn văn 9 Cánh diều (hay nhất)
- Soạn văn 9 Cánh diều (ngắn nhất)
- Giải sgk Toán 9 - Cánh diều
- Giải sgk Khoa học tự nhiên 9 - Cánh diều
- Giải sgk Lịch Sử 9 - Cánh diều
- Giải sgk Địa Lí 9 - Cánh diều
- Giải sgk Giáo dục công dân 9 - Cánh diều
- Giải sgk Tin học 9 - Cánh diều
- Giải sgk Công nghệ 9 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 9 - Cánh diều
- Giải sgk Âm nhạc 9 - Cánh diều
- Giải sgk Mĩ thuật 9 - Cánh diều













 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

