Ma trận đề thi Giữa kì 2 Hóa học 12 năm 2024
Tài liệu Ma trận đề thi Giữa kì 2 Hóa học 12 năm 2024 mới nhất gồm bảng đặc tả và 3 đề thi có đáp án và lời giải chi tiết. Hi vọng Ma trận đề thi Giữa kì 2 Hóa học 12 năm 2024 sẽ giúp học sinh có kế hoạch ôn tập, luyện đề hiệu quả từ đó đạt kết quả cao trong các bài thi môn Hóa học lớp 12.
Ma trận đề thi Giữa kì 2 Hóa học 12 năm 2024
MA TRẬN ĐỀ THI GIỮA HỌC KÌ 2
MÔN: HÓA HỌC 12– THỜI GIAN LÀM BÀI: 45 PHÚT
|
TT |
Nội dung kiến thức |
Đơn vị kiến thức |
Mức độ nhận thức |
Tổng |
% tổng điểm |
||||||||||
|
Nhận biết |
Thông hiểu |
Vận dụng |
Vận dụng cao |
|
|
||||||||||
|
Số CH |
Thời gian (phút) |
||||||||||||||
|
Số CH
|
Thời gian (phút) |
Số CH
|
Thời gian (phút) |
Số CH
|
Thời gian (phút) |
Số CH
|
Thời gian (phút) |
TN |
TL |
|
|
||||
|
1 |
Chương 5: Đại cương về kim loại |
Sự ăn mòn kim loại |
0 |
0 |
1 |
1 |
1* |
|
|
|
1 |
|
1 |
2,5% |
|
|
2 |
Điều chế kim loại |
2 |
1,5 |
0 |
0 |
1* |
|
|
|
2 |
|
1,5 |
5% |
||
|
3 |
Chương 6: Kim loại kiềm. Kim loại kiềm thổ. Nhôm |
Kim loại kiềm |
4 |
3 |
2 |
2 |
1* |
4,5 |
|
|
6 |
1 |
9,6 |
25% |
|
|
4 |
Kim loại kiềm thổ và hợp chất |
6 |
4,5 |
4 |
4 |
1* |
|
1** |
6 |
10 |
1 |
14,5 |
30% |
||
|
5 |
Nhôm và hợp chất |
4 |
3 |
3 |
3 |
1* |
|
1** |
|
7 |
|
6 |
17,5% |
||
|
6 |
|
Tổng hợp kiến thức |
|
|
2 |
2 |
1* |
4,5 |
1** |
6 |
2 |
2 |
12,5 |
20% |
|
|
Tổng |
16 |
12 |
12 |
12 |
2 |
9 |
2 |
12 |
28 |
4 |
45 |
100 |
|||
|
Tỉ lệ % |
40% |
30% |
20% |
10% |
|
|
|
|
|||||||
|
Tỉ lệ chung |
70% |
30% |
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Lưu ý:
- Các câu hỏi ở cấp độ nhận biết và thông hiểu là các câu hỏi trắc nghiệm khách quan 4 lựa chọn, trong đó có duy nhất 1 lựa chọn đúng.
- Các câu hỏi ở cấp độ vận dụng và vận dụng cao là các câu hỏi tự luận.
- Mỗi câu trắc nghiệm khách quan được tính 0,25 điểm, các câu hỏi tự luận được cho điểm cụ thể trong hướng dẫn chấm theo tỉ lệ như trong ma trận.
- Đã chọn câu mức độ “vận dụng” ở đơn vị kiến thức này thì không chọn câu “vận dụng cao” ở đơn vị kiến thức đó và các câu trong cùng mức độ nhận thức không chọn vào cùng một nội dung.
- (1* ) Giáo viên có thể ra 2 câu hỏi cho đề kiểm tra ở cấp độ vận dụng ở đơn vị kiến thức: (1) →(6)
- (1**) Giáo viên có thể ra 2 câu hỏi cho đề kiểm tra ở cấp độ vận dụng cao ở đơn vị kiến thức: (4) hoặc (5) hoặc (6)
Đề thi Giữa học kì 2 năm học 2021
Môn thi Hóa học - Lớp 12
Thời gian làm bài: 45 phút
(không kể thời gian phát đề)
PHẦN TRẮC NGHIỆM.
Mức độ: Nhận biết
Câu 1. Kim loại nào sau đây được điều chế bằng phương pháp điện phân dung dịch?
A. Al.
B. Ca.
C. Na.
D. Cu.
Câu 2. Trong công nghiệp, kim loại Na được điều chế bằng phương pháp nào sau đây?
A. Điện phân hợp chất nóng chảy.
B. Điện phân dung dịch.
C. Thủy luyện.
D. Nhiệt luyện.
Câu 3. Ở nhiệt độ thường, kim loại Na phản ứng với H2O, thu được H2 và chất nào sau đây?
A. NaCl.
B. Na2O.
C. NaOH.
D. Na2O2.
Câu 4. Kim loại nào sau đây không phải là kim loại kiềm?
A. Li.
B. K.
C. Ba.
D. Cs.
Câu 5. Kim loại Na được bảo quản bằng cách ngâm chìm trong
A. rượu.
B. giấm.
C. nước.
D. dầu hỏa.
Câu 6. Chất X được dùng làm thuốc giảm đau dạ dày. Công thức của X là
A. NH4Cl.
B. NaHCO3.
C. NaCl.
D. Na2SO4.
Câu 7. Kim loại nào sau đây là kim loại kiềm thổ?
A. Na.
B. Fe.
C. Al.
D. Mg.
Câu 8. Công thức chung của oxit kim loại nhóm IIA là
A. RO.
B. R2O.
C. RO2.
D. R2O3.
Câu 9. Kim loại Mg tác dụng với dung dịch HCl tạo ra muối và
A. H2.
B. O2.
C. H2O.
D. Cl2.
Câu 10. Thạch cao sống có công thức hóa học là
A. CaCO3.
B. CaSO4.2H2O.
C. CaSO4.
D. CaSO4.H2O.
Câu 11. Khí X là sản phẩm của phản ứng nhiệt phân CaCO3. Công thức hóa học của X là
A. CO2.
B. CH4.
C. CO.
D. C2H2.
Câu 12. Một mẫu nước có chứa các ion: K+, Na+, 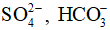 . Mẫu nước này thuộc loại
. Mẫu nước này thuộc loại
A. nước có tính cứng tạm thời.
B. nước có tính cứng toàn phần.
C. nước có tính cứng vĩnh cửu.
D. nước mềm.
Câu 13. Quặng nào sau đây được dùng làm nguyên liệu sản xuất nhôm?
A. Boxit.
B. Đolomit.
C. Apatit.
D. Manhetit.
Câu 14. Trong phân tử nhôm clorua, tỉ lệ số nguyên tử nhôm và nguyên tử clo là
A. 3 : 1.
B. 2 : 1.
C. 1 : 3.
D. 1 : 2.
Câu 15. Trên bề mặt của đồ vật làm bằng nhôm được phủ kín một lớp hợp chất X rất mỏng, bền và mịn, không cho nước và khí thấm qua. Chất X là
A. nhôm clorua.
B. nhôm oxit.
C. nhôm sunfat.
D. nhôm nitrate.
Câu 16. Phèn chua được dùng trong ngành thuộc da, công nghiệp giấy, chất cầm màu trong công nghiệp nhuộm, chất làm trong nước. Công thức hóa học của phèn chua viết gọn là
A. KAl(SO4)2.12H2O.
B. NaAl(SO4)2.12H2O.
C. NH4Al(SO4)2.12H2O.
D. LiAl(SO4)2.12H2O.
Mức độ: Thông hiểu
Câu 17. Để bảo vệ vỏ tàu biển làm bằng thép, người ta gắn vào vỏ tàu (phần ngâm dưới nước) những tấm kim loại
A. Zn.
B. Cu.
C. Pb.
D. Ag.
Câu 18. Dung dịch Na2CO3 tác dụng với dung dịch chất nào sau đây thu được kết tủa?
A. HCl.
B. KCl.
C. NaNO3.
D. CaCl2.
Câu 19. Dung dịch nào sau đây làm phenolphtalein chuyển màu hồng?
A. NaCl.
B. HCl.
C. NaOH.
D. KNO3.
Câu 20. Chất nào sau đây không bị nhiệt phân?
A. Ca(HCO3)2.
B. CaO.
C. Mg(HCO3)2.
D. CaCO3.
Câu 21. Cho dãy các chất: NaOH, NaCl, Na2SO4, Ca(OH)2. Số chất tác dụng được với dung dịch Ba(HCO3)2 là
A. 1.
B. 2.
C. 3.
D. 4.
Câu 22. Chất nào sau đây được dùng để làm mềm nước có tính cứng tạm thời?
A. Na2CO3.
B. NaCl.
C. HCl.
D. H2SO4.
Câu 23. Hấp thụ hoàn toàn 2,24 lít khí CO2 (đktc) vào dung dịch Ba(OH)2 dư, thu được m gam kết tủa. Giá trị của m là
A. 29,55.
B. 19,70.
C. 39,40.
D. 59,10.
Câu 24. Hòa tan hoàn toàn 4,05 gam Al trong dung dịch KOH dư, thu được V lít khí H2 (đktc). Giá trị của V là
A. 3,36.
B. 5,04.
C. 10,08.
D. 6,72.
Câu 25. Khử hoàn toàn 16 gam Fe2O3 cần dùng vừa đủ m gam Al. Giá trị của m là
A. 2,7.
B. 5,4.
C. 11,2.
D. 5,6.
Câu 26. Chất nào sau đây tan trong dung dịch NaOH?
A. Al(OH)3.
B. MgO.
C. Fe2O3.
D. Mg(OH)2.
Câu 27. Phát biểu nào sau đây sai?
A. Kim loại Al tan được trong dung dịch KOH.
B. Kim loại Ca không tan trong nước.
C. Al(OH)3 là một hiđroxit lưỡng tính.
D. Dung dịch HCl hòa tan được MgO.
Câu 28. Cho các phát biểu sau:
(a) Để làm mất tính cứng tạm thời của nước, người ta dùng một lượng vừa đủ Ca(OH)2.
(b) Thành phần chính của vỏ và mai các loài ốc, sò, hến, mực là canxi carbonate.
(c) Kim loại xesi được dùng làm tế bào quang điện.
(d) Sử dụng nước cứng trong ăn uống gây ngộ độc.
Số phát biểu đúng là
A. 3.
B. 1.
C. 4.
D. 2.
PHẦN TỰ LUẬN:
Mức độ: Vận dụng.
Bài 29 (1 điểm). Viết phương trình hóa học các phản ứng trong sơ đồ chuyển hóa sau:
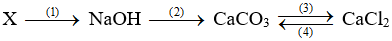
Bài 30 (1 điểm). Hòa tan m gam kim loại Na vào nước, thu được 200 ml dung dịch X và 0,448 lít khí (đktc). Thêm 100 ml dung dịch HCl 0,15M vào 100 ml dung dịch X. Cô cạn dung dịch sau phản ứng, thu được chất rắn khan Y.
a) Viết phương trình hóa học các phản ứng xảy ra. Tính m.
b) Tính khối lượng của Y.
Mức độ: Vận dụng cao
Bài 31 (0,5 điểm). Cho hỗn hợp X gồm Na và Ba (có cùng số mol) vào H2O thu được dung dịch Y và 0,336 lít khí (đktc). Cho Y vào 125 ml dung dịch gồm H2SO4 0,1M và CuSO4 0,1M. Khi các phản ứng xảy ra hoàn toàn, thu được m gam kết tủa Z.
a) Tính số mol của mỗi kim loại trong X.
b) Tính m.
Bài 32 (0,5 điểm). Cho 4 chất rắn dạng bột: BaSO4, CaCO3, Na2CO3, NaCl. Chỉ dùng thêm H2O và dung dịch HCl, trình bày cách nhận biết 4 chất trên.
Xem thêm tài liệu ma trận đề thi môn Hóa học lớp 12 chọn lọc, có đáp án hay khác:
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Đề thi lớp 1 (các môn học)
- Đề thi lớp 2 (các môn học)
- Đề thi lớp 3 (các môn học)
- Đề thi lớp 4 (các môn học)
- Đề thi lớp 5 (các môn học)
- Đề thi lớp 6 (các môn học)
- Đề thi lớp 7 (các môn học)
- Đề thi lớp 8 (các môn học)
- Đề thi lớp 9 (các môn học)
- Đề thi lớp 10 (các môn học)
- Đề thi lớp 11 (các môn học)
- Đề thi lớp 12 (các môn học)
- Giáo án lớp 1 (các môn học)
- Giáo án lớp 2 (các môn học)
- Giáo án lớp 3 (các môn học)
- Giáo án lớp 4 (các môn học)
- Giáo án lớp 5 (các môn học)
- Giáo án lớp 6 (các môn học)
- Giáo án lớp 7 (các môn học)
- Giáo án lớp 8 (các môn học)
- Giáo án lớp 9 (các môn học)
- Giáo án lớp 10 (các môn học)
- Giáo án lớp 11 (các môn học)
- Giáo án lớp 12 (các môn học)






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

