Trắc nghiệm Hóa 10 Chân trời sáng tạo Bài 13 (có đáp án): Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học
Với 18 bài tập trắc nghiệm Hóa 10 Bài 13: Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học sách Chân trời sáng tạo có đáp án và lời giải chi tiết đầy đủ các mức độ, có đúng sai, trả lời ngắn sẽ giúp học sinh ôn luyện trắc nghiệm Hóa học 10.
Trắc nghiệm Hóa 10 Chân trời sáng tạo Bài 13 (có đáp án): Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học
PHẦN I. TRẮC NGHIỆM NHIỀU PHƯƠNG ÁN LỰA CHỌN
Câu 1. Cho các phát biểu sau
(1) Phản ứng tỏa nhiệt là phản ứng hóa học trong đó có sự giải phóng nhiệt năng ra môi trường.
(2) Phản ứng thu nhiệt là phản ứng hóa học trong đó có sự hấp thụ nhiệt năng từ môi trường.
(3) Phản ứng tỏa nhiệt là phản ứng hóa học trong đó có sự hấp thụ nhiệt năng từ môi trường.
(4) Phản ứng thu nhiệt là phản ứng hóa học trong đó có sự giải phóng nhiệt năng ra môi trường.
Các phát biểu đúng là
A. (1) và (2);
B. (1) và (4);
C. (2) và (3);
D. (3) và (4).
Câu 2. Phản ứng nào trong các phản ứng dưới đây là phản ứng thu nhiệt?
A. Vôi sống tác dụng với nước: CaO + H2O ⟶Ca(OH)2
B. Đốt cháy than: C + O2 CO2
C. Đốt cháy cồn: C2H5OH + 3O2 2CO2 + 3H2O
D. Nung đá vôi: CaCO3 CaO + CO2
Câu 3. Điều kiện chuẩn là điều kiện ứng với
A. 1 bar (đối với chất khí);
B. nồng độ 1 mol/L (đối với chất tan trong dung dịch);
C. nhiệt độ thường được chọn là 25° C (298 K);
D. Cả A, B và C.
Câu 4. Nhiệt kèm theo phản ứng trong điều kiện chuẩn là
A. enthalpy chuẩn (hay nhiệt phản ứng chuẩn) của phản ứng đó, kí hiệu là ;
B. biến thiên enthalpy chuẩn (hay nhiệt phản ứng chuẩn) của phản ứng đó, kí hiệu là ;
C. biến thiên enthalpy chuẩn (hay nhiệt phản ứng chuẩn) của phản ứng đó, kí hiệu là ;
D. enthalpy chuẩn (hay nhiệt phản ứng chuẩn) của phản ứng đó, kí hiệu là .
Câu 5. Phương trình nhiệt hóa học là
A. phương trình phản ứng hóa học xảy ra trong điều kiện cung cấp nhiệt độ;
B. phương trình phản ứng hóa học có kèm theo nhiệt phản ứng;
C. phương trình phản ứng hóa học có kèm theo nhiệt phản ứng và trạng thái của các chất đầu và sản phẩm;
D. phương trình phản ứng hóa học tỏa nhiệt ra môi trường.
Câu 6. Cho 2 phương trình nhiệt hóa học sau:
C (s) + H2O (g) CO (g) + H2 (g) = + 131,25 kJ (1)
CuSO4 (aq) + Zn (s) ZnSO4 (aq) + Cu (s) = −231,04 kJ (2)
Khẳng định đúng là
A. Phản ứng (1) là phản ứng tỏa nhiệt, phản ứng (2) là phản ứng thu nhiệt;
B. Phản ứng (1) là phản ứng thu nhiệt, phản ứng (2) là phản ứng tỏa nhiệt;
C. Phản ứng (1) và phản ứng (2) là phản ứng thu nhiệt;
D. Phản ứng (1) và phản ứng (2) là phản ứng tỏa nhiệt.
Câu 7. Enthalpy tạo thành của một chất () là nhiệt kèm theo phản ứng tạo thành
A. 1 gam chất đó từ các đơn chất bền nhất;
B. 1 lít chất đó từ các đơn chất dạng bền nhất;
C. 1 mol chất đó từ các đơn chất bền nhất;
D. 1 mol chất đó từ các hợp chất bền nhất.
Câu 8. Cho phản ứng sau:
S (s) + O2 (g) SO2 (g) (SO2, g) = – 296,8 kJ/mol
Khẳng định sai là
A. (SO2, g) = – 296,8 kJ/mol là lượng nhiệt tỏa ra khi tạo ra 1 mol SO2 (g) từ đơn chất S (s) và O2 (g), đây là các đơn chất bền nhất ở điều kiện chuẩn;
B. Ở điều kiện chuẩn (O2, g) = 0;
C. Ở điều kiện chuẩn (S, s) = 0;
D. Hợp chất SO2(g) kém bền hơn về mặt năng lượng so với các đơn chất bền S (s) và O2 (g).
Câu 9. Cho (Fe2O3, s) = − 825,5 kJ/mol. Biết 1 J = 0,239 cal. Enthalpy tạo thành chuẩn theo đơn vị (kcal) của Fe2O3 (s) là
A. 197,2945 kJ/mol;
B. − 197,2945 kJ/mol;
C. 3454 kJ/mol;
D. − 3454 kJ/mol.
Câu 10. Cho phản ứng: Na (s) + Cl2 (g) ⟶NaCl (s) có (NaCl, s) = − 411,1 kJ/mol.
Nếu chỉ thu được 0,5 mol NaCl (s) ở điều kiện chuẩn thì lượng nhiệt tỏa ra là
A. 411,1 kJ;
B. 25,55 kJ;
C. 250,55 kJ;
D. 205,55 kJ.
Câu 11. Cho phản ứng: N2 (g) + 3H2 (g) ⟶ 2NH3 (g)
Ở điều kiện chuẩn, cứ 1 mol N2 phản ứng hết sẽ tỏa ra 91,8 kJ. Enthalpy tạo thành chuẩn của NH3 là
A. = − 91,8 kJ/mol;
B. = 91,8 kJ/mol;
C. = − 45,9 kJ/mol;
D. = 45,9 kJ/mol.
Câu 12. Cho biết phản ứng tạo thành 2 mol HCl (g) ở điều kiện chuẩn tỏa ra 184,62 kJ:
H2 (g) + Cl2 (g)⟶ 2HCl (g) (*)
Những phát biểu nào dưới đây đúng?
(1) Enthalpy tạo thành chuẩn của HCl (g) là − 184,62 kJ/mol.
(2) Biến thiên enthalpy chuẩn của phản ứng (*) là − 184,62 kJ.
(3) Enthalpy tạo thành chuẩn của HCl (g) là – 92,31 kJ/mol.
(4) Biến thiên enthalpy chuẩn của phản ứng (*) là 184,62 kJ.
A. (1) và (2);
B. (2) và (3);
C. (3) và (4);
D. (1) và (4).
Câu 13. Cho các phản ứng dưới đây:
(1) CO (g) + O2 (g) ⟶ CO2 (g) = − 283 kJ
(2) C (s) + H2O (g) CO (g) + H2 (g) = + 131,25 kJ
(3) H2 (g) + F2 (g) ⟶ 2HF (g) = − 546 kJ
(4) H2 (g) + Cl2 (g)⟶ 2HCl (g) = − 184,62 kJ
Phản ứng xảy ra thuận lợi nhất là
A. Phản ứng (1);
B. Phản ứng (2);
C. Phản ứng (3);
D. Phản ứng (4).
Câu 14. Phương trình nhiệt hóa học giữa nitrogen và oxygen như sau:
N2 (g) + O2 (g) ⟶ 2NO (g) = +180 kJ
Kết luận nào sau đây đúng?
A. Nitrogen và oxygen phản ứng mạnh hơn khi ở nhiệt độ thấp;
B. Phản ứng tỏa nhiệt;
C. Phản ứng xảy ra thuận lợi hơn ở điều kiện thường;
D. Phản ứng hóa học xảy ra có sự hấp thụ nhiệt năng từ môi trường.
Câu 15. Biến thiên enthalpy của một phản ứng được ghi ở sơ đồ dưới đây. Kết luận nào sau đây là đúng?
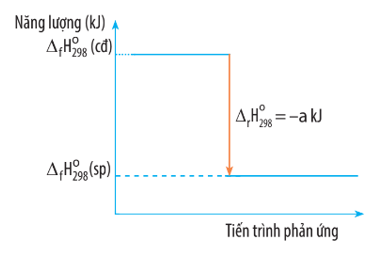
A. Phản ứng tỏa nhiệt;
B. Năng lượng chất tham gia phản ứng nhỏ hơn năng lượng sản phẩm;
C. Biến thiên enthalpy của phản ứng là a kJ/mol;
D. Phản ứng thu nhiệt.
PHẦN II. TRẮC NGHIỆM ĐÚNG – SAI
Câu hỏi. Khi các phản ứng hóa học xảy ra thường có sự trao đổi nhiệt với môi trường, làm thay đổi nhiệt độ của môi trường.
a. Phản ứng tỏa nhiệt là phản ứng giải phóng năng lượng dưới dạng nhiệt.
b. Phản ứng thu nhiệt là phản ứng hấp thụ năng lượng dưới dạng nhiệt.
c. Khi than, củi cháy không khí xung quanh ấm hơn do phản ứng tỏa nhiệt.
d. Pha viên C sủi vitamin C vào nước, khi viên C sủi tan thấy cốc nước mát hơn là do phản ứng thu nhiệt.
PHẦN III. TRẮC NGHIỆM TRẢ LỜI NGẮN
Câu 1. Dựa vào phương trình nhiệt hóa học của các phản ứng sau:
(1) CS2(l) + 3O2(g) CO2(g) + 2SO2(g);
(2) CO2(g) CO(g) + ½ O2(g);
(3) 2Na(s) + 2H2O(l) 2NaOH(aq) + H2(g);
(4) ZnSO4(s) ZnO(s) + SO2(g);
(5) 2SO2(g) + O2(g) 2SO3(g);
Liệt kê các phản ứng thu nhiệt theo số thứ tự tăng dần (ví dụ: 123, 25,...).
Câu 2. Phân tử hemoglobin(Hb) trong máu nhận O2 ở phổi để chuyển thành HbO2. Chất này theo máu tới các bộ phận cơ thể, tại đó HbO2 lại chuyển thành Hb và O2( để cung cấp O2 cho các hoạt động sinh hóa cần thiết trong cơ thể). Nếu trong không khí có lẫn carbon monoxide(CO), cơ thể nhanh chóng bị ngộ độc. Cho các số liệu thực nghiệm sau:
(1) Hb + O2 HbO2;
(2) Hb + CO НbСО;
(3) HbO2 + CO HbCO + O2;
(4) HbCO + O2 HbO2 + CO;
Liệt kê các phản ứng tỏa nhiệt theo số thứ tự tăng dần (ví dụ: 134, 24,...).
Xem thêm bài tập trắc nghiệm Hóa học lớp 10 Chân trời sáng tạo có đáp án hay khác:
Trắc nghiệm Hóa học 10 Bài 14: Tính biến thiên enthalpy của phản ứng hóa học
Trắc nghiệm Hóa học 10 Bài 15: Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng
Trắc nghiệm Hóa học 10 Bài 16: Các yếu tố ảnh hưởng đến tốc độ phản ứng hóa học
Trắc nghiệm Hóa học 10 Bài 17: Tính chất vật lí và hóa học các đơn chất nhóm VIIA
Trắc nghiệm Hóa học 10 Bài 18: Hydrogen halide và một số phản ứng của ion halide
Xem thêm các tài liệu học tốt lớp 10 hay khác:
- Giải sgk Hóa học 10 Chân trời sáng tạo
- Giải Chuyên đề Hóa học 10 Chân trời sáng tạo
- Giải SBT Hóa học 10 Chân trời sáng tạo
- Giải lớp 10 Chân trời sáng tạo (các môn học)
- Giải lớp 10 Kết nối tri thức (các môn học)
- Giải lớp 10 Cánh diều (các môn học)
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Soạn văn 10 (hay nhất) - CTST
- Soạn văn 10 (ngắn nhất) - CTST
- Soạn văn 10 (siêu ngắn) - CTST
- Giải Toán 10 - CTST
- Giải Tiếng Anh 10 Global Success
- Giải Tiếng Anh 10 Friends Global
- Giải sgk Tiếng Anh 10 iLearn Smart World
- Giải sgk Tiếng Anh 10 Explore New Worlds
- Giải sgk Vật lí 10 - CTST
- Giải sgk Hóa học 10 - CTST
- Giải sgk Sinh học 10 - CTST
- Giải sgk Địa lí 10 - CTST
- Giải sgk Lịch sử 10 - CTST
- Giải sgk Kinh tế và Pháp luật 10 - CTST
- Giải sgk Hoạt động trải nghiệm 10 - CTST






 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

