Cách giải bài tập Phản ứng oxi hóa hoàn toàn Anđehit, ketone, carboxylic acid (hay, chi tiết)
Bài viết Cách giải bài tập Phản ứng oxi hóa hoàn toàn Anđehit, ketone, carboxylic acid với phương pháp giải chi tiết giúp học sinh ôn tập, biết cách làm bài tập Phản ứng oxi hóa hoàn toàn Anđehit, ketone, carboxylic acid.
Cách giải bài tập Phản ứng oxi hóa hoàn toàn Anđehit, ketone, carboxylic acid (hay, chi tiết)
Thi online Hóa 11 KNTTThi online Hóa 11 CDThi online Hóa 11 CTST
A. Phương pháp giải & Ví dụ minh họa
- Phản ứng đốt cháy andehit, ketone
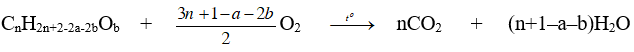
(a là số liên kết π ở gốc hydrocarbon?
+ Đối với anđehit/ketone no, đơn chức (a=0, b=1) ta có :
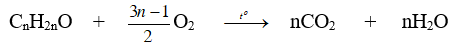
⇒ Nếu nH2O = nCO2 ⇒ andehit/ketone ban đầu phải là andehit/ketone no đơn chức.
+ Đối với andehit/ketone không no (có một liên kết pi) đơn chức ta luôn có
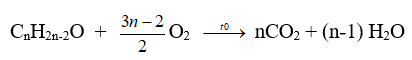
⇒ nandehit/ketone = nCO2 – nH2O
+ Nếu nCO2 > nH2O ⇒ andehit/ketone ban đầu là andehit/ketone no đa chức hoặc là andehit/ketone chưa no đơn chức hoặc là andehit/ketone chưa no đa chức.
+ Không bao giờ có nCO2 < nH2O
- Phương trình đốt cháy carboxylic acid
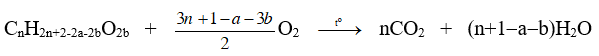
* Nhận xét :
+ Nếu a =0; b = 1 (carboxylic acid no, đơn chức) thì nCO2 = nH2O
+ nO(axit) + nO(O2) = nO(CO2) + nO(H2O)
+ nCnH2n+2-2a-2bO2b =
+ Số nguyên tử cacbon trong axit =
Ví dụ minh họa
Bài 1: Hiđro hoá hoàn toàn m gam hỗn hợp X gồm hai anđehit no, đơn chức, mạch hở, kế tiếp nhau trong dãy đồng đẳng thu được (m + 1) gam hỗn hợp hai ancol. Mặt khác, khi đốt cháy hoàn toàn cũng m gam X thì cần vừa đủ 17,92 lít khí O2 (ở đktc). Giá trị của m là :
Lời giải:
Theo định luật bảo toàn khối lượng ta có :
mH2 = (m+1) – m = 1, nH2 = 0,5 mol
Đặt công thức trung bình của hai anđehit là 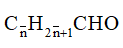
Phương trình phản ứng :
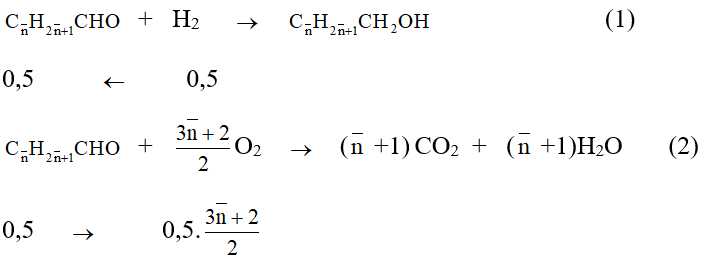
Theo (1), (2) và giả thiết ta có:
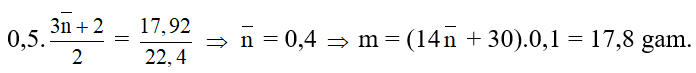
Bài 2: Hiđro hoá hoàn toàn hỗn hợp M gồm hai anđehit X và Y no, đơn chức, mạch hở, kế tiếp nhau trong dãy đồng đẳng (MX < MY), thu được hỗn hợp hai ancol có khối lượng lớn hơn khối lượng M là 1 gam. Đốt cháy hoàn toàn M thu được 30,8 gam CO2. Công thức và phần trăm khối lượng của X lần lượt là :
Lời giải:
Theo định luật bảo toàn khối lượng ta có:
mH2 = (m+1) – m = 1, 0,5 mol
Đặt công thức trung bình của hai anđehit là CnH2n+1CHO
Phương trình phản ứng:
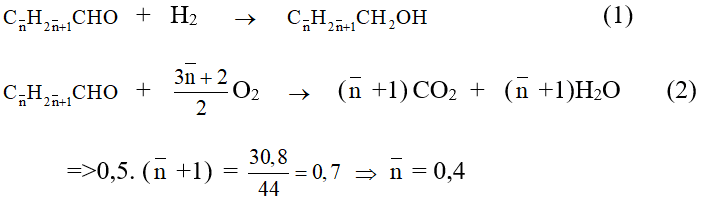
Hai anđehit có công thức là HCHO và CH3CHO.
Áp dụng sơ đồ đường chéo cho số nguyên tử C trung bình của hai anđehit :
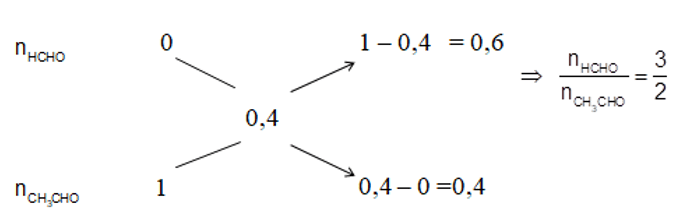
⇒ % về khối lượng của HCHO là : %HCHO = 50,56%
Bài 3: Đốt cháy hoàn toàn 0,1 mol một carboxylic acid đơn chức cần vừa đủ V lít O2 (đktc), thu được 0,3 mol CO2 và 0,2 mol H2O. Giá trị của V là :
Lời giải:
Axit cacbonxylic đơn chức có 2 nguyên tử O nên có thể đặt là ROOH.
Áp dụng định luật bảo toàn nguyên tố đối với oxi ta có :
nO(ROOH) + nO(O2) - nO(CO2) + nO(H2O) ⇒ 0,1.2 + nO(O2) = 0,3.2 + 0,2.1
⇒ nO(O2) = 0,6 mol → nO2 = 0,3 mol ⇒ VO2 = 6,72 lít.
Bài 4: Hỗn hợp X gồm acetic acid, formic acid và oxalic acid. Khi cho m gam X tác dụng với NaHCO3 (dư) thì thu được 15,68 lít khí CO2 (đktc). Mặt khác, đốt cháy hoàn toàn m gam X cần 8,96 lít khí O2 (đktc), thu được 35,2 gam CO2 và y mol H2O. Giá trị của y là :
Lời giải:
Phản ứng của hỗn hợp X với NaHCO3 :
-COOH + HCO3- → -COO- + CO2 + H2O (1)
Theo (1) và giả thiết ta suy ra : nO(axit) = 2n -COOH = 2nCO2 =1,4 mol
Áp dụng định luật BTNT đối với O, ta có :
nO(oxit) + nO(O2) = nO(CO2) + nO(H2O) ⇒ nO(H2O) =1,4 + 2.0,4 - 2.0,8 = 0,6 ⇒ nH2O = 0,6 mol
Bài 5: Trung hòa 3,88 gam hỗn hợp X gồm hai carboxylic acid no, đơn chức, mạch hở bằng dung dịch NaOH, cô cạn toàn bộ dung dịch sau phản ứng thu được 5,2 gam muối khan. Nếu đốt cháy hoàn toàn 3,88 gam X thì thể tích oxi (đktc) cần dùng là :
Lời giải:
Đặt công thức chung của hai axit là CnH2nO2
Phương trình phản ứng của X với NaOH :
–COOH + NaOH → –COONa + H2O (1)
Theo (1) và phương pháp tăng giảm khối lượng, ta có :
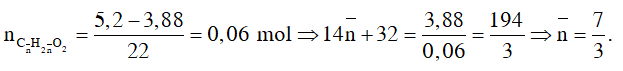
Phương trình phản ứng đốt cháy X :
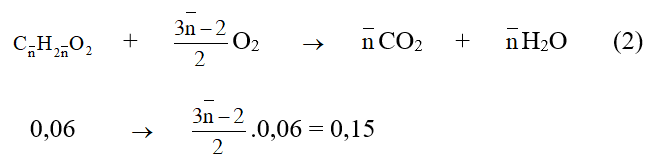
Vậy thể tích oxi (đktc) cần dùng là : V = 0,15.22,4 = 3,36 lít.
B. Bài tập trắc nghiệm
Bài 1: Oxi hóa 17,4 gam một anđehit đơn chức được 16,65 gam axit tương ứng (H = 75%). Anđehit có công thức phân tử là :
A. CH2O. B. C2H4O. C. C3H6O. D. C3H4O.
Lời giải:
Đáp án: C
–CHO + 1/2 O2 −tº, xt→ –COOH
mRCHO = 17,4.75% = 13,05 g , nO2 = 0,1125 mol
M(RCHO) = R + 29 = 58 ⇒ R = 29 (R:C2H5-) ⇒ C2H5CHO.
Bài 2: Oxi hóa 1,8 gam HCHO thành axit với hiệu suất H% thu được hỗn hợp X. Cho X tham gia phản ứng tráng gương thu được 16,2 gam Ag. Giá trị của H là :
A. 60. B. 75. C. 62,5. D. 25.
Lời giải:
Đáp án: B
Gọi số mol HCHO bị oxi hóa thành axit là x, số mol HCHO dư là y.
nHCHO = x+y = 1,8/30
nAg = 2x + 4y = 16,2/108 = 0,15
Giải hệ pt ⇒ x= 0,045 mol, y = 0,025 mol
H= 0,045/0,06= 75%
Bài 3: Một hỗn hợp gồm andehit acrylic và một andehit đơn chức X. Đốt cháy hoàn toàn 1,72 gam hỗn hợp trên cần 2,296 lít khí oxi (đktc). Cho toàn bộ sản phẩm chát hấp thụ hết vào dung dịch Ca(OH)2 dư thu được 8,5 gam kết tủa. Công thức cấu tạo của X là:
A.HCHO B. C2H5CHO C. CH3CHO D. C3H5CHO
Lời giải:
Đáp án: C
nCO2 = 0,085 mol; nO2 = 0,1025 mol;
mH2O = 1,72 + 0,1025.32 – 0,085.44 = 1,26 ⇒ nH2O = 0,07 mol;
mO(X) = 1,72 – 0,085.12 – 0,07.2 = 0,56 g ⇒ nO = 0,035
⇒ nandehit = 0,035 mol ⇒ Mandehit = 49 ⇒ X là andehit no đơn chức : CnH2nO;
Giải hệ 3 ẩn:
x+ y = 0,035
3x + ny = 0,085
56x + (14n+16)y = 1,72 ⇒ n = 2
Bài 4: Đốt cháy hoàn toàn một hợp chất hữu cơ X, thu được 0,351 gam H2O và 0,4368 lít khí CO2 (ở đktc). Biết X có phản ứng với Cu(OH)2 trong môi trường kiềm khi đun nóng. Chất X là
A. CH3COCH3. B. O=CH-CH=O.
C. CH2=CH-CH2-OH. D. C2H5CHO
Lời giải:
Đáp án: D
nH2O = 0,351/18 = 0,0195 mol; nCO2 = 0,0195 ⇒ anđehit no đơn chức
Bài 5: Hỗn hợp Y gồm 2 anđehit đồng đẳng kế tiếp. Đốt 2,62g hỗn hợp Y tạo 2,912 lit CO2 (đktc) và 2,34g H2O. Công thức 2 anđehit là:
A. HCHO và C2H4O B. C3H4O và C4H6O
C. C2H4O và C3H6O D.C3H6O và C4H8O
Lời giải:
Đáp án: C
nH2O = 2,34/18 = 0,13 mol; nCO2 = 2,912/22,4 = 0,13 mol ⇒ andehit no đơn chức mạch hở.
CT của Y: CnH2nO; MY = 2,62n/0,13 ⇒ n = 2,6 ⇒ 2 andehit là C2H4O và C3H6O
Bài 6: Đốt cháy hoàn toàn 7,2g hợp chất hữu cơ A thu được 0,4 mol CO2 và 0,4 mol H2O. Biết A chỉ chứa một loại nhóm chức và 0,05 mol A tham gia phản ứng tráng gương thì tạo ra 0,1 mol Ag. Công thức cấu tạo thu gọn của A là
A. C3H7CHO B. CH3CHO C. C2H5CHO D. C2H3CHO
Lời giải:
Đáp án: A
A là andehit no đơn chức; MA = 7,2n/0,4 ⇒ n =4
Bài 7: Đốt cháy hết 8,8 gam hỗn hợp gồm 1 alkanalA và 1 alkanol B (có cùng số nguyên tử cacbon) thu được 19,8gam CO2 và 9 gam H2O. Tìm công thức phân tử của A
A. CH3CHO B. CH3-CH2-CHO C. HCHO D. (CH3)2CH-CHO
Lời giải:
Đáp án: B
CnH2nO + (3n-1)/2 → O2 nCO2 + n H2O
CnH2n+2O + (3n-1)/2 O2 → nCO2 + (n+1) H2O
nCO2 = 0,45 mol; nH2O = 0,5 mol ⇒ nB = 0,05 mol;
mO (hh) = 8,8 – 0,45.12 – 0,5.2 = 2,4 g ⇒ n(O)hh = 0,15 mol ⇒ nA = 0,1 mol
⇒ n.0,15 = 0,45 ⇒ n = 3
Bài 8: Đốt cháy hỗn hợp 2 anđehit no, đơn chức thu được 0,4 mol CO2. Hidro hóa hoàn toàn 2 anđehit này cần 0,2 mol H2 thu được hỗn hợp 2 rượu no, đơn chức. Đốt cháy hoàn toàn hỗn hợp 2 rượu thì số mol H2O thu được là:
A. 0,4 mol B. 0,6mol C. 0,8 mol D. 0,3 mol
Lời giải:
Đáp án: B
CnH2nO + (3n-1)/2 O2 → nCO2 + n H2O
CnH2nO + H2 −tº, Ni→ CnH2n+2O
CnH2n+2O + (3n-1)/2 O2 → nCO2 + (n+1) H2O
⇒ nH2O thu đc = nCO2 + nH2 = 0,4 + 0,2 = 0,6 mol.
Bài 9: Đốt cháy hoàn toàn 2,22 gam một axit hữu cơ no A thu được 1,62 gam H2O. A là
A. C3H7COOH. B. C2H5COOH.
C. HCOOH. D. CH3COOH.
Lời giải:
Đáp án: B
CnH2nO2 + (3n-2)/2 O2 → n CO2 + n H2O
nH2O = 1,62/18 = 0,09 mol ⇒ nA = 0,09/n ⇒ MA = 74/3 ⇒ n = 3
Bài 10: Đốt cháy hoàn toàn 0,1 mol axit đơn chức cần V lít O2 ở đktc, thu được 0,3 mol CO2 và 0,2 mol H2O. Giá trị V là
A. 6,72 lít. B. 8,96 lít. C. 4,48 lít. D. 5,6 lít.
Lời giải:
Đáp án: A
nO(O2) = 0,3.2 + 0,2 – 0,1.2 = 0,6 ⇒ nO2 = 0,3 ⇒ V = 6,72 lít
Bài 11: Đốt cháy hoàn toàn 4,38 gam một axit E no, mạch thẳng thu được 4,032 lít CO2 (đkc) và 2,7 gam H2O. CTCT của E là
A. CH3COOH. B. C17H35COOH.
C. HOOC(CH2)4COOH. D. CH2=C(CH3)COOH.
Lời giải:
Đáp án: C
CnH2n+2-2aOa + O2 → n CO2 + (n +1 – a) H2O
nCO2 = 0,18 mol; nH2O = 2,7/18 = 0,15 mol; nCO2 > nH2O; E no đa chức mạch thẳng; nE = 0,03 mol ⇒ ME = 146
Bài 12: Đốt cháy hoàn toàn 0,44 gam một axit hữu cơ, sản phẩm cháy được hấp thụ hoàn toàn vào bình 1 đựng P2O5 và bình 2 đựng KOH. Sau thí nghiệm thấy khối lượng bình 1 tăng 0,36g và bình 2 tăng 0,88g. CTPT của axit là:
A. C2H4O2 B. C3H6O2 C. C5H10O2 D. C4H8O2.
Lời giải:
Đáp án: D
nCO2 = nH2O = 0,02 mol ⇒ axit no, đơn chức CnH2nO2 ⇒ naxit = 0,02/n
⇒ Maxit = 22n ⇒ n = 4
Bài 13: Đốt cháy 4,09g hỗn hợp A gồm hai carboxylic acid là đồng đẳng kế tiếp nhau trong dãy đồng đẳng của acetic acid người ta thu được 3,472 lít khí CO2 (đktc). Công thức cấu tạo của các axit trong hỗn hợp phải là:
A. HCOOH và CH3COOH B. CH3COOH và C2H5COOH
C. C2H5COOH và (CH3)2CHCOOH D. C2H5COOH và CH3CH2CH2COOH.
Lời giải:
Đáp án: B
nCO2 = 0,155 mol; nA = 0,155/n ⇒ MA = 26,4n ⇒ n = 2,6
Bài 14: Đốt cháy hoàn toàn 1,18 gam một axit hữu cơ A no, sản phẩm sau phản ứng được hấp thụ hoàn toàn vào dung dịch Ca(OH)2 dư thì thu được 50g kết tủa và khối lượng bình tăng lên 29,2 gam. Mặt khác để trung hoà 0,15 mol A thì cần vừa đủ 300 ml dung dịch NaOH 1M. CTCT của A biết A có cấu tạo mạch thẳng:
A. HOOCCH2CH2COOH B. HOOCCH(CH3)COOH
C. CH3–COOH D. HOOC–COOH
Lời giải:
Đáp án: A
nA = ½ nNaOH ⇒ A là axit 2 chức; nCO2 = 0,5 mol
⇒ nH2O = (29,2-0,5.44)/18 = 0,4 mol ⇒ naxit = 0,1 mol
⇒ Maxit = 118 ⇒ A là: HOOCCH2CH2COOH
Bài 15: Một axit hữu cơ no A có khối lượng 10,5g tương ứng với 0,175 mol. Đốt cháy hoàn toàn A rồi cho sản phẩm qua nước vôi trong dư, thu được 52,5 g kết tủa. Tìm CTCT
A. C2H5COOH B. HOOC–COOH
C. CH3COOH D. HCOOH
Lời giải:
Đáp án: C
nCO2 = 52,5/100 = 0,525 mol;
CnH2n+2-2aO2a + (3n+1-a)/2O2 → n CO2 + (n +1 – a) H2O
⇒ n = 0,525/0,175 = 3
M(TB)= 10,5/0,175 = 60 = 14.3 + 2 – 2a + 16a ⇒ a = 2
⇒ axit đơn chức ⇒ CH3COOH
C. Bài tập tự luyện
Câu 1: Đốt cháy hoàn toàn 1,46 gam hỗn hợp 2 aldehyde no, đơn chức đồng đẳng kế tiếp thu được 1,7354 lít CO2 (đkc). CTPT của 2 aldehyde là
A. CH3CHO và C2H5CHO.
B. HCHO và CH3CHO.
C. C2H5CHO và C3H7CHO.
D. Kết quả khác.
Câu 2: Đốt cháy hoàn toàn 0,35 gam một aldehyde đơn chức X thu được 0,4958 lít CO2 (đkc) và 0,27 gam nước. X có công thức cấu tạo nào sau đây?
A. CH2=CH−CH2−CHO.
B. CH3−CH=CH−CHO.
C. CH2=C(CH3) −CHO.
D. A, B, C đều đúng.
Câu 3: Trong một bình kín chứa hơi chất hữu cơ X (có dạng CnH2nO2) mạch hở và O2 (số mol O2 gấp đôi số mol cần cho phản ứng cháy) ở 139℃, áp suất trong bình là 0,8 atm. Đốt cháy hoàn toàn X sau đó đưa về nhiệt độ ban đầu, áp suất trong bình lúc này là 0,95 atm. X có CTPT là
A. C3H6O2.
B. C2H4O2.
C. C4H8O2.
D. CH2O2.
Câu 4: Đốt cháy hoàn toàn 1,52 gam hỗn hợp formic acid và acetic acid người ta thu được 0,9916 lít CO2 (đkc). Nếu lấy lượng hỗn hợp acid trên rồi thực hiện phản ứng tráng bạc thì khối lượng bạc thu được tối đa là bao nhiêu?
A. 3,72 (g).
B. 4,05 (g).
C. 4,32 (g).
D. 4,65 (g).
Câu 5: Chia hỗn hợp gồm hai aldehyde no đơn chức thành hai phần bằng nhau:
- Đốt cháy hoàn toàn phần thứ nhất thu được 0,54 gam H2O.
- Phần thứ hai cộng H2 (Ni, t°) thu được hỗn hợp X.
Nếu đốt cháy hoàn toàn X thì thể tích khí CO2 thu được (ở đkc) là
A. 0,12395 (L).
B. 0,7437 (L).
C. 1,85925 (L).
D. 2,479 (L).
Thi online Hóa 11 KNTTThi online Hóa 11 CDThi online Hóa 11 CTST
Xem thêm các dạng bài tập Hóa học lớp 11 có trong đề thi Tốt nghiệp THPT khác:
- Dạng 1: Bài tập về tính chất hóa học của Anđehit, ketone, carboxylic acid
- Dạng 2: Đồng phân, gọi tên Anđehit, ketone, carboxylic acid
- Dạng 3: Phản ứng tráng gương của Anđehit
- Dạng 4: Bài tập về phản ứng cộng H2 của Anđehit
- Dạng 5: Phản ứng oxi hóa không hoàn toàn Anđehit
- Dạng 7: Dạng bài tập tính axit của carboxylic acid
- Dạng 8: Phản ứng ester hóa
- Dạng 9: Điều chế, nhận biết Anđehit, ketone, carboxylic acid
Đã có app VietJack trên điện thoại, giải bài tập SGK, SBT Soạn văn, Văn mẫu, Thi online, Bài giảng....miễn phí. Tải ngay ứng dụng trên Android và iOS.
Theo dõi chúng tôi miễn phí trên mạng xã hội facebook và youtube:Nếu thấy hay, hãy động viên và chia sẻ nhé! Các bình luận không phù hợp với nội quy bình luận trang web sẽ bị cấm bình luận vĩnh viễn.
- Giải Tiếng Anh 11 Global Success
- Giải sgk Tiếng Anh 11 Smart World
- Giải sgk Tiếng Anh 11 Friends Global
- Lớp 11 - Kết nối tri thức
- Soạn văn 11 (hay nhất) - KNTT
- Soạn văn 11 (ngắn nhất) - KNTT
- Giải sgk Toán 11 - KNTT
- Giải sgk Vật Lí 11 - KNTT
- Giải sgk Hóa học 11 - KNTT
- Giải sgk Sinh học 11 - KNTT
- Giải sgk Lịch Sử 11 - KNTT
- Giải sgk Địa Lí 11 - KNTT
- Giải sgk Giáo dục KTPL 11 - KNTT
- Giải sgk Tin học 11 - KNTT
- Giải sgk Công nghệ 11 - KNTT
- Giải sgk Hoạt động trải nghiệm 11 - KNTT
- Giải sgk Giáo dục quốc phòng 11 - KNTT
- Giải sgk Âm nhạc 11 - KNTT
- Lớp 11 - Chân trời sáng tạo
- Soạn văn 11 (hay nhất) - CTST
- Soạn văn 11 (ngắn nhất) - CTST
- Giải sgk Toán 11 - CTST
- Giải sgk Vật Lí 11 - CTST
- Giải sgk Hóa học 11 - CTST
- Giải sgk Sinh học 11 - CTST
- Giải sgk Lịch Sử 11 - CTST
- Giải sgk Địa Lí 11 - CTST
- Giải sgk Giáo dục KTPL 11 - CTST
- Giải sgk Hoạt động trải nghiệm 11 - CTST
- Giải sgk Âm nhạc 11 - CTST
- Lớp 11 - Cánh diều
- Soạn văn 11 Cánh diều (hay nhất)
- Soạn văn 11 Cánh diều (ngắn nhất)
- Giải sgk Toán 11 - Cánh diều
- Giải sgk Vật Lí 11 - Cánh diều
- Giải sgk Hóa học 11 - Cánh diều
- Giải sgk Sinh học 11 - Cánh diều
- Giải sgk Lịch Sử 11 - Cánh diều
- Giải sgk Địa Lí 11 - Cánh diều
- Giải sgk Giáo dục KTPL 11 - Cánh diều
- Giải sgk Tin học 11 - Cánh diều
- Giải sgk Công nghệ 11 - Cánh diều
- Giải sgk Hoạt động trải nghiệm 11 - Cánh diều
- Giải sgk Giáo dục quốc phòng 11 - Cánh diều
- Giải sgk Âm nhạc 11 - Cánh diều

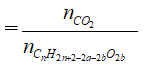





 Giải bài tập SGK & SBT
Giải bài tập SGK & SBT
 Tài liệu giáo viên
Tài liệu giáo viên
 Sách
Sách
 Khóa học
Khóa học
 Thi online
Thi online
 Hỏi đáp
Hỏi đáp

